Перейти к:
Значение показателя артериальной жесткости “сердечно-лодыжечный сосудистый индекс — CAVI” для прогноза сердечно-сосудистых событий в популяционной выборке взрослого городского населения (по материалам исследования ЭССЕ-РФ, Томск)
https://doi.org/10.15829/1728-8800-2021-2967
Аннотация
Цель. Определение прогностической роли показателя артериальной жесткости (АЖ) CAVI (Cardio-Ankle Vascular Index) в отношении сердечно-сосудистых событий (ССС) в популяции взрослого населения РФ на модели данных исследования ЭССЕ-РФ (Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в регионах Российской Федерации), г. Томск.
Материал и методы. Проанализированы данные 1342 человек в возрасте 25-64 (47,3±11,6) лет, которым в рамках исследования ЭССЕ-РФ проведена оценка АЖ на аппарате VaSeraVS-1500 с последующим контрольным обзвоном, в среднем, через 4,7 года. Изучена прогностическая роль показателя CAVI в отношении первичной комбинированной (смерть от сердечно-сосудистых заболеваний (ССЗ), нефатальный инфаркт миокарда (ИМ) или инсульт) и вторичной комбинированной (все ССС) конечных точек (КТ).
Результаты. Выявлено, что наличие в анамнезе ИМ или инсульта (n=52) ассоциировано с повышением частоты ССС с 2,3 до 11,5% — первичная комбинированная КТ (р=0,0003) и с 5% до 23% — вторичная комбинированная КТ (р<0,001). В группе из 1290 человек (без ИМ или инсульта в анамнезе) продемонстрировано, что у мужчин CAVI значимо выше, чем у женщин: 7,4±1,4 vs 7,1±1,3 (р=0,002), несмотря на более молодой возраст: 45,4±11,8 vs 48,0±11,3 лет (р<0,001). Определен критерий риска развития ССС в виде CAVI >7,8 (относительный риск (ОР): 5,06; 95% доверительный интервал (ДИ): 2,32-11,06) (р<0,001) и (ОР: 3,95; 95% ДИ: 2,37-6,58) (р<0,001), который сохраняет свою прогностическую ценность и при поправке на традиционные факторы риска (ОР: 3,13; 95% ДИ: 1,26-7,75) (p=0,014) и (ОР: 2,16; 95% ДИ: 1,18-3,98) (p=0,013) — первичная и вторичная комбинированные КТ, соответственно.
Заключение. Показатель АЖ CAVI имеет существенное независимое прогностическое значение в отношении ССС в популяционной выборке взрослого городского населения г. Томска в возрасте 25-64 лет. Для уточнения сердечно-сосудистого риска может быть рекомендовано проведение объемной сфигмографии с определением CAVI при профилактических и диспансерных осмотрах мужчинам с 35 и женщинам с 45 лет.
Ключевые слова
Для цитирования:
Заирова А.Р., Рогоза А.Н., Ощепкова Е.В., Яровая Е.Б., Куценко В.А., Шальнова С.А., Трубачева И.А., Кавешников В.С., Серебрякова В.Н., Бойцов С.А. Значение показателя артериальной жесткости “сердечно-лодыжечный сосудистый индекс — CAVI” для прогноза сердечно-сосудистых событий в популяционной выборке взрослого городского населения (по материалам исследования ЭССЕ-РФ, Томск). Кардиоваскулярная терапия и профилактика. 2021;20(5):2967. https://doi.org/10.15829/1728-8800-2021-2967
For citation:
Zairova A.R., Rogoza A.N., Oshchepkova E.V., Yarovaya E.B., Kutsenko V.A., Shalnova S.A., Trubacheva I.A., Kaveshnikov V.S., Serebryakova V.N., Boytcov S.A. Contribution of cardio-ankle vascular index to prediction of cardiovascular events in the adult urban population: data from the ESSE-RF study (Tomsk). Cardiovascular Therapy and Prevention. 2021;20(5):2967. (In Russ.) https://doi.org/10.15829/1728-8800-2021-2967
Введение
Показатели артериальной жесткости (АЖ) рассматриваются как интегральные маркеры сердечно-сосудистого риска (ССР) [1][2]. В последние годы широко изучается сердечно-лодыжечный сосудистый индекс CAVI (cardio-ankle vascular index), предложенный японскими авторами [1-3]. Этот показатель АЖ, в отличие от скорости пульсовой волны, является корригированным по уровню артериального давления (АД) в момент измерения и позиционируется как показатель “истинной артериальной жесткости”. Метод объемной сфигмографии (ОС), при котором оценивается CAVI, основан на регистрации сфигмограмм с конечностей с помощью пневмоманжет, является простым и удобным [4], в связи с чем может применяться и в эпидемиологических исследованиях [5]. Показано, что повышенные значения CAVI ассоциированы с коронарным и периферическим атеросклерозом и имеют независимую диагностическую ценность [2][3][6]. Так, некоторыми авторами CAVI >8,9 признается маркером коронарного атеросклероза [6]; рекомендуется вводить CAVI в шкалу для диагностики этого заболевания наряду с традиционными факторами риска (ФР) [7]. За последние 10 лет в ряде работ зарубежных авторов продемонстрирована и независимая прогностическая ценность CAVI в отношении сердечно-сосудистых событий (ССС) в отдельных группах обследованных — у больных с ожирением [8], с метаболическим синдромом [9], сахарным диабетом (СД) 2 типа [10]. Однако в работах других авторов прогностическая значимость CAVI не подтверждается или же статистическая значимость теряется при поправке на традиционные ФР [11-13]. При этом большинство исследований проведены в странах Азии и преимущественно на небольших выборках лиц старшего возраста с высоким риском сердечнососудистых заболеваний (ССЗ). В опубликованном в 2019г метаанализе подчеркивается очевидная необходимость исследований, оценивающих показатель CAVI как прогностический фактор ССС среди населения в целом и в неазиатских странах [14].
Референсные значения показателя CAVI получены для некоторых регионов РФ в рамках эпидемиологического многоцентрового исследования ЭССЕ-РФ (Эпидемология сердечно-сосудистых заболеваний и их факторов риска в регионах Российской Федерации) и других исследований и отражены в согласительном документе российских экспертов по оценке АЖ [2]. Однако данные о прогностическом значении показателя CAVI в популяции РФ отсутствуют.
Цель работы — определение прогностической роли CAVI в отношении ССС по данным проспективного наблюдения в популяции взрослого населения РФ на модели данных исследования ЭССЕРФ (г. Томск).
Материал и методы
В рамках эпидемиологического исследования ЭССЕ-РФ [15] в г. Томск проведена оценка АЖ в случайной популяционная выборке из 1379 человек в возрасте 25-64 лет. До включения в исследование у всех участников было получено письменное информированное согласие. Протокол исследования был одобрен этическим комитетом НИИ кардиологии Томского НИМЦ.
Определение АЖ выполнено методом 4-канальной ОС (рисунок 1) на аппарате VaSeraVS-1500 (Fukuda Denshi, Япония). Обследование проводилось в положении пациента лежа на кушетке после наложения 4-х пневмоманжет справа и слева на плечи и лодыжки для регистрации сфигмограмм и измерения АД, а также электрокардиографических электродов на запястья и микрофона фонодатчика на грудную клетку. Общее время регистрации сигналов составляло не >10 мин. CAVI рассчитывается аппаратом автоматически по скорости пульсовой волны на участке от клапана аорты до артерий правой и левой голени [6].
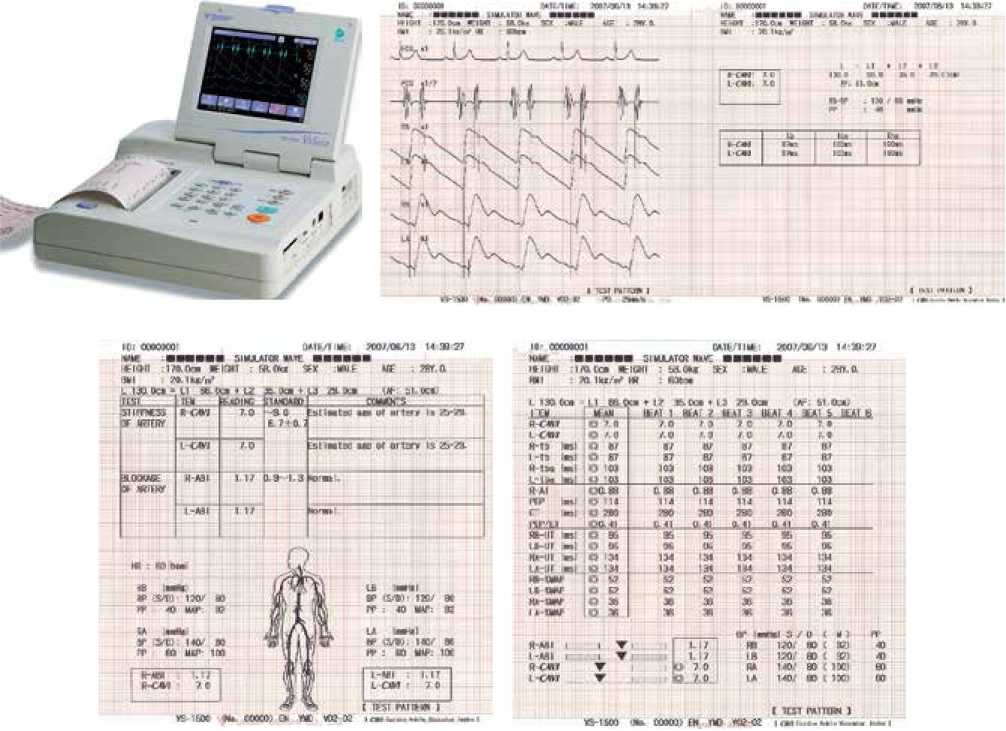
Рис. 1 Аппарат VaSeraVS-1500 и результаты исследования: кривые ЭКГ, фонокардиограммы, сфигмограммы, показатели САД и ДАД, CAVI и ЛПИ справа и слева.
Для централизованной групповой обработки первичные данные в цифровом формате пересылались в ФГБУ “НМИЦ кардиологии” Минздрава России. Анализировались качество регистрации, значения систолического (САД), диастолического (ДАД) АД, CAVI и лодыжечно-плечевой индекс (ЛПИ). После проведенного контроля качества записанных сфигмограмм, а также исключения из анализа лиц с ЛПИ <0,9 (методические ограничения для оценки CAVI) в итоге проанализированы данные 1342 человек, 543 мужчин и 799 женщин, средний возраст 47,3±11,6 лет. Значимых различий между CAVI справа и слева выявлено не было (p>0,3), что позволило при анализе использовать среднее значение.
Проведено проспективное наблюдение за исходно сформированной когортой. Средний период наблюдения обследованных составил 4,7 года (1716 дней). В ходе исследования достигнут необходимый отклик — в результате прямых и непрямых контактов с населением была получена информация в отношении 99% исходно обследованных представителей популяционной когорты.
Прогностическое значение CAVI изучалось в отношении следующих конечных точек (КТ): первичная комбинированная КТ — смерть от ССЗ, нефатальный инфаркт миокарда (ИМ) или инсульт (n=36) и вторичная комбинированная КТ — все ССС: смерть от ССЗ, нефатальный ИМ или инсульт, операция по реваскуляризации миокарда, госпитализация по поводу обострения ишемической болезни сердца (ИБС), хронической сердечной недостаточности (ХСН) (n=76).
Статистический анализ. При обработке результатов использовались пакеты статистических программ SPSS v. 20, Statistica 10, а также среда статистического анализа R 3.6.1 с открытым исходным кодом. Для непрерывных показателей вычислялся коэффициент непараметрической асимметрии Пирсона, т.е. разность между выборочным средним и медианой, нормированная на стандартное отклонение [16]. Если значение коэффициента непараметрической асимметрии для унимодального непрерывного параметра было <0,2, то распределение считалось незначительно отклоняющимся от нормального и параметр описывался средним и стандартным отклонением (M±SD). Если эти условия нарушались, то распределение параметра считалось отклоняющимся от нормального и для параметра приводились медиана и интерквартильный размах [Me (Q25-Q75)]. Качественные показатели описаны абсолютными и относительными частотами (%). Оценка различий между двумя независимыми выборками для непрерывных параметров в зависимости от их типа распределения проводилась c использованием t-критерия Стьюдента или его непараметрического аналога — критерия Манна-Уитни, для дискретных — точного двустороннего критерия Фишера. Сравнение двух кривых выживаемости Каплана-Мейера проведено лог-ранговым тестом. С помощью ROCанализа для двух видов КТ определялись отрезные значения для показателя АЖ по значению, при котором чувствительность была наиболее близка к специфичности. Оценивалась значимость площади (AUC) под ROCкривой (AUC ROC) и проводилось сравнение данного показателя для изучаемых параметров. Ассоциации между показателем АЖ и другими ФР с выявлением КТ двух видов определялись с помощью моделей пропорциональных рисков Кокса и модели бинарной логистической регрессии. При проверке гипотез p-значения приводились с точностью до третьего знака после запятой. Значимость различий для всех проверяемых гипотез устанавливалась на уровне р<0,05.
Результаты
В таблице 1 представлены отдельные параметры исходно обследованной популяционной когорты (n=1342). Обследованная выборка характеризовалась большей долей женщин (60%), возраст которых был значимо выше, чем у мужчин (в среднем на 2 года), отмечены высокая частота ФР ССЗ: третья часть обследованных имела ожирение, 40% курили, у 70% выявлена артериальная гипертония (АГ) — в анамнезе и/или при обследовании, у 18% — ИБС в анамнезе, у 11% — СД. За период наблюдения в обследованной выборке произошло 37 (2,8%) смертей от всех причин, из них 15 (1,1%) — от ССЗ. Количество случаев первичной комбинированной КТ составило 36 (2,7%) человек, вторичной комбинированной КТ — 76 (5,7%) человек.
Таблица 1
Клинико-инструментальная характеристика обследованных (n=1342)
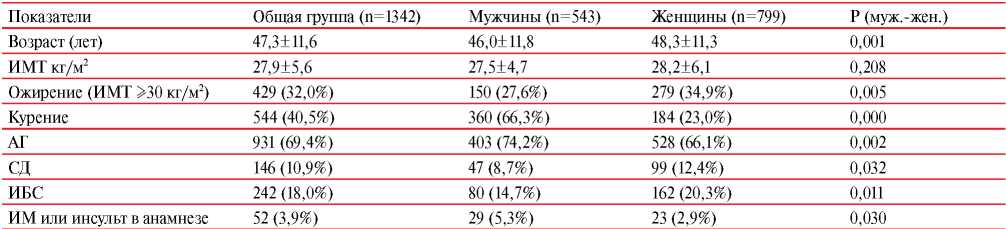
Примечание: данные представлены в виде М±SD; дискретные величины представлены в формате “n (%)”. Для дискретных величин использован точный тест Фишера, для непрерывных — критерий Манна-Уитни.
Известно, что наличие в анамнезе ССЗ значительно повышает риск смерти и других ССС и позволяет отнести данных пациентов к группе высокого и очень высокого риска. Это нашло подтверждение и в данном исследовании. Среди 52 (3,9% от общего числа) человек с ранее перенесенным ИМ или инсультом частота регистрации первичной комбинированной КТ в сравнении с лицами без отягощенного анамнеза возрастала с 2,3 до 11,5% (р=0,0003), а вторичной комбинированной КТ — с 5 до 23% (р<0,001). Дальнейший анализ прогностической значимости показателя CAVI был проведен в группе из 1290 человек, не имевших в анамнезе ИМ или инсульта. В таблице 2 представлена характеристика этой группы. Выявлено, что показатели CAVI у мужчин значимо выше, чем у женщин: 7,4±1,4 vs 7,1±1,3 (р=0,002), несмотря на более молодой возраст — 45,4±11,8 vs 48,0±11,3 лет (р<0,001). Количество случаев первичной комбинированной КТ в данной выборке составило 30 (2,3%) человек, вторичной комбинированной КТ — 64 (5,7%) человека без значимого различия у мужчин и женщин.
Таблица 2
Клинико-инструментальная и лабораторная характеристика обследованных без ССЗ в анамнезе (n=1290)
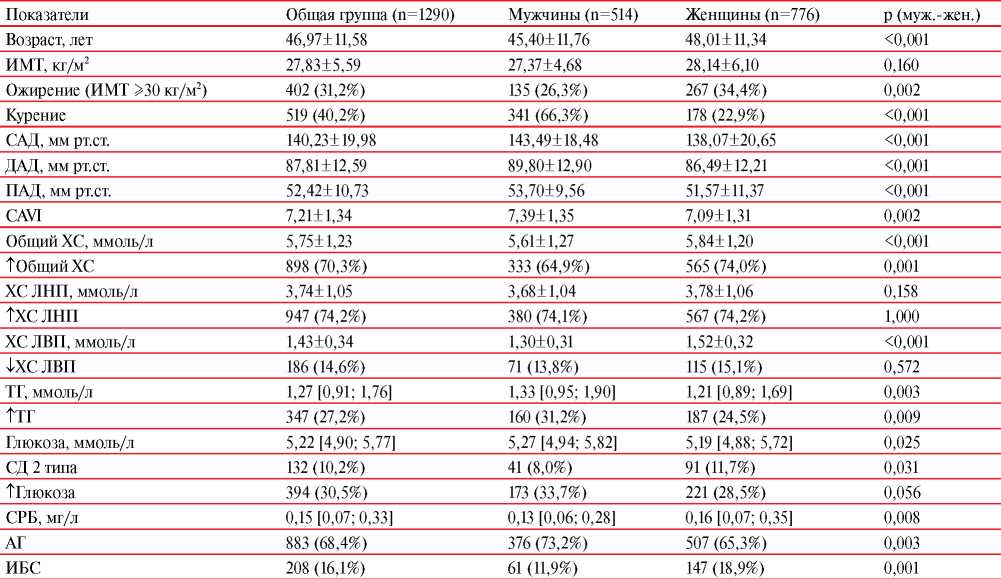
Примечание: данные представлены в виде М±SD, Me (Q25-Q75), дискретные величины представлены в формате “n (%)”. Для дискретных величин использован точный тест Фишера, для непрерывных — критерий Манна-Уитни. ↑общий ХС ≥5 ммоль/л; ↑ХС ЛНП ≥3,0 ммоль/л; ↓ХС ЛВП <1,0/1,2 ммоль/л (м/ж); ↑ТГ ≥1,7 ммоль/л; ↑глюкоза ≥6,1 ммоль/л. СРБ — C-реактивный белок.
Для обеспечения многофакторного дискретного анализа на первом этапе определены “пороговые” значения показателя CAVI, разделяющие лиц с наличием и отсутствием ССС за период наблюдения. Поскольку известно, что параметры АЖ тесно связаны с возрастом, аналогичный анализ проведен также для показателя “паспортный возраст”. ROCанализ с определением оптимального “отрезного значения” по критерию “чувствительность равна специфичности” определил для первичной комбинированной КТ “отрезное значение” CAVI =7,8 (AUC ROC =0,718, чувствительность 70%, специфичность 70%), для паспортного возраста “отрезное значение” 54 года (AUC ROC =0,696, чувствительность 60%, специфичность 68%). Аналогичный анализ для вторичной комбинированной КТ выявил “отрезное значение” для CAVI =7,7 (AUC ROC =0,716, чувствительность 69%, специфичность 68%), для возраста 54 (AUC ROC =0,743, чувствительность 66%, специфичность 69%). В связи с близостью полученных “отрезных значений” для CAVI, было принято решение в дальнейшем рассматривать максимальную из них (равную 7,8) как отрезную для первичной и вторичной комбинированных КТ. На рисунке 2 представлены ROC-кривые для анализируемых показателей.
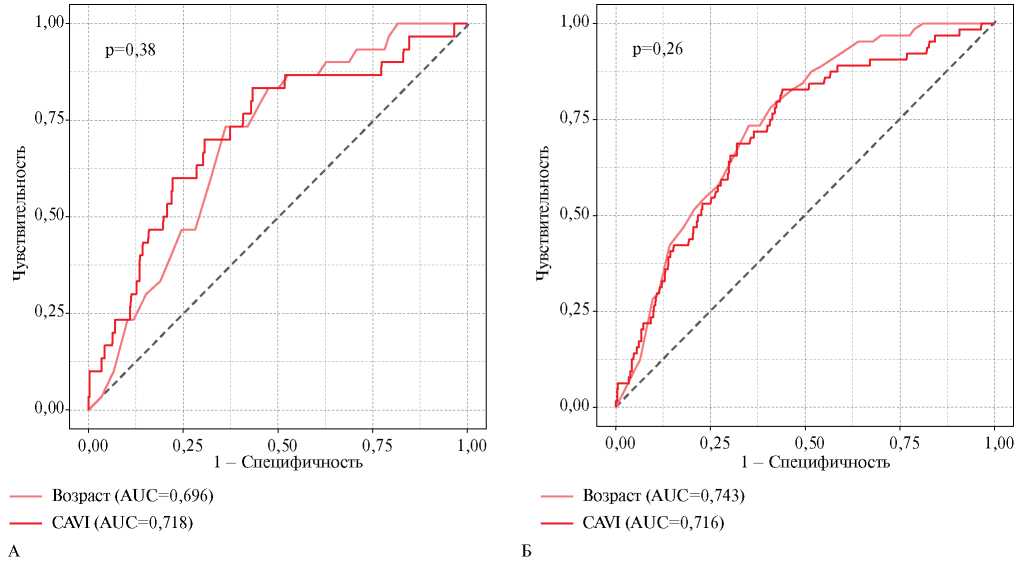
Рис. 2 ROC-кривые для показателей паспортный возраст и CAVI для первичной комбинированной (А) и вторичной комбинированной (Б) конечных точек.
По результатам однофакторного анализа в рамках дискретной модели Кокса выявлена статистически значимая прогностическая ценность показателя CAVI >7,8 в отношении риска развития первичной комбинированной КТ — относительный риск (ОР): 5,06; 95% ДИ: 2,32-11,06 (р<0,001) и вторичной комбинированной КТ — ОР: 3,95; 95% ДИ: 2,37-6,58 (р<0,001).
Анализ дожития без ССС у обследованных лиц с повышенной жесткостью сосудистой стенки (CAVI >7,8) выполнен методом Каплана-Мейера. На рисунке 3 представлены кривые дожития Каплана-Мейера без ССС у обследованных лиц, которые статистически значимо различались при CAVI >7,8 и CAVI ≤7,8.
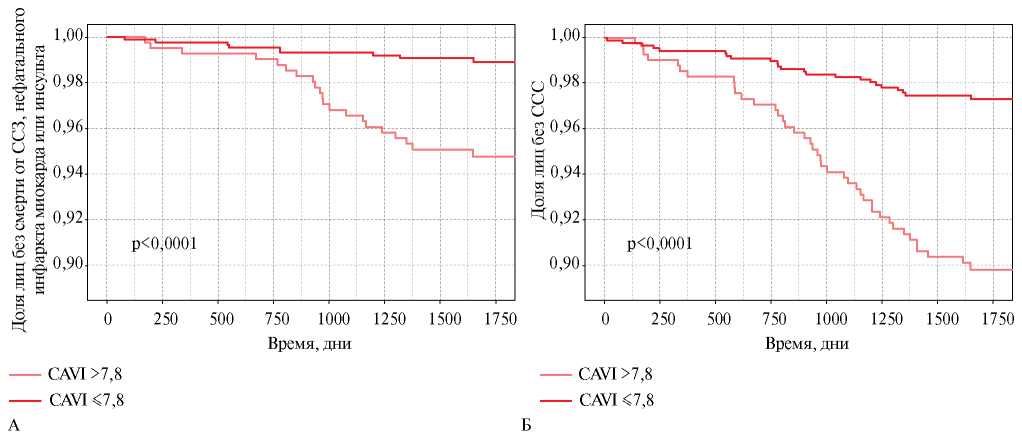
Рис. 3 Кривые дожития Каплана-Мейера для первичной комбинированной (А) и вторичной комбинированной (Б) КТ при CAVI >7,8 и CAVI ≤7,8.
На основании известной взаимосвязи показателей АЖ и традиционных ФР ССЗ, подтвержденной и в данной выборке, на следующем этапе анализа был поставлен основной вопрос: сохраняет ли свою значимость в прогнозе ССС критерий повышенной АЖ — CAVI >7,8 после учета вклада в прогноз традиционных ФР.
Прогностическое значение показателя CAVI анализировалось в рамках многофакторной прогностической модели Кокса. Для перевода рассматриваемых в данной работе непрерывных показателей, влияющих на прогноз ССС в дискретные, применены пороговые значения в соответствии с рекомендациями [17][18]: САД ≥140 мм рт.ст., пульсовое АД (ПАД) ≥60 мм рт.ст., индекс массы тела (ИМТ) ≥30 кг/м2, уровень холестерина (ХС) липопротеинов низкой плотности (ЛНП) >3,0 ммоль/л, ХС липопротеинов высокой плотности (ЛВП) <1,0/1,2 ммоль/л (м/ж), триглицеридов (ТГ) >1,7 ммоль/л. Также учитывались пол, наличие табакокурения, СД.
Показано, что в 3-факторной модели, включающей САД, возраст и CAVI, последний показатель сохраняет прогностическую значимость как в отношении первичной комбинированной КТ — ОР: 3,44; 95% ДИ: 1,41-8,4 (р=0,007), так и вторичной комбинированной КТ — ОР: 2,3; 95% ДИ: 1,27- 4,16 (р=0,006). Эта закономерность сохраняется и в 4-факторной модели, учитывающей гендерный признак — ОР: 3,26; 95% ДИ: 1,32-8,09 (р=0,011) и ОР: 2,21; 95% ДИ: 1,21-4,03 (р=0,010), соответственно, для первичной и вторичной комбинированных КТ. Более того, в модели пропорциональных рисков Кокса с включением в анализ помимо CAVI таких 10 традиционных ФР ССЗ, как возраст, пол, САД, ПАД, ИМТ, ХС ЛНП, ХС ЛВП, ТГ, курение, СД, было продемонстрировано, что признак повышенной АЖ CAVI >7,8 также сохраняет свою прогностическую ценность. При этом в модели прогноза вторичной комбинированной КТ только признак старшего возраста >54 лет — ОР: 2,42; 95% ДИ: 1,29-4,56 (р=0,006) и признак повышенной АЖ CAVI >7,8 — ОР: 3,13; 95% ДИ: 1,26-7,75 (p=0,014), сохраняют статистическую значимость для прогноза. В аналогичной модели прогноза первичной комбинированной КТ только показатель повышенной АЖ CAVI >7,8 (ОР: 2,16; 95% ДИ: 1,18-3,98) (p=0,013) сохраняет свою статистическую значимость.
В таблице 3 представлены результаты анализа для всех анализируемых параметров при включении показателя CAVI >7,8 в модели с различным числом факторов. Таким образом, проведенный анализ убедительно продемонстрировал как самостоятельное, так и независимое прогностическое значение показателя АЖ — CAVI в отношении риска развития ССС в исследованной выборке.
Таблица 3
Результаты анализа моделей пропорциональных рисков Кокса для традиционных ФР и маркера CAVI >7,8
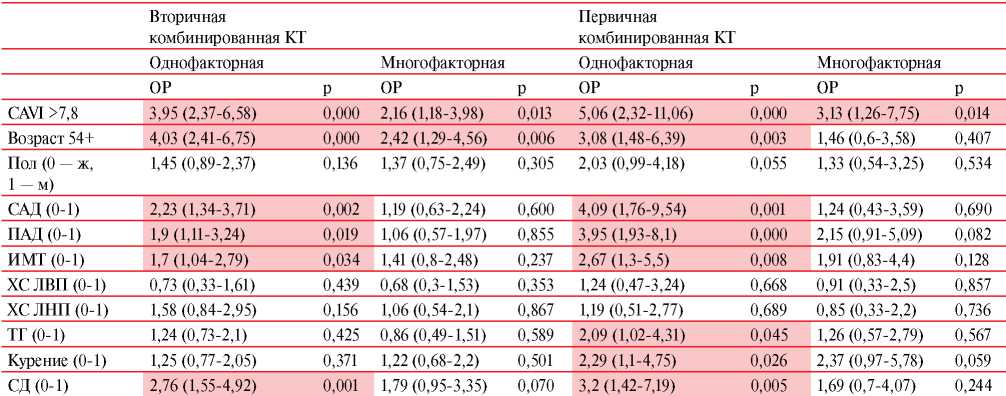
Примечание: данные представлены в виде Me (Q25-Q75); цветом выделены статистически значимые компоненты различных моделей.
В связи с полученными результатами возникает вопрос о целесообразности и необходимости проведения оценки АЖ методом ОС с включением данного исследования в алгоритм обследования при профилактических и диспансерных осмотрах. При этом с учетом необходимости оптимизации работы важно определить соответствующий контингент лиц, кому может быть рекомендована ОС с определением CAVI в первую очередь. Проведен анализ с определением частоты выявления повышенной АЖ в разных возрастных группах с учетом гендерного фактора (таблица 4). Полученные результаты позволяют заключить, что в возрастной группе до 35 лет ожидаются только единичные случаи превышения CAVI >7,8, причем как у мужчин, так и у женщин, но начиная со 2-ой возрастной группы (35-44 года) этот признак выявляется уже у 11,5% обследованных мужчин и у 5,8% женщин, в 3-ей возрастной группе (45-54 года) у каждого третьего обследованного, а в 4-ой возрастной группе (55-64 года) у > половины обследованных, при этом у мужчин значимо чаще чем у женщин — 77,6 vs 56,4% (р<0,0005). Таким образом, проведенный анализ позволяет рекомендовать проведение ОС с определением показателя CAVI для уточнения ССР в популяции взрослого населения в целом, но с учетом того, что выявление CAVI >7,8 маловероятно (<10%) у мужчин до 35 и женщин до 45 лет. Важно отметить, что при ограничении возраста диапазоном 55-64 года (старшая возрастная группа) возраст теряет свою прогностическую значимость и, в связи с этим, определение CAVI приобретет решающее значение в прогнозе ССС (рисунок 4).
Таблица 4
Частота CAVI >7,8 в разных возрастных группах, n (%)

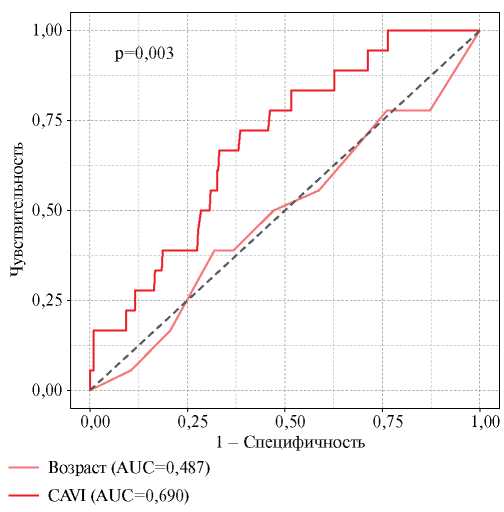
Рис. 4 ROC-кривые для CAVI и возраста в отношении ССС (первичная комбинированная КТ) в возрастной группе 55-64 года.
На сегодняшний день в странах Европы наиболее распространенной при оценке риска ССС является шкала SCORE (Systematic Coronary Risk Evaluation). Проведен сравнительный анализ прогностической ценности показателя CAVI со шкалой SCORE. Количественный прогноз риска ССС по шкале SCORE выполнен в соответствии с рекомендациями [19]. ROC-анализ продемонстрировал, что “простой” прогноз на основании только значения CAVI имеет сопоставимую со шкалой SCORE прогностическую ценность в отношении ССС (рисунок 5). В модели с добавлением к CAVI паспортного возраста значение AUC ROC увеличивается с 0,718 до 0,730 (первичная комбинированная КТ) и с 0,716 до 0,756 (“комбинированная” КТ). А когда в модель прогноза ССС кроме CAVI и возраста добавляются пол, САД и курение, то значение AUC ROC увеличивается до 0,765 (первичная комбинированная КТ) и 0,763 (вторичная комбинированная КТ), но не достигает статистически значимых различий при сравнении со SCORE (0,759 и 0,747, соответственно), (рисунок 6).
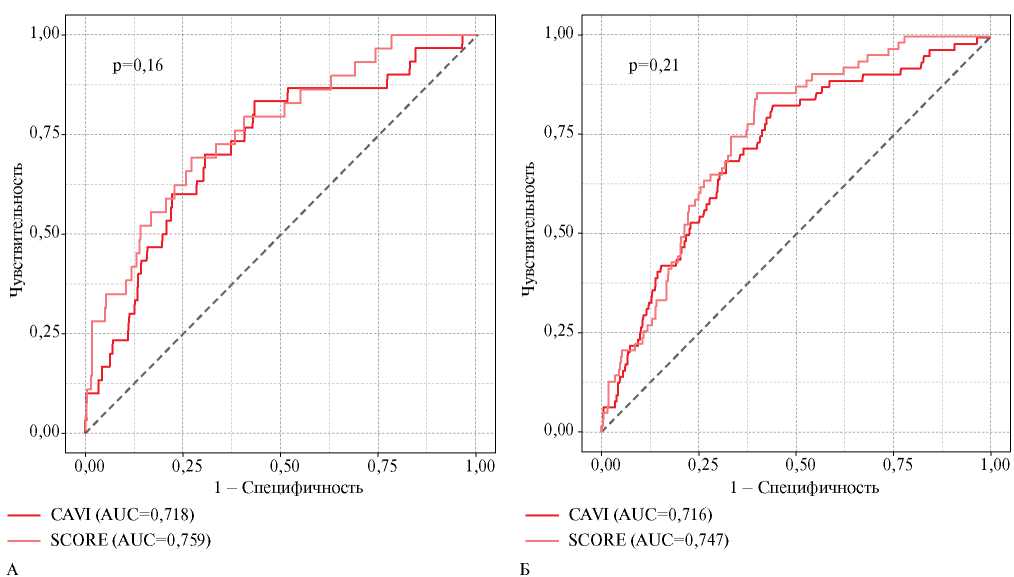
Рис. 5 ROC-кривые CAVI и шкалы SCORE в прогнозе риска ССС — первичная комбинированная (А) и вторичная комбинированная (Б) КТ.
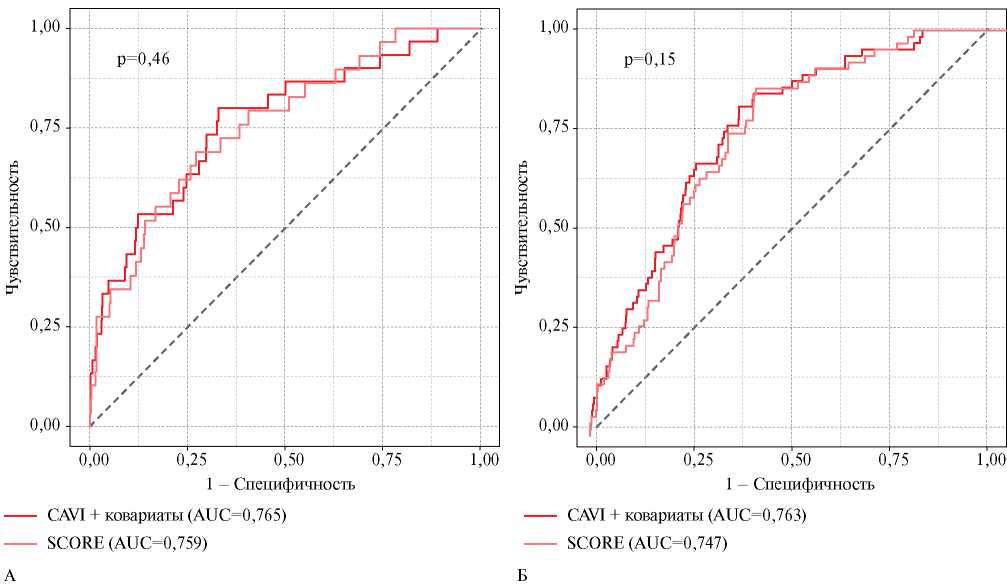
Рис. 6 ROC-кривые модели CAVI+возраст+пол+САД+курение и шкалы SCORE в прогнозе риска ССС — первичная комбинированная (А) и вторичная комбинированная (Б) КТ.
Таким образом, полученные результаты позволяют предложить метод оценки рисков CCC (“модель CAVI”), не требующий, в отличие от SCORE, привлечения данных лабораторных методов исследования. Например, для оценки 5 летнего риска ССС у конкретного обследуемого на основе модели бинарной логистической регрессии с бинарными независимыми переменными (возраст, пол, СAVI, CАД, курение), где в качестве зависимой переменной выступает вторичная комбинированная КТ, необходимо провести следующие вычисления:
1. Вычислить величину показателя Z по следующему правилу:
+1,24 балла, если возраст ≥54 лет
+0,24 балла, если обследуемый — мужчина
+0,68 балла, если CAVI >7,8
+0,32 балла, если САД ≥140 мм рт.ст.
+0,25 балла, если курит
2. Рассчитать 5-летний риск ССС (в %) по формуле: R=100/(1+exp(4,3–Z)).
Для применения представленной модели на практике предлагается алгоритм отнесения к группам риска ССС, для чего необходимо:
1. Вычислить величину показателя Z* по следующему правилу:
+10 баллов, если возраст ≥54 лет
+2 балла, если обследуемый — мужчина,
+8 баллов, если CAVI >7,8
+4 балла, если САД ≥140 мм рт.ст.
+3 балла, если курит
2. По рассчитанному числу баллов определить группу риска ССС.
В ходе анализа установлено, что распределение пациентов по квартилям Z совпадает с распределением по квартилям Z*. Если значение показателя Z* было ниже выборочной медианы Z*≤Q50, где Q50=10, то пациента относили к группе низкого риска, если Q50<Z*≤Q75, где Q75=17 к группе среднего риска, если Z*>Q75, то к группе высокого риска. Таким образом, на основе вычисленного Z* пациент попадает в одну из следующих групп риска: Z≤10: (низкий уровень риска ССС — вероятность наступления ССС <2,9%); 10<Z≤17 (средний уровень риска ССС — вероятность наступления ССС от 2,9 до 7,4%); Z>17 (высокий уровень риска ССС — вероятность наступления ССС >7,4%).
Полученные в данном исследовании результаты позволяют также предположить, что выявление повышенной АЖ по критерию CAVI >7,8 у лиц низкого или среднего риска по шкале SCORE позволит реклассифицировать часть обследуемых в группу высокого риска. Согласно Российским национальным рекомендациям 2017г, дополнительные ФР, такие как отягощенная наследственность, наличие атеросклеротических бляшек, снижение ЛПИ, избыточная масса тела и др. могут реклассифицировать обследуемого в более высокую группу риска ССС [20], однако в этом ряду фактор повышенной АЖ отсутствует. Проведен дополнительный анализ c оценкой возможности реклассификации за счет фактора АЖ с расчетом показателя NRI (Net Reclassification Improvement) [21]. Анализировалось добавление CAVI к SCORE по правилам, приведенным на рисунке 7, т.е. группы риска формировались по рекомендуемым отрезным значениям SCORE, но если у обследуемого CAVI был >7,8, то он переходил в следующую по тяжести группу риска. Показано, что это значимо реклассифицирует риск наступления первичной (NRI=0,30; p=0,035) и вторичной (NRI=0,20; p=0,0045) комбинированных КТ у женщин. Отметим, что у мужчин при подобной реклассификации значимого улучшения предсказательной способности не обнаружено, что рассматриваем как предварительный результат, требующий подтверждения в исследовании с бóльшим числом КТ.
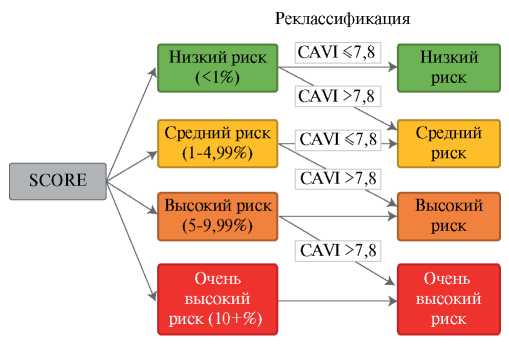
Рис. 7 Схема реклассификации для оценки риска ССС при добавлении критерия повышенной АЖ CAVI >7,8 к шкале SCORE.
Обсуждение
Эпидемиологическое исследование ЭССЕ-РФ явилось первым популяционным исследованием, в рамках которого проводилась оценка АЖ в 5 регионах РФ [5]. В настоящей работе представлены результаты оценки прогностической значимости показателя АЖ CAVI в отношении ССС в выборке из российской популяции на основе анализа материала, полученного в г. Томск.
В опубликованных ранее работах зарубежных авторов получены неоднозначные результаты. В некоторых исследованиях продемонстрирована независимая прогностическая ценность CAVI; например, данные 5-летнего наблюдения за 425 пациентами с ожирением (средний возраст 51,5 лет) показали статистически значимую ценность CAVI в отношении прогноза ССС (ИМ, инсульт, чрескожное коронарное вмешательство) в многофакторной модели Кокса с учетом пола, возраста, ИМТ, курения, АГ, дислипидемии (ДЛП) и СД: для повышения на единицу значения CAVI ОР составило 1,50; 95% ДИ: 1,04-2,02 (р=0,029) [8]. Независимая прогностическая ценность CAVI в отношении острых коронарных событий и хронической ИБС подтверждена и при 6,7±1,6-летнем наблюдении за 1003 пациентами (средний возраст 62,5 лет) с метаболическими нарушениями (СД, ДЛП) и АГ: в многофакторной модели, включающей традиционные ФР (возраст, пол, курение, наличие СД и АГ), повышение CAVI на единицу увеличивало риск ССС: ОР 1,13; 95% ДИ: 1,01-1,26 (р=0,039) [9]. Значение CAVI >8,3 при наблюдении в течение 15 мес. за 288 пациентом после перенесенного острого коронарного события оказалось предиктором ССС: в отношении таких ССС, как смерть от ССЗ, нефатальный ИМ — ОР 18,0; 95% ДИ 2,4-136,8 (р=0,005 с учетом возраста и курения), а в отношении нефатального инсульта — ОР 9,4; 95% ДИ: 1,18-74,2 (р=0,034 с учетом возраста и наличия СД) [22]. Результаты 4-летнего наблюдения за 626 пациентами с СД 2 типа показали, что повышенное значение CAVI ≥ 9 является значимым независимым предиктором ССС в логистическом регрессионном анализе — ОШ 1,18; 95% ДИ: 1,0-1,38 (р=0,049) (c учетом таких факторов как пол, возраст, курение, ИМТ, АГ, ДЛП, уровень глюкозы) и что прогностическое значение CAVI ≥9,0 и кальциевого индекса >100 равноценны [10], а данные 3-летнего наблюдения за 400 пациентами с АГ, СД и ДЛП >63 лет при многофакторном анализе с учетом возраста, пола, курения, СД, АГ, ДЛП и хронической болезни почек продемонстрировали, что у обследованных с CAVI ≥10,0 значительно выше риск ССС и инсульта — ОР: 2,25; 95% ДИ: 1,02-4,95 (р=0,04) [23]. В то же время в работе других авторов [14] показано, что CAVI не обладает независимой прогностической ценностью, а именно: первоначально при наблюдении за пациентами среднего возраста с метаболическим синдромом (n=2106) в течение 3,8 лет выявлено, что повышение CAVI на одно стандартное отклонение увеличивает риск ССС (ИМ, инсульт, внезапная смерть) на 26% — ОР: 1,26; 95% ДИ: 1,03-1,55 (р=0,026). Однако при поправке на традиционные ФР статистическая значимость CAVI не сохранялась. В ряде других исследований [12][13] при наблюдении от 3 до 5 лет за небольшими группами пациентов пожилого возраста с высоким риском ССЗ (больные хронической болезнью почек, СД, АГ) CAVI не обладал независимой прогностической ценностью в отношении ССС. Сложность однозначного вывода о прогностическом значении CAVI заключается в небольшом количестве исследований, проведенных, в основном, в странах Азии на отдельных группах больных или лиц с высоким риском ССЗ, в отсутствии результатов крупных многоцентровых, а также эпидемиологических исследований в этом направлении [14].
Несмотря на то, что исследование ЭССЕ-РФ было популяционным, в рамках которого обследована случайная выборка взрослого населения в г. Томск, оказалось, что большинство имеет АГ и ДЛП, а ожирение и курение встречаются чаще, чем у каждого третьего. Более того, выявлено 52 человека с наличием ИМ или инсульта в анамнезе, у которых частота ССС за время наблюдения превышала частоту ССС среди других обследованных в 5 раз. В данном исследовании “отрезной точкой”, разделяющей лиц с наличием и отсутствием ССС явилось значение CAVI >7,8 — несколько более низкое, чем в опубликованных ранее работах (от 8,3 до 10) [8][11][22][23]; возможно, это объясняется тем, что оно получено на популяционной выборке трудоспособного населения 25-64 лет, из которой для многофакторного анализа на первом этапе были исключены лица с отягощенным по ССЗ анамнезом. Сопоставимым с нашим “отрезным значением” CAVI являются данные публикации российских авторов, в исследовании которых значение CAVI >8,0 было ассоциировано с перенесенным ИМ, в связи с чем, этот критерий предлагается считать маркером очень высокого риска [24]. В данном исследовании в однофакторном анализе показано, что превышение CAVI >7,8 может быть предиктором как “жестких” КТ (нефатального ИМ, инсульта или смерти от ССЗ) — ОР 5,06; 95% ДИ: 2,32-11,06 (р<0,001), так и всех ССС (смерть от ССЗ, нефатальный ИМ или инсульт, операция по реваскуляризации миокарда, госпитализация по поводу обострения ИБС или ХСН) — ОР 3,95; 95% ДИ: 2,37-6,58 (р<0,001). В многофакторной модели пропорциональных рисков Кокса с включением параметров, формирующих традиционные ФР (возраст, пол, САД, ПАД, ИМТ, ХС ЛНП, ХС ЛВП, ТГ) подтверждено независимое прогностическое значение повышенного CAVI >7,8 в отношении ССС: ОР 3,13; 95% ДИ: 1,26-7,75 (p=0,014) для первичной комбинированной КТ и ОР 2,16; 95% ДИ: 1,18- 3,98 (p=0,013) для вторичной комбинированной КТ. Кроме того, показано, что определение CAVI в старшей возрастной группе (55-64 года) приобретает решающее значение в прогнозе ССС.
Поскольку показатели АЖ, в т.ч. и CAVI, являются интегральными маркерами воздействия на сосудистую стенку всех неблагоприятных ФР, очевидным становится вопрос практической оценки риска ССС с использованием этого показателя. В настоящей работе продемонстрирована сопоставимая со шкалой SCORE прогностическая ценность показателя CAVI, а также предложена модель, включающая возраст, пол, курение, САД и CAVI, равноценная по прогностической значимости оценке риска ССС по шкале SCORE и не требующая проведения каких-либо лабораторных исследований. При использовании предлагаемого алгоритма оценки 5-летнего риска ССС возможно определение как категории риска, так и его конкретного уровня для каждого обследуемого.
Ранее некоторыми авторами в РФ предлагалось определение CAVI в группах пациентов высокого риска [25][26]. Настоящее исследование продемонстрировало целесообразность определения CAVI как в популяционных обследованиях, так и при диспансерных и профилактических осмотрах, в первую очередь, мужчинам, начиная с 35 и женщинам с 45 лет. При этом необходимо учитывать, что при стенозирующих поражениях артерий нижних конечностей с ЛПИ <0,9 и при значимых нарушениях ритма сердца (фибрилляция предсердий и частая экстрасистолия) определение CAVI не может быть выполнено или адекватно интерпретировано, кроме того, имеются противопоказания к проведению исследования в виде флеботромбоза и выраженных заболеваний кожи на конечностях.
Результаты настоящего исследования получены в “обучающей выборке” и должны быть подтверждены и уточнены в “контрольных выборках”, тем более что возможны и ожидаемы специфические особенности и закономерности в различных регионах и группах населения РФ.
Заключение
Показатель АЖ, корригированный на уровень АД в момент измерения, индекс CAVI имеет существенное независимое прогностическое значение в отношении ССС в популяционной выборке взрослого городского населения г. Томска. Для уточнения ССР при профилактических и диспансерных осмотрах может быть рекомендовано проведение ОС с определением показателя CAVI мужчинам, начиная с 35 лет, и женщинам, начиная с 45 лет.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Laurent S, Cockcroft J, van Bortel L, et al. Expert consensus document on arterial stiffness: methodological issues and clinical applications. Eur Heart J. 2006;27:2588-605. doi:10.1093/eurheartj/ehl254.
2. Васюк Ю. А., Иванова С. В., Школьник Е. Л. и др. Согласованное мнение российских экспертов по оценке артериальной жесткости в клинической практике. Кардиоваскулярная терапия и профилактика. 2016;15(2):4-19. doi:10.15829/1728-8800-2016-2-4-19.
3. Maliha G, Townsend RR. A study of the VaSera arterial stiffness device in US patients. J Clin Hypertens (Greenwich). 2017;19(7):661-8. doi:10.1111/jch.12967.
4. Заирова А. Р., Рогоза А. Н. “Объёмная сфигмография сегодня”, Медицинский алфавит. Современная функциональная диагностика. 2018;4(36):8-18.
5. Рогоза А. Н., Заирова А. Р., Жернакова Ю. В. и др. Состояние сосудистой стенки в популяции взрослого населения РФ на примере жителей города Томск по данным исследования ЭССЕ-РФ. Системные гипертензии. 2014;11(4):42-8.
6. Saiki А, Ohira M, Yamaguchi T, et al. New Horizons of Arterial Stiffness Developed Using Cardio-Ankle Vascular Index (CAVI) J Atheroscler Thromb. 2020 Aug 1;27(8):732-48. doi:10.5551/jat.RV17043.
7. Yingchoncharoen T, Limpijankit T, Jongjirasiri S, et al. Arterial stiffness contributes to coronary artery disease risk prediction beyond the traditional risk score (RAMA-EGAT score) Heart Asia. 2012:77e82. doi:10.1136/heartasia-2011-010079.
8. Satoh-Asahara N, Kotani K, Yamakage H, et al. Cardio-ankle vascular index predicts for the incidence of cardiovascular events in obese patients: a multicenter prospective cohort study (Japan Obesity and Metabolic Syndrome Study: JOMS). Atherosclerosis. 2015;242:461-8. doi:10.1016/j.atherosclerosis.2015.08.003.
9. Sato Y, Nagayama D, Saiki A, et al. Cardio-ankle vascular index is independently associated with future cardiovascular events in outpatients with metabolic disorders. J Atheroscler Thromb. 2016;23:596-605. doi:10.5551/jat.31385.
10. Chung SL, Yang CC, Chen CC, et al. Coronary artery calcium score compared with cardio-ankle vascular index in the predictionof cardiovascular events in asymptomatic patients with type 2 diabetes. J Atheroscler Thromb. 2015;22:1255-65. doi:10.5551/jat.29926.
11. Kato A, Takita T, Furuhashi M, et al. Brachial-ankle pulse wave velocity and the cardio-ankle vascular index as a predictor of cardiovascular outcomes in patients on regular hemodialysis. Ther Apher Dial. 2012;16:232-41. doi:10.1111/j.1744-9987.2012.01058.x.
12. Kusunose K, Sato M, Yamada H, et al. Prognostic implications of non-invasive vascular function tests in high-risk atherosclerosis patients. Circ J. 2016;80:1034-40. doi:10.1253/circj.CJ-15-1356.
13. Laucevicius A, Ryliskyte L, Balsyte J, et al. Association of cardio- ankle vascular index with cardiovascular risk factors and cardiovascular events in metabolic syndrome patients. Medicina. 2015;51:152-8. doi:10.1016/j.medici.2015.05.001.
14. Matsushita K, Ding N, Kim ED, et al. Cardio-ankle vascular index and cardiovascular disease: systematic review and meta-analysis of prospective and cross-sectional studies. J Clin Hypertens (Greenwich). 2019; 21:16-24. doi:10.1111/jch.13425.
15. Научно-организационный комитет проекта ЭССЕ-РФ Эпидемиология сердечно-сосудистых заболеваний в различных регионах России (ЭССЕ-РФ). Обоснование и дизайн исследования. Профилактическая медицина. 2013;16(6):25-34.
16. Arnold BC, Groeneveld RA. Measuring skewness with respect to the mode. Am Stat. 1995;49(1):34-8. doi:10.1080/00031305.1995.10476109.
17. Williams B, Mancia G, Spiering W, et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J. 2018;39:3021-104. doi:10.1093/eurheartj/ehy339.
18. Mach F, Baigent C, Catapano AL, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020;41(1):111-88. doi:10.1093/eurheartj/ehz455.
19. Conroya RM, Pyorala K, Fitzgeralda AP, et al. Estimation of ten-year risk of fatal cardiovascular disease in Europe: the SCORE project. Eur Heart J. 2003;24:987-1003. doi:10.1016/S0195-668X(03)00114-3.
20. Кардиоваскулярная профилактика 2017. Российские национальные рекомендации. Российский кардиологический журнал. 2018;23(6):7-122. doi:10.15829/1560-4071-2018-6-7-122.
21. Pencina MJ, D'Agostino RB Sr, D'Agostino RB Jr, et al. Evaluating the added predictive ability of a new marker: From area under the ROC curve to reclassification and beyond. Statist Med. 2008; 27:157-72. doi:10.1002/sim.2929.
22. Gohbara M, Iwahashi N, Sano Y, et al. Clinical impact of the cardio-ankle vascular index for predicting cardiovascular events after acute coronary syndrome. Circ J. 2016;80:1420-6. doi:10.1253/circj.CJ-15-1257.
23. Kubota Y, Maebuchi D, Makoto Takei M, et al. Cardio-Ankle Vascular Index is a predictor of cardiovascular events. Artery Research. 2011;5(3):91-6. doi:10.1016/j.artres.2011.03.005.
24. Носов А. Е., Горбушина О. Ю., Власова Е. М., Алексеев В. Б. Прогностическая значимость параметров артериальной жесткости в выявлении пациентов очень высокого риска. Кардиология. 2020;60(10):27-32. doi:10.18087/cardio.2020.10. n1239.
25. Отт М. В., Сумин А. Н., Коваленко А. В. Возможности применения сердечно-лодыжечного сосудистого индекса у больных с цереброваскулярными заболеваниями. Журнал неврологии и психиатрии им. С. С. Корсакова. Спецвыпуски. 2020;120(8-2):37-44. doi:10.17116/jnevro202012008237.
26. Трифонова С.С., Гайсенок О.В., Сидоренко Б. А. Применение методов оценки жесткости сосудистой стенки в клинической практике: возможности сердечно-лодыжечного сосудистого индекса. Кардиология. 2015;55(4):61-6. doi:10.18565/cardio.2015.4.61-66.
Об авторах
А. Р. ЗаироваРоссия
Заирова Алсу Рафхатовна — кандидат медицинских наук, научный сотрудник отдела новых методов диагностики.
Москва.
Тел.: +7 (909) 630-80-41
А. Н. Рогоза
Россия
Рогоза Анатолий Николаевич — доктор биологических наук, профессор, ведущий научный сотрудник руководитель отдела новых методов диагностики.
Москва.
Е. В. Ощепкова
Россия
Ощепкова Елена Владимировна — доктор медицинских наук, профессор, ведущий научный сотрудник отдела гипертонии.
Москва.
Е. Б. Яровая
Россия
Яровая Елена Борисовна — доктор физико-математических наук, профессор кафедры теории вероятностей, ведущий научный сотрудник, руководитель лаборатории биостатистики отдела эпидемиологии хронических неинфекционных заболеваний.
Москва.
В. А. Куценко
Россия
Куценко Владимир Александрович — аспирант кафедры теории вероятностей, младший научный сотрудник лаборатории биостатистики отдела эпидемиологии хронических неинфекционных заболеваний.
Москва.
С. А. Шальнова
Россия
Шальнова Светлана Анатольевна — доктор медицинских наук, профессор, руководитель отдела эпидемиологии хронических неинфекционных заболеваний.
Москва.
И. А. Трубачева
Россия
Трубачева Ирина Анатольевна — доктор медицинских наук, заведующий отделением популяционной кардиологии.
Томск.
В. С. Кавешников
Россия
Кавешников Владимир Сергеевич — кандидат медицинских наук, старший научный сотрудник отделения популяционной кардиологии.
Томск.
В. Н. Серебрякова
Россия
Серебрякова Виктория Николаевна — кандидат медицинских наук, заведующий лабораторией регистров сердечно-сосудистых заболеваний, высокотехнологичных вмешательств и телемедицины.
Томск.
С. А. Бойцов
Россия
Бойцов Сергей Анатольевич — доктор медицинских наук, профессор, академик РАН, генеральный директор.
Москва.
Дополнительные файлы
Рецензия
Для цитирования:
Заирова А.Р., Рогоза А.Н., Ощепкова Е.В., Яровая Е.Б., Куценко В.А., Шальнова С.А., Трубачева И.А., Кавешников В.С., Серебрякова В.Н., Бойцов С.А. Значение показателя артериальной жесткости “сердечно-лодыжечный сосудистый индекс — CAVI” для прогноза сердечно-сосудистых событий в популяционной выборке взрослого городского населения (по материалам исследования ЭССЕ-РФ, Томск). Кардиоваскулярная терапия и профилактика. 2021;20(5):2967. https://doi.org/10.15829/1728-8800-2021-2967
For citation:
Zairova A.R., Rogoza A.N., Oshchepkova E.V., Yarovaya E.B., Kutsenko V.A., Shalnova S.A., Trubacheva I.A., Kaveshnikov V.S., Serebryakova V.N., Boytcov S.A. Contribution of cardio-ankle vascular index to prediction of cardiovascular events in the adult urban population: data from the ESSE-RF study (Tomsk). Cardiovascular Therapy and Prevention. 2021;20(5):2967. (In Russ.) https://doi.org/10.15829/1728-8800-2021-2967
JATS XML

























































