Перейти к:
Результаты проспективного наблюдения больных артериальной гипертоний с сопутствующими хроническими болезнями органов дыхания в рутинной практике. Часть II. Предикторы неблагоприятных событий
https://doi.org/10.15829/1728-8800-2022-3424
Аннотация
Цель. Изучить предикторы неблагоприятных событий у больных артериальной гипертонией (АГ), в т.ч. с хроническими болезнями органов дыхания (БОД).
Материал и методы. В регрессионном анализе оценены клинико-анамнестические данные и показатели артериального давления (АД) у амбулаторных пациентов с АГ II-III стадии: n=156, из них 49 с бронхиальной астмой, 20 с хронической обструктивной болезнью легких; возраст 63,4±8,8 лет, женщин 72,4%, продолжительность наблюдения 29,3±8,0 мес. Исходы, вошедшие в комбинированную первичную конечную точку (КТ), зарегистрированы у 32 пациентов (смерть, серьезные сердечно-сосудистые события и осложнения), во вторичную КТ — у 57 (госпитализации, вызовы скорой медицинской помощи, временная нетрудоспособность в связи с сердечно-сосудистым заболеванием/БОД, гипертонический криз, обострение БОД, пневмония, дыхательная недостаточность), в третичную КТ — у 76 (другие значимые заболевания/состояния, включая повышения АД без развития гипертонического криза, требующие коррекции регулярной терапии).
Результаты. Предикторами первичной КТ оказались степень ночного снижения диастолического АД (ДАД) (β=-5,335, р=0,026), вариабельность ДАД ночью (β=1,796, р=0,007), уровень лейкоцитов крови (β=0,241, р=0,039); вторичной КТ — систолическое АД≥170 мм рт.ст. в анамнезе (β=1,305-1,641, р=0,037-0,017), прием статинов (β=-0,997, р=0,037), БОД (β=0,734, р=0,023), уровень тромбоцитов крови (β=-0,008, р=0,022); третичной КТ — только БОД (β=1,082, р<0,0001).
Заключение. Пациенты с АГ нуждаются в комплексной многофакторной профилактике. Необходимо улучшать контроль клинического и амбулаторного АД, липидов крови, особенно при наличии БОД, улучшать контроль самих БОД. Целесообразно чаще использовать метод суточного мониторирования АД в рутинной практике, включая оценку степени ночного снижения АД и его вариабельности.
Ключевые слова
Для цитирования:
Смирнова М.И., Горбунов В.М., Курехян А.С., Андреева Г.Ф., Кошеляевская Я.Н., Деев А.Д. Результаты проспективного наблюдения больных артериальной гипертоний с сопутствующими хроническими болезнями органов дыхания в рутинной практике. Часть II. Предикторы неблагоприятных событий. Кардиоваскулярная терапия и профилактика. 2022;21(12):3424. https://doi.org/10.15829/1728-8800-2022-3424
For citation:
Smirnova M.I., Gorbunov V.M., Kurekhyan A.S., Andreeva G.F., Koshelyaevskaya Ya.N., Deev А.D. Results of the prospective observation in routine practice of hypertensive patients with concomitant chronic respiratory diseases. Part II. Predictors of adverse events. Cardiovascular Therapy and Prevention. 2022;21(12):3424. (In Russ.) https://doi.org/10.15829/1728-8800-2022-3424
Введение
Независимый вклад болезней органов дыхания (БОД) в прогноз пациентов с сердечно-сосудистыми заболеваниями (ССЗ), в частности с артериальной гипертонией (АГ), широко известен [1-3]. Основу профилактики неблагоприятных исходов у коморбидных пациентов составляет контроль болезней и факторов риска (ФР). Однако предупреждение неблагоприятных исходов у пациентов с сочетанием АГ и БОД представляет определенную проблему. Во-первых, требуется выявление всех модифицируемых ФР, а во-вторых, необходим их длительный контроль и периодическая оценка пациента, учитывающая вероятность утраты контроля, появления новых ФР, а также изменения течения болезней. При этом, несмотря на обширные знания о пользе мер первичной и вторичной профилактики, неудовлетворительный контроль ФР сохраняется. Например, по данным исследования ЭССЕ-РФ (Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в регионах Российской Федерации), на фоне некоторого снижения уровня заболеваемости и смертности взрослого населения в России, благодаря внедрению современных методов профилактики, диагностики и лечения ССЗ, остаются проблемы с контролем артериального давления (АД), гиперлипидемии, массы тела, курения и других модифицируемых ФР [4]. Отмеченное нацеливает на проведение дальнейших исследований в области изучения АГ, в частности у больных с БОД, для поиска направлений совершенствования профилактики неблагоприятных исходов. Эти исследования включают/могут включать оценку разнообразных параметров — потенциальных предикторов неблагоприятных событий, в т.ч. отдельных характеристик АД, особенностей течения сопутствующих заболеваний, медикаментозной терапии и профилактики.
В представленной ранее первой части данной работы были проанализированы различные типы неблагоприятных событий у больных АГ, в т.ч. с хроническими БОД — бронхиальной астмой (БА) и хронической обструктивной болезнью легких (ХОБЛ) [5].
Цель второй части исследования — изучение факторов, ассоциированных с неблагоприятными событиями у пациентов с АГ (в т.ч. с БОД), включая клинико-анамнестические данные и некоторые показатели АД.
Материал и методы
Основой для анализа послужили результаты проспективного когортного исследования больных эссенциальной АГ, обращающихся к кардиологу муниципальной поликлиники, часть которых имела сопутствующую БА или ХОБЛ. Протокол исследования был одобрен этическим комитетом ФГБУ "НМИЦ ТПМ" Минздрава России. Некоторые детали протокола и характеристики пациентов опубликованы в 1 части статьи [5].
Критериями включения в проспективное наблюдение были:
- возраст 30-79 лет,
- регулярная антигипертензивная терапия (АГТ) не <2 нед. подряд с уровнем клинического АД на момент включения <180/110 мм рт.ст.,
- у больных с БА и ХОБЛ наличие верифицирующей диагноз медицинской документации,
- информированное согласие на участие в исследовании.
Критерии невключения:
- симптоматическая АГ,
- состояния, препятствующие проведению качественного суточного мониторирования АД (СМАД): постоянная форма фибрилляции предсердий, психические заболевания и др.,
- регистрация разовых значений систолического АД (САД) ≥200 мм рт.ст. или диастолического АД (ДАД) ≥115 мм рт.ст. при СМАД, самоконтроле или клиническом измерении АД,
- острые заболевания и сопутствующие хронические болезни в стадии обострения/декомпенсации,
- беременность, лактация.
Оценка отдельных характеристик АД
Вариабельность АД оценивали по данным СМАД с помощью SD (standard deviation); отдельно анализировали дневной и ночной периоды (07:00-22:59 ч, 23:00-06:59 ч, соответственно). Также по данным СМАД анализировали степень ночного снижения (СНС) АД, которую рассчитывали по формуле: СНС АД =[(АДд-АДн)/АДд]×100%, где АДд — уровень АД в дневное время, АДн — уровень АД в ночное время. Фенотип АД классифицировали как соотношение клинического и амбулаторного АД в зависимости от соответствия пороговым значениям; учитывали 4 фенотипа — эффективная АГТ (показатели АД ниже пороговых), гипертония белого халата на лечении (повышено только клиническое АД), скрытая неэффективность АГТ (повышено только амбулаторное АД), неэффективная АГТ (повышено и клиническое, и амбулаторное АД) [6].
Основные характеристики пациентов
Последовательно включено 156 амбулаторных больных АГ II-III стадии, из них в группу без БОД — 87 пациентов, в группу с БОД — 69 (49 с БА, 20 с ХОБЛ). Средний возраст составил 63,4±8,8 лет, женщин было 72,4%. Пациенты с БОД оказались старше (p=0,047), чаще имели анамнез воздействия профессиональных вредных факторов (р=0,001), группу инвалидности (р=0,001) и заболевания опорно-двигательного аппарата — 11,6 vs 2,3% (p=0,019). По другим сопутствующим заболеваниям и их количеству, факту курения в настоящее время или в прошлом, индексу курения группы не различались [5]. Монотерапию АГ получали 28,8% пациентов, остальные — комбинацию из ≥2 антигипертензивных препаратов. 60,9% пациентов принимали препараты регулярной терапии сопутствующих заболеваний. Регулярную терапию БОД или препараты для купирования респираторных симптомов принимали 78,3% пациентов. Пациенты с БОД в 2 раза реже принимали статины и антиагреганты или антикоагулянты (таблица 1).
Показатели клинического АД в среднем превышали целевой уровень в обеих группах (соответствовали АГ 1 ст.). Амбулаторное АД по данным СМАД в среднем не превышало пороговых значений. Однако и клиническое, и амбулаторное АД было выше в группе с БОД, как и вариабельность САД. Эти и другие характеристики пациентов представлены в таблице 2. Для оценки значимости различий количественных переменных использовали дисперсионный анализ (ANOVA), категориальных — критерий Пирсона.
Таблица 1
Регулярная терапия при включении в исследование, %
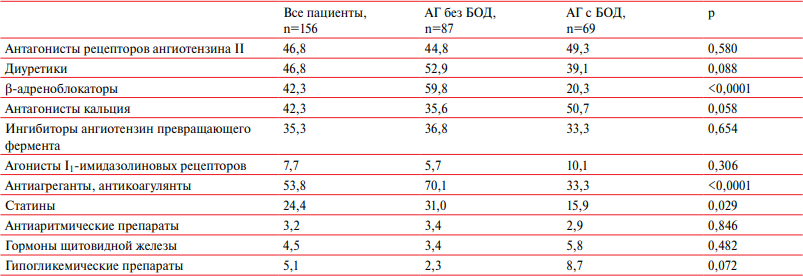
Примечание: р — оценка различий между группами АГ без БОД и АГ с БОД. АГ — артериальная гипертония, БОД — болезни органов дыхания.
Таблица 2
Инструментальные и лабораторные данные на визите включения*
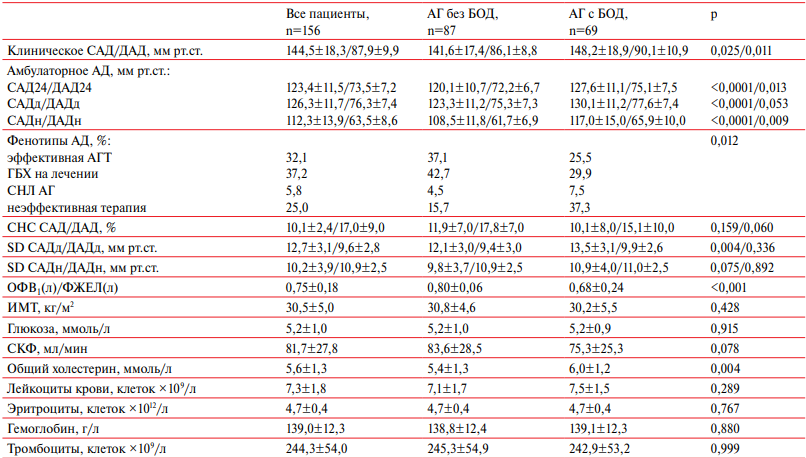
Примечание: * — данные представлены как среднее и стандартное отклонение (M±SD), если не указаны проценты. 24 — среднесуточный показатель, д — усредненный показатель за день, н — усредненный показатель за ночь, SD — вариабельность АД, ОФВ1/ФЖЕЛ — соотношение объема форсированного выдоха за первую сек. к форсированной жизненной емкости легких по данным спирометрии после ингаляции сальбутамола 400 мкг, р — значимость различий между группами АГ без БОД и АГ с БОД, АГ — артериальная гипертония, АД — артериальное давление, АГТ — антигипертензивная терапия, БОД — болезни органов дыхания, ГБХ — гипертония "белого халата", ДАД — диастолическое АД, ИМТ — индекс массы тела, САД — систолическое АД, СКФ — скорость клубочковой фильтрации, СНЛ — скрытая неэффективность лечения, СНС — степень ночного снижения.
Основные результаты проспективного наблюдения
Продолжительность наблюдения варьировала от 6 до 39 мес., в среднем — 29,3±8,0 мес. Все визиты исследования прошли 143 пациента: 7 отказались от дальнейшего участия, 4 умерли, 2 поменяли место жительства. Причины смерти: острая сердечная недостаточность (n=2), прогрессирование дыхательной недостаточности, как осложнения ХОБЛ (n=1), рак предстательной железы (n=1). Исходы, вошедшие в комбинированную первичную конечную точку (ПКТ), зарегистрированы у 32 пациентов (смерть, серьезные сердечно-сосудистые события и осложнения), вторичную конечную точку (ВКТ) — у 57 (госпитализации, вызовы скорой медицинской помощи и временная нетрудоспособность в связи с ССЗ или БОД, гипертонический криз, обострение БА/ХОБЛ, пневмония, дыхательная недостаточность), третичную конечную точку (ТКТ) — у 76 (другие клинически значимые заболевания и состояния). Подробнее неблагоприятные события описаны в 1 части статьи [5].
Статистический анализ
Взаимосвязь характеристик исследуемых пациентов с исходами, вошедшими в конечную точку (предикторы), изучали в регрессионном анализе. Статистически значимой считали независимую связь характеристики с исходом, если p<0,05. В качестве возможных предикторов рассматривали следующие параметры: социально-демографические, антропометрические, анамнестические и лабораторные данные, усредненные значения АД (клинического, дневного, ночного), показатели вариабельности клинического и амбулаторного АД, СНС и фенотип АД, данные вопросника ACQ-5 (Asthma Control Questionnaire) и теста САТ (COPD Assessment Test) [7][8], классы препаратов, учитывали наличие моно- или комбинированной АГТ. На заключительном этапе анализа в модель вводили переменную "БОД".
Результаты
В регрессионном анализе комбинированная ПКТ оказалась прямо взаимосвязана с вариабельностью ночного ДАД, уровнем лейкоцитов и обратно связана с СНС ДАД (таблица 3). Принадлежность к группе с БОД не вносила вклад в развитие ПКТ. Однако напомним, что кривые выживаемости, составляющие комбинацию данных исходов, между больными АГ с и без БОД, расходились после 10 мес. наблюдения [5].
События ВКТ были прямо связаны с указанием на высокие значения САД в анамнезе (до включения в исследование) и отрицательно — с приемом статинов и уровнем тромбоцитов крови. При введении в регрессионную модель факта принадлежности к группе с БОД указанные параметры не теряли значимости и фактор "БОД" также являлся независимым предиктором событий ВКТ (таблица 4).
С исходами, включенными в ТКТ, были прямо связаны уровень клинического САД >139 мм рт.ст. и длительность АГ, отрицательно — СНС ДАД. Принадлежность к группе с БОД оказалась самой весомой — значимость других факторов снизилась до уровня тенденции (таблица 5).
Другие характеристики пациентов, включая курение, индекс массы тела, класс и количество антигипертензивных препаратов, фенотип АД, показатели функции внешнего дыхания, препараты для лечения БА и ХОБЛ, не были связаны с исходами у изучавшихся пациентов.
Таблица 3
Предикторы комбинированной ПКТ у больных АГ с учетом БОД (регрессия Кокса; n=156, длительность наблюдения 29,3±8,0 мес.)
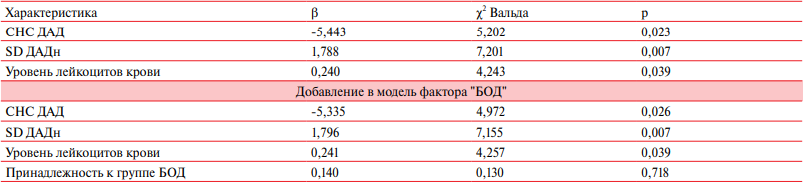
Примечание: БОД — болезни органов дыхания, ДАД — диастолическое артериальное давление, СНС — степень ночного снижения, SD ДАДн — вариабельность диастолического артериального давления ночью.
Таблица 4
Предикторы ВКТ (регрессия Кокса; n=156, длительность наблюдения 29,3±8,0 мес.)
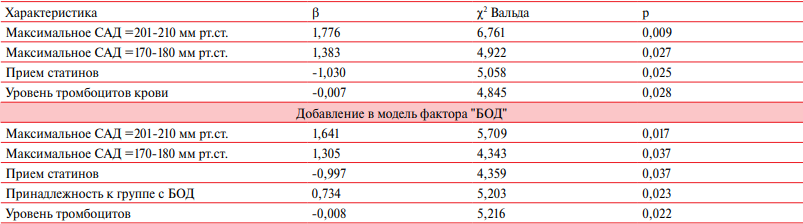
Примечание: БОД — болезни органов дыхания, САД — анамнестические сведения о максимальных значениях систолического артериального давления.
Таблица 5
Предикторы ТКТ (регрессия Кокса; n=156, длительность наблюдения 29,3±8,0 мес.)
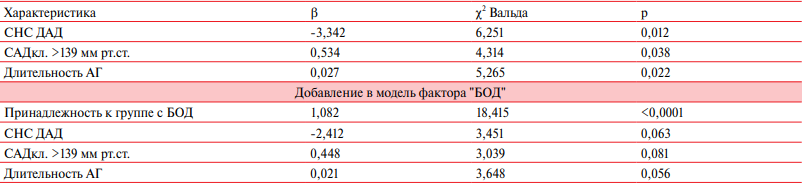
Примечание: АГ — артериальная гипертония, БОД — болезни органов дыхания, ДАД — диастолическое артериальное давление, САДкл. — клиническое систолическое артериальное давление, СНС — степень ночного снижения.
Обсуждение
Предикторы комбинированной ПКТ
Известно, что неблагоприятные исходы у пациентов с АГ ассоциированы и с традиционными ФР (возраст, мужской пол, курение, ожирение и другие), и с эффективностью контроля АД [6]. У пациентов с БОД, кроме указанных выше ФР, отмечают взаимосвязь ССЗ и летальных исходов с показателями функции внешнего дыхания, частотой и тяжестью обострений БОД. В исследовании Mannino DM, et al. было убедительно показано, что 5-летняя выживаемость больных АГ (n=8137) зависит от выраженности обструкции дыхательных путей [9]. Результаты настоящей работы таких взаимосвязей с комбинированной ПКТ не обнаружили (меньшая длительность наблюдения). Однако ПКТ была независимо ассоциирована с вариабельностью ДАД ночью и СНС ДАД, уровнем лейкоцитов крови — маркера системного воспаления (таблицы 2, 3; по этим показателям группы пациентов в среднем не отличались). Более крупные исследования также показывают, что вариабельность и СНС АД связаны с неблагоприятным прогнозом. Например, в работе Celik M, et al. вариабельность САД была независимо ассоциирована с повышенным сердечнососудистым риском при его оценке с помощью The Pooled Cohort Risk Assessment Equations 10-year risk calculator (n=250, отношение рисков (ОР) 1,26; 95% доверительный интервал (ДИ): 1,08-1,47, р=0,004) [10], а СНС АД (n=9828) с риском смерти в анализе базы данных IDACO (the International Database of Ambulatory blood pressure in relation to Cardiovascular Outcome): для СНС САД ОР смерти от всех причин составлял 1,13 (95% ДИ: 1,07-1,19, р<0,0001), для СНС ДАД этот ОР был 1,12 (95% ДИ: 1,06-1,19, р<0,001), при этом только для СНС ДАД был повышен ОР смерти от сердечно-сосудистых причин (1,10; 95% ДИ: 1,00-1,21, р<0,05) и всех сердечно-сосудистых событий (1,07; 95% ДИ: 1,00-1,13, р<0,05) [11].
Системное воспаление является патогенетической основной многих острых и хронических заболеваний, включая БОД, ССЗ и сердечно-сосудистые осложнения (ССО) [12][13]. В крупном исследовании больных ХОБЛ (n=8656) уровень лейкоцитов крови >9×109/л, как и уровень С-реактивного белка, фибриногена, был ассоциирован с 2-4-кратным риском инфаркта миокарда, сердечной недостаточности, сахарного диабета, рака легкого и пневмонии [14].
Отсутствие вклада БОД в настоящем исследовании в развитие летального исхода, ССО и других событий ПКТ, по-видимому, связано с относительно небольшим периодом наблюдения и количеством пациентов, особенно с ХОБЛ.
Предикторы ВКТ
Взаимосвязь ВКТ в представленной работе с анамнестическими сведениями о САД ≥170 мм рт.ст. свидетельствует о весьма неудовлетворительном до включения в исследование контроле АД. Возможно, именно у этих же пациентов хуже контролировалось АД и в течение периода наблюдения. Можно только предположить, что пациенты с таким анамнезом характеризуются плохим контролем ФР, низкой приверженностью АГТ. При этом отрицательная взаимосвязь приема статинов с данным типом конечной точки (таблица 4), частота компонентов которой отличалась между группами преимущественно за счет "респираторных" событий [5], еще раз свидетельствует, на наш взгляд, о плейотропном противовоспалительном эффекте данного класса препаратов. Именно этим эффектом объясняют снижение частоты обострений ХОБЛ у пациентов, нуждающихся в назначении статинов по прямым показаниям [15][16]. Например, в когортном исследовании Huang CC, et al. прием статинов достоверно снижал риск госпитализации в связи с ХОБЛ (n=6252; ОР 0,66; 95% ДИ: 0,60-0,74; р<0,001) [17]. Прием статинов также ассоциируют с улучшением контроля АД и антиагрегантным эффектом [18][19]; их вклад в снижение сердечно-сосудистого риска у больных с нарушениями липидного обмена в комментариях не нуждается.
Настоящее исследование демонстрирует независимый вклад самих БОД в вероятность развития гипертонического криза, госпитализации с ССЗ и других событий ВКТ, включая "респираторные" (таблица 4). При этом, взаимосвязь ВКТ с препаратами для лечения БОД отсутствует. Существенные повышения уровня АД у пациентов с БОД известны многие десятилетия [20-23], а плохой контроль БА или ХОБЛ ассоциирован не только с риском их обострений и осложнений, ССО, но и с летальным исходом [24-26].
Обращает на себя внимание находка значимого, хотя и наименьшего по значению β-коэффициента, вклада в развитие ВКТ в представленной регрессионной модели уровня тромбоцитов крови. Можно предположить, что данный факт опосредован приемом каких-либо препаратов (например, нестероидных противовоспалительных (НПВП) по поводу заболеваний опорно-двигательного аппарата, частота их значимо выше в группе с БОД) или повышенной агрегацией тромбоцитов с формированием микроагрегатов (особенно в случае малых размеров тромбоцитов), которая при использовании автоматических анализаторов может не определяться, но привести к недооценке их уровня и состояния [27]. Данную гипотезу можно поддержать тем, что с приемом НПВП ассоциируют ухудшение контроля АД, в частности у принимающих ингибитор ангиотензинпревращающего фермента, ухудшение контроля БА, обострение ХОБЛ, ухудшение прогноза больных ССЗ. Эти события отмечались и в настоящем исследовании, однако их связь с приемом НПВП не анализировалась. В то же время данный параметр (уровень тромбоцитов) мог оказаться значимым в модели анализа из-за ограничений работы, но представляется интересным для изучения в более крупных исследованиях больных АГ с БОД.
Предикторы ТКТ
У обследованных пациентов с АГ хронические БОД явились доминирующим фактором, ассоциированным с ТКТ (таблица 5). Напомним, что основную их часть составили: ухудшение течения БА (у 1/3 пациентов) и ХОБЛ (у 1/2 пациентов) по данным ACQ-5 и САТ, острый бронхит в группе с БОД, а также ухудшение течения АГ без развития гипертонического криза, потребовавшее коррекции АГТ. Последний факт значимо чаще регистрировался у пациентов с БОД (33,3%), чем без БОД (19,5%) [5]. Опираясь на эти данные, вновь можно предположить, что при более длительном наблюдении БОД, особенно при неудовлетворительном их контроле, могли оказаться предиктором ПКТ в представленной когорте пациентов с АГ.
Ограничения исследования. Основными ограничениями исследования являются относительно небольшое количество включенных пациентов и длительность наблюдения, объединение пациентов с БА и ХОБЛ в одну группу, их разное количество. Дополнительным ограничением является оценка связи исходов, включавших характеристики АД, с другими параметрами АД, которые могут быть взаимозависимы.
Заключение
БОД существенно влияют на течение ССЗ и прогноз в целом. Пациенты с АГ нуждаются в рациональной многофакторной профилактике, регулярном диспансерном наблюдении. Необходимо у больных АГ лучше контролировать клиническое и амбулаторное АД, показатели липидного спектра крови, особенно при наличии БОД. Целесообразно чаще использовать метод СМАД в рутинной практике не только для оценки уровня АД, но и таких дополнительных показателей, как СНС и вариабельность. Весьма важен и оптимальный контроль самих БОД, включая профилактику обострений, респираторных инфекций. Требуются более крупные исследования в области изучения коморбидности АГ и БОД, в т.ч. с разработкой специальных подходов к ведению таких пациентов для предупреждения неблагоприятных событий.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Chen W, Thomas J, Sadatsafavi M, et al. Risk of cardiovascular comorbidity in patients with chronic obstructive pulmonary disease: a systematic review and meta-analysis. Lancet Respir Med. 2015;3(8):631-9. doi:10.1016/S2213-2600(15)00241-6.
2. Бойцов С. А., Погосова Н. В., Палеев Ф. Н. и др. Клиническая картина и факторы, ассоциированные с неблагоприятными исходами у госпитализированных пациентов с новой коронавирусной инфекцией COVID-19. Кардиология. 2021;61(2):4-14. doi:10.18087/cardio.2021.2.n1532.
3. Mehra MR, Desai SS, Kuy S, et al. Cardiovascular Disease, Drug Therapy, and Mortality in COVID-19. N Engl J Med. 2020;382(25):e102. doi:10.1056/NEJMoa2007621.
4. Бойцов С. А., Драпкина О. М., Шляхто Е. В. и др. Исследование ЭССЕ-РФ (Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в регионах Российской Федерации). Десять лет спустя. Кардиоваскулярная терапия и профилактика. 2021;20(5):3007. doi:10.15829/1728-8800-2021-3007.
5. Смирнова М. И., Курехян А. С., Горбунов В. М. и др. Результаты проспективного наблюдения больных артериальной гипертонией с сопутствующими хроническими болезнями органов дыхания в рутинной практике. Часть I. Характеристика неблагоприятных событий. Кардиоваскулярная терапия и профилактика. 2022;21(10):3383. doi:10.15829/1728-8800-2022-3383. EDN RCAAZO.
6. Артериальная гипертензия у взрослых. Клинические рекомендации 2020. Российский кардиологический журнал. 2020;25(3):3786. doi:1015829/1560-4071-2020-3-3786.
7. Juniper EF, Svensson K, Mörk AC, et al. Measurement properties and interpretation of three shortened versions of the asthma control questionnaire. Respir Med. 2005;99(5):553-8. doi:10.1016/j.rmed.2004.10.008.
8. Белевский А. С. Новый тест для оценки течения ХОБЛ: САТ тест. Практическая пульмонология. 2010;1:37-9.
9. Mannino DM, Thorn D, Swensen A, et al. Prevalence and outcomes of diabetes, hypertension and cardiovascular disease in COPD. Eur Respir J. 2008;32(4):962-9. doi:10.1183/09031936.00012408.
10. Celik M, Yuksel UC, Yildirim E, et al. The relationship between blood pressure variability and Pooled Cohort Risk Assessment Equations 10-year cardiovascular risk score. Blood Press Monit. 2016;21(5):282-7. doi:10.1097/MBP.0000000000000200.
11. Stolarz-Skrzypek K, Thijs L, Richart T, et al. Blood pressure variability in relation to outcome in the International Database of Ambulatory blood pressure in relation to Cardiovascular Outcome. Hypertens Res. 2010;33(8):757-66. doi:10.1038/hr.2010.110.
12. Метельская В. А., Гуманова Н. Г. Валидные кардиоспецифические биохимические маркеры. Часть I. Кардиоваскулярная терапия и профилактика. 2020;19(4): 2573. doi:10.15829/1728-8800-2020-2573.
13. Гуманова Н. Г., Климушина М. В., Богданова Н. Л. и др. Валидные кардиоспецифические биохимические маркеры. Часть II. Кардиоваскулярная терапия и профилактика. 2020;19(5):2588. doi:10.15829/1728-8800-2020-2588.
14. Thomsen M, Dahl M, Lange P, et al. Inflammatory Biomarkers and Comorbidities in Chronic Obstructive Pulmonary Disease. AJRCCM. 2012;186:982-8. doi:10.1164/rccm.201206-1113OC.
15. Ingebrigtsen TS, Marott JL, Nordestgaard BG, et al. Statin use and exacerbations in individuals with chronic obstructive pulmonary disease. Thorax. 2015;70(1):33-40. doi:10.1136/thoraxjnl-2014-205795.
16. Герасимова Е. Б., Баздырев Е. Д., Смакотина С. А. и др. Эффективность гиполипидемической терапии у пациентов с хронической обструктивной болезнью лёгких. Journal of Siberian Medical Sciences. 2014;2.
17. Huang CC, Chan WL, Chen YC, et al. Statin use and hospitalization in patients with chronic obstructive pulmonary disease: a nationwide population-based cohort study in Taiwan. Clin Ther. 2011;33(10):1365-70. doi:10.1016/j.clinthera.2011.08.010.
18. Рубаненко О. А., Кириченко Н. А., Фатенков О. В. Оптимизация гемостазиологических показателей под влиянием терапии статинами у больных ишемической болезнью сердца. Атеросклероз и дислипидемии. 2015;2:50-5.
19. Федоришина О. В., Протасов К. В., Торунова А. М. Влияние статина при добавлении к антигипертензивной терапии на показатели сосудистой жёсткости у больных артериальной гипертензией высокого сердечно-сосудистого риска. Acta Biomedica Scientifica. 2018;3(5):27-32. doi:10.29413/ABS.2018-3.5.4.
20. Jarvinen KA. Fluctuation of arterial blood pressure in asthma. Br Med J. 1957;1(5031):1328-30. doi:10.1136/bmj.1.5031.1328.
21. Мухарлямов Н. М., Саттбеков Ж. С., Сучков В. В. Системная артериальная гипертензия у больных хроническими неспецифическими заболеваниями легких. Кардиология. 1974;12;(34):55-61.
22. Козырев А. Г., Жданов В. Ф. Дневные колебания артериального давления и пиковой объемной скорости выдоха у больных бронхиальной астмой в сочетании с гипертонической болезнью. Пульмонология. 2003;(2):52-6.
23. Боровков Н. Н., Добротина И. С., Бердникова Л. В. Особенности артериального давления по данным суточного мониторирования у больных артериальной гипертензией на фоне обострения бронхиальной астмы. Медицинский альманах. 2012;(1):183-5.
24. Raita Y, Camargo CA Jr, Faridi MK, et al. Risk of Acute Myocardial Infarction and Ischemic Stroke in Patients with Asthma Exacerbation: A Population-Based, Self-Controlled Case Series Study. J Allergy Clin Immunol Pract. 2020;8(1):188-94.e8. doi:10. 1016/j.jaip.2019.06.043.
25. Donaldson GC, Hurst JR, Smith CJ, et al. Increased risk of myocardial infarction and stroke following exacerbation of COPD. Chest. 2010;137(5):1091-7. doi:10.1378/chest.09-2029.
26. Демко И. В., Петрова М. М., Гордеева Н. В. и др. Бронхиальная астма: особенности клинического течения и лечения в сочетании с патологией сердечно-сосудистой системы. Сибирское медицинское обозрение. 2008;52(4):71-7.
27. Cattaneo M, Cerletti C, Harrison P, et al. Recommendations for the Standardization of Light Transmission Aggregometry: A Consensus of the Working Party from the Platelet Physiology Subcommittee of SSC/ISTH. J Thromb Haemost. 2013;11(6):1183-9. doi:10.1111/jth.12231.
Об авторах
М. И. СмирноваРоссия
Марина Игоревна Смирнова — кандидат медицинских наук, руководитель лаборатории профилактики хронических болезней органов дыхания.
Москва
В. М. Горбунов
Россия
Владимир Михайлович Горбунов — доктор медицинских наук, профессор, руководитель лаборатории применения амбулаторных диагностических методов в профилактике хронических неинфекционных заболеваний.
Москва
А. С. Курехян
Россия
Армине Сарибековна Курехян — научный сотрудник лаборатории профилактики хронических болезней органов дыхания.
Москва
Г. Ф. Андреева
Россия
Галия Фатиховна Андреева — кандидат медицинских наук, старший научный сотрудник лаборатории применения амбулаторных диагностических методов в профилактике хронических неинфекционных заболеваний.
Москва
Я. Н. Кошеляевская
Россия
Яна Николаевна Кошеляевская — программист лаборатории применения амбулаторных диагностических методов в профилактике хронических неинфекционных заболеваний.
Москва
А. Д. Деев
Россия
Александр Дмитриевич Деев — кандидат физико-математических наук, ведущий научный сотрудник отдела эпидемиологии хронических неинфекционных заболеваний.
Москва
Дополнительные файлы
Рецензия
Для цитирования:
Смирнова М.И., Горбунов В.М., Курехян А.С., Андреева Г.Ф., Кошеляевская Я.Н., Деев А.Д. Результаты проспективного наблюдения больных артериальной гипертоний с сопутствующими хроническими болезнями органов дыхания в рутинной практике. Часть II. Предикторы неблагоприятных событий. Кардиоваскулярная терапия и профилактика. 2022;21(12):3424. https://doi.org/10.15829/1728-8800-2022-3424
For citation:
Smirnova M.I., Gorbunov V.M., Kurekhyan A.S., Andreeva G.F., Koshelyaevskaya Ya.N., Deev А.D. Results of the prospective observation in routine practice of hypertensive patients with concomitant chronic respiratory diseases. Part II. Predictors of adverse events. Cardiovascular Therapy and Prevention. 2022;21(12):3424. (In Russ.) https://doi.org/10.15829/1728-8800-2022-3424
JATS XML

























































