Перейти к:
Динамика закрытия резидуального шунта в течение одного года после эндоваскулярного закрытия открытого овального окна: клиническое исследование
https://doi.org/10.15829/1728-8800-2024-4040
Аннотация
Цель. Изучить динамику закрытия резидуального шунта (РШ) после выполнения эндоваскулярного закрытия открытого овального окна (ООО) в течение 12 мес.
Материал и методы. Проанализированы данные 80 пациентов, которым выполняли эндоваскулярное закрытие ООО в ФГБУ "НМИЦК им. акад. Е. И. Чазова" Минздрава России в период 20182023гг. Всем пациентам выполняли полный объем обследований согласно действующим клиническим рекомендациям. Степень выраженности РШ непосредственно после имплантации окклюдера, а также через 1, 6 и 12 мес. после вмешательства оценивали на основании чреспищеводной эхокардиографии с пузырьковой пробой в рамках контрольного визита пациентов.
Результаты. В послеоперационном периоде РШ визуализировался у 17,5% (n=14) пациентов. Значимым являлся сброс у 7,5% (n=6) больных. Через 1 мес. после вмешательства остаточный значимый сброс сохранялся у 10,0% (n=8) пациентов. Через 6 мес. РШ визуализировался у 2,5% (n=2) пациентов, а через 12 мес. только у одного больного (1,3%). Доля пациентов с РШ через 1 мес. после вмешательства снизилась до 42,9%, через 6 мес. до 85,7%, а через 12 мес. до 92,9% (p<0,05).
Заключение. Для большинства пациентов с РШ после эндоваскулярного вмешательства по поводу ООО характерна полная эндокардиализация окклюдера и закрытие ООО в течение первого года.
Для цитирования:
Терещенко А.С., Меркулов Е.В. Динамика закрытия резидуального шунта в течение одного года после эндоваскулярного закрытия открытого овального окна: клиническое исследование. Кардиоваскулярная терапия и профилактика. 2024;23(8):4040. https://doi.org/10.15829/1728-8800-2024-4040
For citation:
Tereshchenko A.S., Merkulov E.V. Dynamics of residual shunt closure within one year after endovascular patent foramen ovale closure: a clinical study. Cardiovascular Therapy and Prevention. 2024;23(8):4040. (In Russ.) https://doi.org/10.15829/1728-8800-2024-4040
Введение
Открытое овальное окно (ООО) — малая аномалия развития сердца, представляющая собой отверстие, располагающееся в межпредсердной перегородке в области овальной ямки [1]. Распространенность ООО, по данным литературы, достигает 25% [2]. Впервые данную аномалию описал итальянский хирург Леонардо Боттали в 1564г [3].
Развитие эндоваскулярных методов лечения способствовало тому, что в 1976г King TD выполнил первую имплантацию окклюдера по типу "double umbrella" в зону дефекта межпредсердной перегородки [4]. В настоящее время эндоваскулярная коррекция патологического межпредсердного сообщения стала полноправной альтернативой "открытому" хирургическому вмешательству [5].
Несмотря на высокие показатели безопасности и эффективности транскатетерных вмешательств, после эндоваскулярного закрытия может отмечаться неполная окклюзия дефекта [6][7]. В большинстве случаев после имплантации окклюдера происходит постепенное закрытие межпредсердного сообщения за счет эндокардиализации [8]. Однако, согласно опубликованным данным, у 20% пациентов может сохраняться остаточный сброс крови в левое предсердие, так называемый "резидуальный шунт" (РШ) [6][7]. Клинические проявления РШ зависят от его размера. "Золотым стандартом" диагностики и оценки объемов право-левостороннего патологического сброса является проведение "bubble test" (пузырьковой пробы), основанной на внутривенном введении физиологического раствора, содержащего микропузырьки воздуха. В результате, при тугом заполнении правого предсердия за счет право-левостороннего сброса в левых камерах сердца визуализируются микропузырьки, на основании подсчета которых возможно определить размер РШ [9][10]. Малые дефекты не оказывают негативного влияния на организм человека, тогда как шунты средних или больших размеров в 4 раза увеличивают риск развития повторных эмболических событий [11][12].
В связи с этим актуальной исследовательской задачей является изучение динамики закрытия РШ после эндоваскулярного закрытия ООО.
Материал и методы
В проспективное исследование были включены 80 пациентов, госпитализированных в ФГБУ "НМИЦК им. акад. Е. И. Чазова" Минздрава России за период 2018-2023гг для планового эндоваскулярного закрытия ООО.
Критериями включения в исследование являлось наличие в анамнезе криптогенного инсульта и/или транзиторной ишемической атаки. Все пациенты, принимавшие участие в исследовании, подписывали добровольное информированное согласие на проведение медицинских вмешательств и участие в клиническом исследовании.
Всем пациентам выполнялся объем диагностических мероприятий, соответствующий актуальным клиническим рекомендациям по ведению пациентов с ООО Минздрава России [13]. Связь между криптогенным инсультом и наличием ООО основывалась на подсчете баллов по шкале RoPe (Risk of Paradoxical Embolism) [14].
Перед проведением эндоваскулярного вмешательства по поводу ООО у всех пациентов оценивались клинико-анамнестические данные, а также результаты инструментальных (эхокардиография (ЭхоКГ), чреспищеводная ЭхоКГ (ЧП-ЭхоКГ)) исследований. Для оценки объема право-левостороннего патологического сброса при ЧП-ЭхоКГ выполнялась пузырьковая проба с подсчетом микропузырьков, визуализируемых в левых камерах сердца: "малым" считался сброс с визуализацией <20 пузырьков, "большим" — сброс с визуализацией ≥20 пузырей или занавесом.
Отдаленные исходы оценивались через 1, 6 и 12 мес. после проведенного вмешательства в рамках повторного визита, в ходе каждого из которых отмечалось наличие или отсутствие субъективных жалоб и выполнялась ультразвуковая визуализация для оценки эндокардиализации имплантированного окклюдера с проведением пузырьковой пробы.
Статистическую обработку данных проводили с использованием программного комплекса SPSS Statistica v. 26 ("IBM", США) и MedCalc v. 22.017 ("MedCalc Ltd", Бельгия). Проверка распределения непрерывных показателей на нормальность выполнялась с помощью теста Шапиро-Уилка. Показатели с распределением, отличным от нормального, описывались в виде медианы (Me) и интерквартильного размаха ([Q25; Q75]). Качественные признаки представлены в виде долей и частот выявления признака (%). Достоверность различия между изучаемыми несвязанными группами для качественных признаков выполнялась с использованием критерия χ2 Пирсона, в случае связанных выборок — с помощью теста МакНемара. Уровень значимости при проверке статистических гипотез соответствовал уровню ошибки первого рода, не превышающей 5%.
Результаты
После эндоваскулярного закрытия ООО были проанализированы данные 80 пациентов, средний возраст которых составил 43,2±11,8 лет, 60,0% (n=48) пациентов были женского пола. Клинико-анамнестическая характеристика пациентов представлена в таблице 1.
У четверти пациентов отмечалось нарушение липидного обмена (увеличение уровня общего холестерина ≥5,0 ммоль/л и/или холестерина липопротеинов низкой плотности ≥3,0 ммоль/л), обращала на себя внимание низкая распространенность артериальной гипертензии и сахарного диабета 1 и 2 типов в изученной когорте. Острое нарушение мозгового кровообращения ранее перенесли 67,5% пациентов. Средний балл по шкале RoPe (Risk of Paradoxical Embolism) составил 6,9 [ 6,0; 8,0].
Перед эндоваскулярным вмешательством всем больным выполнялись ЭхоКГ и ЧП-ЭхоКГ с пузырьковой пробой. Результаты инструментальных исследований представлены в таблице 1.
По данным ЭхоКГ дилатация левого предсердия — LAVi (Left Atrial Volume index) ≥34 мл/м2, отмечалась у 14,3% (n=6) пациентов. У 66,3% (n=53) пациентов визуализировался постоянный шунт, аневризма межпредсердной перегородки — у 67,5% (n=54) больных. При проведении пузырьковой пробы у 73,4% (n=59) пациентов визуализировалось ≥20 пузырьков в левых камерах сердца вплоть до занавеса, что свидетельствовало о большом размере шунта. Наличие дополнительных структур, таких как сеть Хиари или Евстахиева заслонка, выявлялись у 6,3% (n=5) пациентов.
Технический успех вмешательства составил 100% (n=80). Средняя длительность операции составила 58,3 [ 44,8; 70,0] мин. У большинства пациентов имплантирован окклюдер Amplatzer PFO (40% (n=32)), в остальных случаях применялись устройства Figulla Flex PFO и UNI. Развитие интраоперационных осложнений отмечено в 12,5% (n=10) случаев. При этом развитие осложнений было связано непосредственно с техническими аспектами вмешательства и не являлось реакцией на имплантированный окклюдер — 7,5% (n=6) vs 5,0% (n=4). Течение оперативного вмешательства представлено в таблице 2.
В послеоперационном периоде всем пациентам назначалась антитромбоцитарная терапия по схеме: прием Ацетилсалициловой кислоты по 100 мг и Клопидогрела по 75 мг 1 раз/сут. ежедневно в течение 6 мес. после эндоваскулярного закрытия ООО, затем в течение 5 лет монотерапия Ацетилсалициловой кислотой в дозировке по 100 мг 1 раз/сут. После имплантации окклюдера осложнения на госпитальном этапе возникли у 16,3% (n=13) пациентов. В послеоперационном периоде всем больным после закрытия ООО выполняли контрольную ультразвуковую визуализацию. РШ визуализировался у 17,5% (n=14) пациентов, при этом по данным пузырьковой пробы значимый сброс отмечен у 7,5% (n=6) больных. Течение раннего послеоперационного периода представлено в таблице 2.
Средний срок госпитализации составил 6,2 [ 4,0; 7,0] дней. В стабильном состоянии все пациенты были выписаны из стационара.
Через 1 мес. после вмешательства по данным контрольной ЧП-ЭхоКГ РШ со значимым сбросом сохранялся только у 10,0% (n=8) больных, по сравнению с данными в послеоперационном периоде. Через 6 мес. остаточный сброс сохранялся только у 2,5% (n=2) пациентов, по сравнению с предыдущими показателями. По результатам контрольной визуализации через 12 мес. после имплантации окклюдера доля пациентов с сохранившимся РШ снизилась до 1,3% (n=1). Несмотря на наличие РШ, тромбоэмболических осложнений у всей когорты пациентов в течение периода наблюдения отмечено не было.
Таким образом, при анализе результатов ультразвуковой визуализации непосредственно после эндоваскулярного вмешательства, а также через 1, 6 и 12 мес. после имплантации окклюдера зарегистрировано статистически значимое уменьшение доли пациентов с РШ, как при оценке динамики в целом, так и при попарном сравнении измерений (p<0,01), (рисунок 1).
Так, через 1 мес. после оперативного лечения число больных с остаточным сбросом снизилось на 42,9%, через 6 мес. — на 85,7%, а через 12 мес. — на 92,9% от исходного количества пациентов с РШ (p<0,01). Случаев рецидива право-левостороннего сброса за период наблюдения не отмечено.
Таблица 1
Клинико-анамнестическая характеристика пациентов и результаты инструментальных исследований до эндоваскулярного вмешательства
Показатель | n=80 |
Клинико-анамнестическая характеристика | |
Возраст, лет, Me [Q25; Q75] | 43,2 [ 35,8; 50,3] |
Женский пол, n (%) | 48 (60,0) |
ИМТ, кг/м2, Me [Q25; Q75] | 26,0 [ 22,7; 30,1] |
Курение, n (%) | 8 (10,0) |
Артериальная гипертензия, n (%) | 6 (7,5) |
Дислипидемия, n (%) | 21 (26,3) |
Атеросклероз сонных артерий, n (%) | 3 (3,8) |
ОНМК, n (%) | 54 (67,5) |
ТИА, n (%) | 26 (32,5) |
Сахарный диабет, n (%) | 3 (3,8) |
Систолическое АД при поступлении, мм рт.ст., Me [Q25; Q75] | 118,7 [ 110,0; 130,0] |
Диастолическое АД при поступлении, мм рт.ст., Me [Q25; Q75] | 75,0 [ 70,0; 80,0] |
Шкала RoPe, балл, Me [Q25; Q75] | 6,9 [ 6,0; 8,0] |
Результаты инструментальных исследований | |
ЭхоКГ | |
Размер ЛП, мм, Me [Q25; Q75] | 3,5 [ 3,1; 4,0] |
Объем ЛП, мл, Me [Q25; Q75] | 54,7 [ 41,0; 64,3] |
Дилатация ЛП (LAVi), мл/м2, Me [Q25; Q75] | 29,1 [ 22,9; 31,7] |
LAVi ≥34, мл/м, n (%) | 6 (14,3) |
Конечно-диастолический размер ЛЖ, мм, Me [Q25; Q75] | 4,8 [ 4,5; 5,0] |
Фракция выброса ЛЖ, %, Me [Q25; Q75] | 59,9 [ 60,0; 60,0] |
Толщина МЖП, см, Me [Q25; Q75] | 0,9 [ 0,8; 0,9] |
Масса миокарда ЛЖ, г/м2, Me [Q25; Q75] | 75,6 [ 65,3; 88,4] |
Размер ПП, мм, Me [Q25; Q75] | 16,5 [ 13,0; 18,0] |
СДЛА, мм рт.ст., Me [Q25; Q75] | 26,6 [ 24,0; 29,8] |
ЧП-ЭхоКГ | |
Прерывный шунт, n (%) | 27 (33,8) |
Постоянный шунт, n (%) | 53 (66,3) |
Аневризма МПП, n (%) | 54 (67,5) |
Аневризма по классификации Olivares-Reyes >3, n (%) | 29 (36,3) |
Длина тоннеля >12 мм, n (%) | 49 (61,3) |
Шунт, n (%): — средний (<20 пузырей) — большой (≥20 пузырей/занавес) | 21 (26,6) 59 (73,4) |
Дополнительные структуры, n (%): — сеть Хиари — Евстахиева заслонка — нет дополнительных структур | 1 (1,2) 4 (5,0) 75 (93,8) |
Примечание: LAVi — Left atrial volume index, RoPe — Risk of Paradoxical Embolism, АД — артериальное давление, ИМТ — индекс массы тела, ЛЖ — левый желудочек, ЛП — левое предсердие, МЖП — межжелудочковая перегородка, МПП — межпредсердная перегородка, ОНМК — острое нарушение мозгового кровообращения, ПП — правое предсердие, СДЛА — систолическое давление легочной артерии, ТИА — транзиторная ишемическая атака, ЧП-ЭхоКГ — чреспищеводная эхокардиография, ЭхоКГ — эхокардиография.
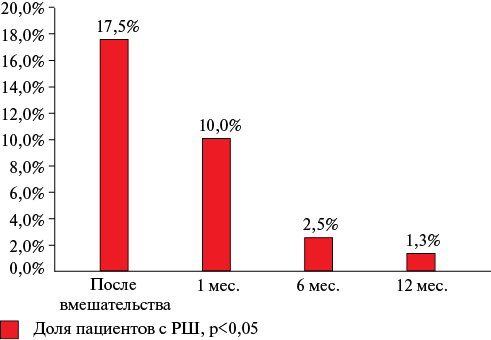
Рис. 1 Доля пациентов с РШ после эндоваскулярного закрытия ООО за весь период наблюдения.
Примечание: ООО — открытое овальное окно, РШ — резидуальный шунт.
Таблица 2
Эндоваскулярное закрытие ООО и течение госпитального периода
Показатель | n=80 |
Оперативное вмешательство | |
Длительность операции, мин, Me [Q25; Q75] | 58,3 [ 44,8; 70,0] |
Время облучения, сек, Me [Q25; Q75] | 652,9 [ 306,0; 742,5] |
Доза облучения, мЗВ, Me [Q25; Q75] | 8,8 [ 3,8; 12,6] |
Пункция МПП, n (%) | 4 (5,0) |
Окклюдер, n (%): — Amplatzer PFO — Figulla Flex PFO — Figulla Flex UNI | 32 (40,0) 30 (37,5) 18 (22,5) |
Интраоперационные осложнения, n (%) | 10 (12,5) |
Интраоперационные осложнения, связанные с устройством, n (%) | 4 (5,0) |
Интраоперационные осложнения, связанные с процедурой, n (%) | 6 (7,5) |
Течение госпитального периода | |
Срок госпитализации, дней, Me [Q25; Q75] | 6,2 [ 4,0; 7,0] |
Летальный исход, n (%) | 0 |
Осложнения на госпитальном этапе, n (%): — осложнения места доступа — повышение t тела >37,1о | 13 (16,3) 6 (7,5) 6 (7,5) |
УЗ-контроль после вмешательства | |
Контрольная визуализация, n (%): — трансторакальная ЭхоКГ — ЧП-ЭхоКГ — ВС-ЭхоКГ | 50 (62,5) 16 (20,0) 14 (17,5) |
Значимый сброс по данным пузырьковой пробы, n (%) | 6 (7,5) |
Остаточный кровоток, n (%) | 14 (17,5) |
Примечание: ВС-ЭхоКГ — внутрисердечная эхокардиография, МПП — межпредсердная перегородка, ООО — открытое овальное окно, УЗ — ультразвуковой, ЧП-ЭхоКГ — чреспищеводная эхокардиография, ЭхоКГ — эхокардиография.
Обсуждение
Наличие патологического сообщения между предсердиями даже после имплантации окклюдера тесно сопряжено с негативными последствиями в отдаленном периоде, в частности, с развитием повторных ишемических событий головного мозга [1][15][16].
В результате проведенного анализа установлено, что у большинства пациентов с визуализируемым остаточным сбросом непосредственно после эндоваскулярного закрытия ООО наблюдается его полная окклюзия в течение 12 мес.
Наличие остаточного сброса после имплантации окклюдера является широко распространённым осложнением после вмешательства. Так, на ранних этапах становления транскатетерных методик коррекции данной аномалии, число РШ, визуализируемых непосредственно после вмешательства, достигало 38% [7]. В более поздних исследованиях авторы отмечали небольшое снижение числа РШ. В исследовании Hammerstingl C, et al. (2011) из 124 пациентов с ООО у 34,7% (n=43) больных визуализировался остаточный межпредсердный сброс при контрольном обследовании через 24 ч после имплантации окклюдера [17]. Нами получены в целом более позитивные результаты: РШ визуализировался только в 17,5% случаев на госпитальном этапе.
Ряд авторов указывает на эндокардиализацию окклюдера в течение первых 3-х мес. после эндоваскулярного вмешательства. Так, в одноцентровом когортном исследовании, включавшем 730 пациентов с имплантированным окклюдером, у 7,1% (n=46) пациентов визуализировался РШ через 3 мес. после операции [18]. Схожие данные представлены в наблюдении Sorensen SG, et al. (2012), где, проанализировав данные 315 пациентов после эндоваскулярного закрытия ООО, у 7% (n=21) отмечалось сохранение остаточного кровотока через 3 мес. после вмешательства [6]. В нашем исследовании уже через 1 мес. после лечения количество РШ снизилось практически вполовину (динамика -42,9%, p=0,041).
При контрольном обследовании через 6 мес. после вмешательства нами также отмечено значимое снижение числа РШ до 2,5% (n=2), (p=0,0015). Уменьшение доли пациентов с остаточным сбросом через полгода после операции также было отмечено в опубликованных работах других исследователей. По мнению, Diaz T, et al. (2010), уменьшение числа больных с РШ через 6 мес. после эндоваскулярного вмешательства обусловлено размером исходного шунта. Так, проанализировав результаты обследования 424 пациентов после закрытия ООО, авторы отметили, что шунты малого размера, как правило, закрывались через 6 мес. после операции, тогда как шунты среднего или большого размеров визуализировались и на более поздних сроках [7]. На протяжении 6 мес. РШ среднего и большого размеров сохранялись у 5% (n=21) пациентов [7]. В исследовании Cheli M, et al. (2015) выполнили контрольную визуализацию у 120 пациентов с имплантированным окклюдером, при этом у 29% (n=35) больных ранее визуализируемый РШ отсутствовал через 6 мес. после проведенного вмешательства [8]. В недавно представленном исследовании Laissac Q, et al. (2023) из 174 пациентов, РШ через 6 мес. после имплантации окклюдера визуализировался только в 19,6% (n=31) случаев [19].
В изученной нами когорте больных через 12 мес. после эндоваскулярного закрытия ООО получены достаточно оптимистичные результаты — РШ сохранился только лишь у 1 пациента. В целом, опубликованные данные указывают на высокую частоту полного закрытия РШ у большинства пациентов. Так, в исследовании Gaspardone A, et al. (2020), при контроле 247 пациентов через год после вмешательства, отсутствие остаточного шунта отмечалось у 62% (n=142) больных [20]. Схожие результаты получены Nakayama R, et al. (2024), проанализировавших показатели 106 пациентов с имплантированным окклюдером за период с марта 2011г по январь 2022г. Через год после эндоваскулярного вмешательства РШ визуализировался лишь в четверти случаев [21]. По мнению ряда авторов, сохранение значимости остаточного сброса по данным пузырьковой пробы характерно для РШ, визуализируемых в отдаленном периоде после эндоваскулярного вмешательства [19][21]. В нашем исследовании также было отмечено, что через год после имплантации окклюдера единственный сохранившийся РШ являлся значимым.
Ограничением настоящего исследования являлся малый объем выборки пациентов, которые прошли все контрольные обследования через 1, 6 и 12 мес. после эндоваскулярного закрытия ООО.
Заключение
Наличие РШ после эндоваскулярного вмешательства является распространенным осложнением, однако у большинства пациентов происходит полная эндокардиализация окклюдера и закрытие дефекта в течение первого года после лечения. Полученные данные указывают на высокую эффективность имплантации окклюзирующих устройств пациентам с ООО, что в свою очередь может способствовать более эффективной профилактике повторных ишемических событий у больных данной группы.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Комаров А. Л., Кривошеева Е. Н., Макеев М. И. и др. Открытое овальное окно как причина рецидивирующих эмболических инсультов. Клиническое наблюдение. Терапевтический архив. 2022;94(9):1109-14. doi:10.26442/00403660.2022.09.201842.
2. Кужель Д.А., Матюшин Г.В., Савченко Е.А. Вопросы диагностики открытого овального окна. Сибирское медицинское обозрение. 2014;1(85):70-5.
3. Игишева Л.Н., Князева Е.В., Болгова И.В. и др. Открытое овальное окно у детей раннего возраста. Мать и дитя в Кузбассе. 2014;1(56):18-23.
4. King TD, Thompson SL, Steiner C, et al. Secundum atrial septal defect: nonoperative closure during cardiac catheterization. JAMA. 1976;235(23):2506-9. doi:10.1001/jama.1976.03260490024013.
5. Трошкинев Н. М., Тарасов Р.С. Транскатетерное закрытие множественных дефектов межпредсердной перегородки: интервенционные подходы и результаты. Комплексные проблемы сердечнососудистых заболеваний. 2023;12(4S):184-95. doi:10.17802/2306-1278-2023-12-4S-184-195.
6. Sorensen SG, Spruance SL, Smout R, et al. Transcranial Doppler quantification of residual shunt after percutaneous patent foramen ovale closure: correlation of device efficacy with intracardiac anatomic measures. J Interv Cardiol. 2012;25(3): 304-12. doi:10.1111/j.1540-8183.2011.00714.x.
7. Diaz T, Cubeddu RJ, Rengifo‐Moreno PA, et al. Management of residual shunts after initial percutaneous patent foramen ovale closure: A single center experience with immediate and long‐ term follow‐up. Catheter Cardiovasc Interv. 2010;76(1):145-50. doi:10.1002/ccd.22475.
8. Cheli M, Canepa M, Brunelli C, et al. Recurrent and Residual Shunts After Patent Foramen Ovale Closure: Results From a Long‐Term Transcranial Doppler Study. J Interv Cardiol. 2015; 28(6):600-8. doi:10.1111/joic.12255.
9. Кулеш А.А., Демин Д.А., Белопасова А.В. и др. Криптогенный инсульт. Часть 2: парадоксальная эмболия. Медицинский совет. 2021;19:16-33. doi:10.21518/2079-701X2021-19-16-33.
10. Рыбин С.Ю. Открытое овальное окно, как фактор риска развития ОНМК (клинический случай). Вселенная мозга. 2019;1(3):31-4.
11. Spies C, Strasheim R, Timmermanns I, et al. Patent foramen ovale closure in patients with cryptogenic thrombo-embolic events using the Cardia PFO occlude. Eur Heart J. 2006;27(3):365-71. doi:10.1093/eurheartj/ehi617.
12. Windecker S, Wahl A, Chatterjee T, et al. Percutaneous closure of patent foramen ovale in patients with paradoxical embolism: long-term risk of recurrent thromboembolic events. Circulation. 2000;101(8):893-8. doi:10.1161/01.CIR.101.8.893.
13. Бокерия Л.А., Архипов А.Н., Болотова Е.В. и др. Клинические рекомендации по ведению взрослых пациентов с врожденными пороками сердца. М.: НЦССХ им. АН Бакулева РАМН, 2010. c. 358. ISBN: 978-5-7982-0258-4.
14. Kent DM, Ruthazer R, Weimar C, et al. An index to identify stroke-related vs incidental patent foramen ovale in cryptogenic stroke. Neurology. 2013;81(7):619-25. doi:10.1212/WNL.0b013e3182a08d59.
15. Кузнецов А. Н., Виноградов О. И., Рыбалко Н.В. Этиопатогенез кардиоэмболического инсульта. Клиническая патофизиология. 2014;2:3-8.
16. Богданов Э. И. Ишемический инсульт в молодом возрасте. Неврологический вестник. 2012;44(2):30-40.
17. Hammerstingl C, Bauriedel G, Stüsser C, et al. Risk and fate of residual interatrial shunting after transcatheter closure of patent foramen ovale: a long term follow-up study. Eur J Med Research. 2011;16:13-9. doi:10.1186/2047-783X-16-1-13.
18. Taggart NW, Reeder GS, Lennon RJ, et al. Long‐term follow‐up after PFO device closure: outcomes and complications in a single‐ center experience. Catheter Cardiovasc Interv. 2017;89(1):124-33. doi:10.1002/ccd.26518.
19. Laissac Q, Levesque T, Bettinger N, et al. Incidence, predictive factors, and prognostic impact of residual shunt after percutenous patent foramen ovale closure. Arch Cardiovasc Dis Suppl. 2023;15(1):63-4. doi:10.1016/j.acvdsp.2022.10.118.
20. Gaspardone A, Sgueglia GA, De Santis A, et al. Predictors of residual right-to-left shunt after percutaneous suture-mediated patent fossa ovalis closure. Cardiovasc Interv. 2020;13(18):2112- 20. doi:10.1016/j.jcin.2020.06.004.
21. Nakayama R, Takaya Y, Akagi T, et al. Relationship between patent foramen ovale anatomical features and residual shunt after patent foramen ovale closure. Cardiovasc Interv Ther. 2024;39:200-6. doi:10.1007/s12928-023-00979-y
Об авторах
А. С. ТерещенкоРоссия
Терещенко Андрей Сергеевич — к.м.н., с.н.с. отдела рентгенэндоваскулярных методов диагностики и лечения
Москва
Е. В. Меркулов
Россия
Меркулов Евгений Владимирович — д.м.н., г.н.с. отдела рентгенэндоваскулярных методов диагностики и лечения
Москва
Дополнительные файлы
Что известно о предмете исследования?
- Наличие остаточного сброса после имплантации окклюдера сопряжено с развитием повторных ишемических событий головного мозга.
- У 29% пациентов с резидуальным шунтом (РШ) в течение 6 мес. после эндоваскулярного закрытия открытого овального окна наступает эндокардиализация окклюдера.
Что добавляют результаты исследования?
- Через 1 мес. после эндоваскулярного закрытия открытого овального окна доля пациентов с РШ снизилась вполовину.
- У 85,7% пациентов не визуализировался РШ через 6 мес. после вмешательства.
- Для большинства пациентов с РШ после имплантации окклюдера характерно его полное закрытие в течение первого года.
Рецензия
Для цитирования:
Терещенко А.С., Меркулов Е.В. Динамика закрытия резидуального шунта в течение одного года после эндоваскулярного закрытия открытого овального окна: клиническое исследование. Кардиоваскулярная терапия и профилактика. 2024;23(8):4040. https://doi.org/10.15829/1728-8800-2024-4040
For citation:
Tereshchenko A.S., Merkulov E.V. Dynamics of residual shunt closure within one year after endovascular patent foramen ovale closure: a clinical study. Cardiovascular Therapy and Prevention. 2024;23(8):4040. (In Russ.) https://doi.org/10.15829/1728-8800-2024-4040
JATS XML

























































