Перейти к:
Биохимический профиль сыворотки крови пациентов с декомпенсированной сердечной недостаточностью с сохраненной фракцией выброса в зависимости от наличия ожирения
https://doi.org/10.15829/1728-8800-2025-4453
EDN: TEWGYU
Аннотация
Цель. Провести сравнительный анализ комплекса кардиомаркеров, адипоцитокинов, белков теплового шока (БТШ) и биомаркеров ремоделирования межклеточного матрикса у пациентов с острой декомпенсацией сердечной недостаточности с сохраненной фракцией выброса (ОДСНсФВ) в зависимости от наличия ожирения и его степени.
Материал и методы. Обследован 151 больной ОДСНсФВ в возрасте 47-95 лет: 85 больных ОДСНсФВ с ожирением (индекс массы тела ≥30 кг/м2) в качестве основной группы и 66 пациентов с ОДСНсФВ без ожирения (индекс массы тела <30 кг/м2) в качестве группы сравнения. Уровень биохимических показателей крови определяли с использованием рутинных биохимических методов на анализаторах BS-800M1 (Mindray, КНР) и Maglumi 2000 (Snibe, КНР), а также иммуноферментным методом с применением фотометра MultisKan FC (Thermo, США) и наборов реагентов компаний Вектор-Бест (РФ), Ray-Biotech (США), Cloud-Clone (КНР), DBC (Канада) и Biovendor (Чехия).
Результаты. У больных ОДСНсФВ и ожирением выявлены статистически значимо более высокие медианы уровней лептина и соотношения лептин/адипонектин, чем у больных ОДСНСсФВ без ожирения, при этом уровни адипонектина и БТШ70 при ожирении были статистически значимо ниже. Медиана [Q25-Q75] концентрации БТШ27 при морбидном ожирении составила 4,7 [1,2-24,2] нг/мл и оказалась статистически значимо выше, чем у больных ожирением I и II ст. — 1,3 [0,3-2,7] и 0,6 [0,3-1,3] нг/мл, соответственно. У больных ОДСНСсФВ с толщиной эпикардиального жира ≥5 мм выявлена не только более высокая концентрация лептина и соотношения лептин/адипонектин, но и повышенное содержание в крови миоглобина.
Заключение. Для биохимического профиля сыворотки крови больных ОДСНсФВ выявлен ряд особенностей, связанных с ожирением, включая различия по основным показателям адипоцитокинового комплекса, а также биомаркерам клеточного стресса — БТШ 27 и БТШ70, что может свидетельствовать о вовлеченности ожирения в патогенез хронической сердечной недостаточности и патофизиологические процессы, происходящие при декомпенсации данного заболевания.
Ключевые слова
Для цитирования:
Тимофеев Ю.С., Метельская В.А., Иванова А.А., Дубовская Н.И., Рогожкина Е.А., Веденикин Т.Ю., Замятин Р.А., Борисова А.Л., Джиоева О.Н., Драпкина О.М. Биохимический профиль сыворотки крови пациентов с декомпенсированной сердечной недостаточностью с сохраненной фракцией выброса в зависимости от наличия ожирения. Кардиоваскулярная терапия и профилактика. 2025;24(7):4453. https://doi.org/10.15829/1728-8800-2025-4453. EDN: TEWGYU
For citation:
Timofeev Yu.S., Metelskaya V.A., Ivanova A.A., Dubovskaya N.I., Rogozhkina E.A., Vedenikin T.Yu., Zamyatin R.A., Borisova A.L., Dzhioeva O.N., Drapkina O.M. Serum biochemical profile in patients with decompensated heart failure with preserved ejection fraction depending on obesity. Cardiovascular Therapy and Prevention. 2025;24(7):4453. (In Russ.) https://doi.org/10.15829/1728-8800-2025-4453. EDN: TEWGYU
Введение
Согласно современным представлениям, хроническая (ХСН) сердечная недостаточность (СН) рассматривается как некий финал сердечно-сосудистого континуума, приводящий к возрастанию рисков неблагоприятных сердечно-сосудистых исходов [1-3]. ХСН с сохраненной фракцией выброса левого желудочка (ХСНсФВ) является наиболее распространенным фенотипом данной нозологии, частота ее выявления варьирует от 30 до 60% от всех случаев ХСН по зарубежным данным [3][4] и до 53% случаев от всех больных ХСН в России [5]. Развитие острой декомпенсации (ОДСН) ХСНсФВ (ОДСНсФВ) существенно ухудшает прогноз течения заболевания, при этом вероятность повторной декомпенсации и смерти повышается [2].
Пациенты с ХСНсФВ в большинстве случаев имеют определенное количество коморбидных заболеваний, включая артериальную гипертензию, сахарный диабет 2 типа, гиперлипидемию, фибрилляцию предсердий и ожирение [6]. Ожирение представляет собой мультифакториальное хроническое заболевание, характеризующееся как избыточным накоплением жировой ткани (ЖТ), так и аномалиями секреторной активности адипоцитов и других клеток ЖТ; ожирение в анамнезе является независимым предиктором широкого спектра сердечно-сосудистых заболеваний, включая ХСНсФВ [7]. Влияние ожирения на патогенез ХСНсФВ и ее декомпенсацию обусловлено широким комплексом гемодинамических, гормональных и метаболических изменений, ассоциированных с накоплением в организме ЖТ, в т.ч. эпикардиальной (ЭЖТ), для которой характерна высокая биохимическая активность, а анатомическая близость к миокарду способствует воздействию секретируемых ЭЖТ соединений непосредственно на миокард [4][8].
В настоящее время в научном сообществе нет полного понимания всего комплекса молекулярных механизмов, приводящих к декомпенсации СН. Открытыми остаются вопросы о биохимических путях, непосредственно вовлеченных в развитие ОДСНсФВ, а также о роли ожирения и ассоциированной с ним секреторной активности в этом процессе. На сегодняшний день известно, что ключевую роль в декомпенсации СН играют процессы гипертрофии миокарда, которые сопряжены с нарушением метаболизма кардиомиоцитов, что, в конечном счете, провоцирует их апоптоз с последующим замещением соединительной тканью. Эти нарушения сопровождаются каскадом биохимических процессов, включающих активацию протеолитических ферментов, и интенсификацией хронического воспаления [4][8][9].
Несмотря на активное изучение биомаркеров ожирения, в литературе практически не описаны биохимические профили больных ОДСНсФВ, включающие широкий комплекс аналитов, ассоциированных с определенными молекулярно-патогенетическими звеньями, вовлеченными в патогенез как СН, так и ожирения. С позиции оценки биологических изменений, происходящих при ОДСНсФВ на фоне ожирения, перспективным направлением представляется изучение факторов, связанных с секреторной активностью ЖТ — адипоцитокинов [9][10], поражением и ремоделированием миокарда — кардиомаркеров и биомаркеров ремоделирования внеклеточного матрикса [11-13], а также белков теплового шока (БТШ) — биологических маркеров клеточного стресса, как интегрального процесса, связанного с нарушением структурной целостности и функциональной активности внутриклеточных белков на фоне декомпенсации заболевания [14][15]. Поиск диагностических биомаркеров и их комплексов является достаточно нетривиальной задачей на стыке медицинской биохимии, лабораторной диагностики и кардиологии, поэтому разработка и использование мультимаркерных панелей позволит выделить ключевые биохимические процессы, детерминирующие развитие заболевания, разработать диагностические подходы к персонализированному раннему определению рисков осложнений.
Цель исследования — провести сравнительный анализ комплекса кардиомаркеров, адипоцитокинов, БТШ и биомаркеров ремоделирования межклеточного матрикса у пациентов с ОДСНсФВ в зависимости от наличия ожирения и его степени.
Материал и методы
В исследование включен 151 больной с диагнозом ОДСНсФВ в возрасте 47-95 лет, медиана (Me) [Q25-Q75] — 77 [ 69-84] лет, госпитализированных в городскую клиническую больницу им. В. В. Вересаева г. Москвы в период с 01.10.2023 по 01.04.2025. Пациенты были разделены на две группы согласно индексу массы тела (ИМТ): 85 пациентов с ОДСНсФВ и ожирением (ИМТ ≥30 кг/м2) в качестве основной группы и 66 пациентов с ОДСНсФВ без ожирения (ИМТ <30 кг/м2) в качестве группы сравнения. Между анализируемыми группами не было статистически значимых различий по возрасту, полу и предшествующему амбулаторному лечению (таблица 1).
Исследование проводилось в соответствии с принципами, изложенными в Хельсинкской декларации, и получило одобрение локального этического комитета ФГБУ "НМИЦ ТПМ" Минздрава России (протокол № 04-05/23 от 18.09.2023). Все пациенты подписывали информированное согласие на участие в исследовании. Исследование зарегистрировано в рецензируемой базе клинических исследований Clinical.Trials.gov под регистрационным номером NCT06114498.
Критерии включения в исследование: наличие установленного диагноза ОДСНсФВ, а именно: быстрое нарастание тяжести клинических проявлений, ставшее причиной экстренной госпитализации у пациента, уже страдающего ХСНсФВ [16]. Диагноз ОДСНсФВ устанавливался согласно актуальным клиническим рекомендациям при наличии фракции выброса (ФВ) левого желудочка >50% и характерных для диастолической дисфункции симптомов и признаков ХСН, структурных и/или функциональных изменений сердца, а также признаков ОДСН, включающих нарастание одышки, застойные явления, ортопноэ, клиническую картину "сердечной астмы", отека легких на фоне какого-либо триггера, например, колебаний артериального давления или нарушений сердечного ритма и проводимости, таких как пароксизм фибрилляции предсердий или брадикардия; повышение концентрации N-концевого промозгового натрийуретического пептида (NT-proBNP) >900 пг/мл у больных 50-75 лет и >1800 пг/мл у больных >75 лет [17]. Критерии невключения: наличие острых инфекционных заболеваний на момент госпитализации, злокачественные новообразования, острое нарушение мозгового кровообращения в течение последних 3 мес., тяжелые пороки клапанов сердца, тяжелые нарушения ритма и проводимости, требующие электрокардиостимуляции. Всем пациентам при поступлении проводилась трансторакальная эхокардиография по стандартному протоколу, а также оценивалась толщина эпикардиального жира (ТЭЖ) в мм.
Взятие крови для рутинных и иммуноферментных исследований биохимических показателей проводилось из кубитальной вены при поступлении до проведения каких-либо лечебных мероприятий, в т.ч. инициации медикаментозной терапии. Рутинные биохимические показатели определялись спектрофотометрическими, ионоселективным и турбидиметрическими методами на автоматическом анализаторе BS-800M1 (Mindray, Китай). Сывороточные концентрации NT-proBNP исследовались иммунохемилюминесцентным методом на иммунохимическом анализаторе Maglumi 2000 (Snibe, Китай).
Образцы крови, предназначенные для иммуноферментного анализа (ИФА), центрифугировалась в режиме 2000 g/10 мин при комнатной температуре, после чего аликвотированная сыворотка крови поступала в Банк биологического материала ФГБУ "НМИЦ ТПМ" Минздрава России, где хранилась при температуре -80 оC до момента проведения анализа. Для определения уровня миоглобина применялся набор реактивов "Миоглобин-ИФА-БЕСТ" компании Вектор-Бест (Россия) с аналитической чувствительностью 4 нг/мл и калибровочным диапазоном 0-1000 нг/мл в рекомендованном производителем разведении. Анализ кардиоваскулярного БТШ (квБТШ) проводился в нативной сыворотке с использование тест-системы "Human HSPb7 ELISA kit" (Cloud Clone, КНР) с аналитической чувствительностью 122 пг/мл и калибровочным диапазоном 0,312-20,0 нг/мл. Уровень БТШ27 определяли в нативной сыворотке с применением тест-системы "Human HSP27 ELIXA kit Assay Max" (Assay Pro, США) с калибровочным диапазоном 0-80 нг/мл и минимальной детектируемой концентрацией 0,16 нг/мл. Уровень БТШ70 также определяли в нативной сыворотке с применением набора "Human HSP70 ELISA kit" (Cloud Clone, КНР) c аналитической чувствительностью 1,33 нг/мл и калибровочным диапазоном до 200 нг/мл. Количественное определение лептина проводилось в нативной сыворотке с использованием набора для ИФА "Leptin ELISA" компании DBC (Канада), аналитическая чувствительность 0,5 нг/мл (калибровочный диапазон 0-100 нг/мл), а адипонектина — методом конкурентного ИФА с применением реактивов "Human Adiponectn ELISA" (Biovendor, Чехия), лимитом детекции 26 нг/мл (калибровочный диапазон 0,1-10 мкг/мл) в разведенной согласно инструкции производителя сыворотке. Соотношение лептин/адипонектин — расчетный коэффициент, полученный делением концентрации лептина на концентрацию адипонектина. Интерлейкин (ИЛ)-6 определялся в нативной сыворотке с применением стандартизованного набора реактивов "Интерлейкин-6 ИФА-БЕСТ, комплект 1" компании Вектор-Бест (Россия) с аналитической чувствительностью 0,5 пг/мл и калибровочным диапазоном 0-300 пг/мл. Концентрации матриксных металлопротеиназ (ММП)2 и ММП9 определялись в сыворотке, разведенной фосфатным буфером (0,01 ммоль/л PBS, pH=7,0-7,2) согласно инструкции производителя с применением наборов реактивов "ELISA kit for MMP2 Human" и "ELISA kit for MMP9 Human" (Cloud Clone, КНР) с лимитом детекции 0,114 и 0,122 нг/мл, соответственно, и калибровочным диапазоном 0,312-20,0 нг/мл. Уровень тканевого ингибитора ММП 1 типа (ТИМП-1) определялся в разведенной согласно инструкции производителя сыворотке крови с применением набора "TIMP1-ELISA-KIT" (RayBiotech, США) с аналитической чувствительностью 40 пг/мл и калибровочным диапазоном 25-18000 пг/мл. ИФА проводился в полуавтоматическом формате с промывкой на автоматическом микропланшетном вошере AnthosFluido, (Biochrom, Великобритания) и детекцией оптической плотности на фотометре MultisKan FC (Thermo, США).
Статистический анализ полученных данных проводился в программе Statistica 10 (Statsoft) и SPSS (IBM). Для сравнительного анализа исследуемых параметров между независимыми выборками использовались непараметрические критерии Манна-Уитни и Краскела-Уолисса, для сравнения качественных параметров применялся критерий χ2 (Chi-square). Результаты представлены в виде медианы (Ме) и интерквартильного размаха [Q25-Q75]. Корреляционный анализ проводился с применением непараметрического критерия Спирмена. Гипотезы принимались как статистически значимые при p<0,05.
Результаты
Согласно результатам проведенного сравнительного анализа, статистически значимых различий в рутинных биохимических показателях между группами пациентов с ОДСНсФВ с ожирением и без ожирения выявлено не было (таблица 1). Ме концентраций кардиоспецифических маркеров: NT-proBNP, миоглобина и квБТШ, а также маркеров ремоделирования межклеточного матрикса ММП2 и ММП9 и ТИМП-1 не продемонстрировали статистически значимых различий в зависимости от ИМТ исследуемых больных.
В то же время получены статистически значимые различия между пациентами исследуемых групп по сывороточным концентрациям БТШ70 — биомаркера, отражающего системный ответ на клеточный стресс; действительно, медиана его концентрации в сыворотке крови у больных, госпитализированных с ОДСНсФВ и ожирением, была ниже в 1,3 раза по сравнению с группой больных с ИМТ <30 кг/м2.
Исследуемые группы статистически значимо различались по содержанию в сыворотке крови лептина и адипонектина, а также по их соотношению. Так, Ме концентрации лептина в группе ОДСНсФВ с ожирением была более чем в 4 раза выше, чем у больных ОДСНсФВ без ожирения, а Ме соотношения концентраций лептин/адипонектин отличалась более чем в 5,8 раз (таблица 2).
Сравнительный анализ биохимических показателей в зависимости от степени ожирения показал, что концентрация БТШ27 была статистически значимо выше при ожирении III ст. (морбидном ожирении, ИМТ ≥40 кг/м2), относительно больных с ожирением I ст. (ИМТ 30-34,9 кг/м2) и II ст. (ИМТ 35-39,9 кг/м2), при этом Ме концентрации данного биомаркера у пациентов с морбидным ожирением превышала значения в других группах сравнения в 3,6 и 7,8 раз, соответственно (рисунок 1). Анализ других включенных в настоящее исследование биомаркеров не выявил статистически значимых различий в зависимости от степени ожирения.
С целью оценки возможной взаимосвязи биохимического профиля больных ОДСНсФВ с содержанием эпикардиального жира дополнительно проводился сравнительный анализ между больными с ТЭЖ ≥5 мм (n=88) и больными с ТЭЖ <5 мм (n=63). Статистически значимые различия между исследованными группами были получены для сывороточных концентраций миоглобина и лептина, а также соотношения лептин/адипонектин (рисунок 2). Согласно полученным данным, у больных с ТЭЖ ≥5 мм Ме концентрации миоглобина была выше в 1,2 раза, тогда как Ме концентрации лептина и соотношения лептин/адипонектин были выше в 3,8 и 3,6 раза, соответственно.
Анализ корреляционных связей между биохимическими маркерами выявил наличие прямых корреляционных связей высокой и средней силы между уровнями миоглобина и квБТШ (R=0,45; p<0,001) и ИЛ-6 с NT-proBNP (R=0,32; p<0,001). Корреляционный анализ не показал статистически значимых связей средней силы и более (R>0,3 по модулю) между возрастом больных ОДСНсФВ и концентрациями изучаемых аналитов, кроме аланинаминотрансферазы (R=-0,31; p=0,02).
Таблица 1
Клинико-антропометрическая и лабораторная характеристика исследуемых больных
|
Показатель |
Пациенты с ОДСНсФВ и ожирением (ИМТ ≥30 кг/м2), n=85 |
Пациенты с ОДСНсФВ без ожирения (ИМТ <30 кг/м2), n=66 |
p |
|
Возраст, лет, Me [Q25-Q75] |
76,0 [ 69,0-81,0] |
77,5 [ 70,0-85,0] |
0,11 |
|
Мужчины, n (%) |
16 (18,2) |
22 (33,3) |
0,06 |
|
ИМТ, кг/м2, Me [Q25-Q75] |
34,9 [ 32,0-38,7] |
26,7 [ 24,1-27,9] |
<0,001 |
|
Степень ожирения, n (%) I (ИМТ 30-34,9 кг/м2) II (ИМТ 35-39,9 кг/м2) III (ИМТ ≥40 кг/м2) |
44 (51,8) 22 (25,8) 19 (22,4) |
– |
– |
|
Предшествующее амбулаторное лечение, n (%): Ингибиторы РААС иНГЛТ2 Антикоагулянты β-блокаторы АМКР |
70 (82,4) 7 (8,2) 41 (48,2) 52 (61,2) 14 (16,5) |
58 (87,8) 5 (7,7) 30 (45,5) 31 (47,0) 7 (10,6) |
0,37 0,57 0,74 0,09 0,35 |
|
ФВ ЛЖ (по Симпсону), %, Me [Q25-Q75] |
55,0 [ 53,0-58,0] |
57,0 [ 54,0-59,0] |
0,08 |
|
АСТ, Ед/л, Me [Q25-Q75] |
22,5 [ 17,5-35,0] |
21,6 [ 17,0-42,4] |
0,92 |
|
АЛТ, Ед/л, Me [Q25-Q75] |
22,2 [ 16,0-37,4] |
22,9 [ 13,2-38,1] |
0,41 |
|
Общий билирубин, мкмоль/л, Me [Q25-Q75] |
9,7 [ 6,8-19,7] |
8,8 [ 7,2-15,1] |
0,52 |
|
Креатинин, мкмоль/л, Me [Q25-Q75] |
102,8 [ 78,7-139,2] |
102,8 [ 82,5-126,0] |
0,44 |
|
Мочевина, ммоль/л, Me [Q25-Q75] |
9,2 [ 6,8-14,7] |
8,3 [ 6,4-12,3] |
0,29 |
|
СКФ, CKD-EPI, мл/мин, Me [Q25-Q75] |
58,0 [ 42,0-80,0] |
58,5 [ 43,0-77,0] |
0,68 |
|
Калий, ммоль/л, Me [Q25-Q75] |
4,2 [ 3,9-5,0] |
4,1 [ 3,8-4,6] |
0,11 |
|
вчСРБ, мг/л, Me [Q25-Q75] |
9,1 [ 3,5-23,7] |
11,7 [ 6,8-25,2] |
0,13 |
Примечание: АЛТ — аланинаминотрансфераза, АМКР — антагонисты минералокортикоидных рецепторов, АСТ — аспартатаминотрансфераза, ИМТ — индекс массы тела, вчСРБ — С-реактивный белок, определенный высокочувствительным методом, иНГЛТ — ингибиторы натрий-глюкозного котранспортера 2-го типа, ОДСНсФВ — острая декомпенсация сердечной недостаточности с сохраненной фракцией выброса, РААС — ренин-ангиотензин-альдостероновая система, СКФ по CKD-EPI — скорость клубочковой фильтрации по формуле Chronic Kidney Disease Epidemiology Collaboration, ФВ ЛЖ — фракция выброса левого желудочка, Me [Q25-Q75] — медиана [интерквартильный размах].
Таблица 2
Уровни биохимических показателей у больных ОДСНсФВ в зависимости от наличия ожирения
|
Показатель, Me [Q25-Q75] |
Пациенты с ОДСНсФВ и ожирением (ИМТ ≥30 кг/м2), n=85 |
Пациенты с ОДСНсФВ без ожирения (ИМТ <30 кг/м2), n=66 |
p |
|
Кардиоспецифические биомаркеры |
|||
|
NT-proBNP, пг/мл |
2053 [ 1064-4395] |
1849 [ 903-4571] |
0,81 |
|
Миоглобин, нг/мл |
46,1 [ 37,1-57,4] |
44,1 [ 25,7-54,8] |
0,47 |
|
квБТШ, пг/мл |
1078 [ 961-1203] |
1054 [ 921-1969] |
0,92 |
|
Биомаркеры системного ответа на клеточный стресс |
|||
|
БТШ27, нг/мл |
1,23 [ 0,44-3,02] |
0,57 [ 0,32-2,9] |
0,15 |
|
БТШ70, нг/мл |
2,9 [ 2,1-4,6] |
3,8 [ 2,6-5,6] |
0,04 |
|
Адипоцитокины |
|||
|
Лептин, нг/мл |
39,4 [ 18,7-71,5] |
9,7 [ 3,5-25,5] |
<0,001 |
|
Адипонектин, мкг/мл |
5,7 [ 4,2-8,4] |
7,5 [ 4,6-9,4] |
0,047 |
|
Соотношение лептин/адипонектин |
7,0 [ 3,1-15,4] |
1,2 [ 0,4-4,7] |
<0,001 |
|
ИЛ-6, пг/мл |
9,6 [ 5,4-19,9] |
8,8 [ 3,7-19,2] |
0,38 |
|
Биомаркеры ремоделирования межклеточного матрикса |
|||
|
ММП2, нг/мл |
345,5 [ 307,5-368,0] |
344,5 [ 303,0-372,5] |
0,94 |
|
ММП9, нг/мл |
1084 [ 844-1490] |
1139 [ 642-1584] |
0,96 |
|
ТИМП-1, нг/мл |
369,9 [ 262,7-727,0] |
410,3 [ 266,0-658,3] |
0,66 |
Примечание: БТШ — белок теплового шока, ИЛ-6 — интерлейкин-6, ИМТ — индекс массы тела, квБТШ — кардиоваскулярный белок теплового шока, ММП — матриксная металлопротеиназа, ОДСНсФВ — острая декомпенсация сердечной недостаточности с сохраненной фракцией выброса, ТИМП-1 — тканевый ингибитор металлопротеиназы-1, Me [Q25-Q75]) — медиана [интерквартильный размах], NT-proBNP — N-концевой промозговой натрийуретический пептид.
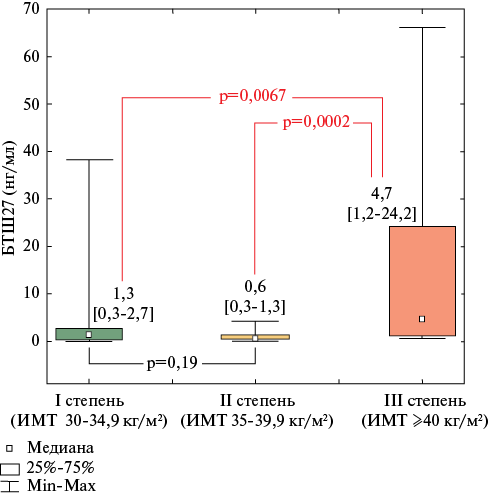
Рис. 1 Сравнительный анализ концентраций БТШ27 в зависимости от степени ожирения.
Примечание: БТШ — белок теплового шока, ИМТ — индекс массы тела.
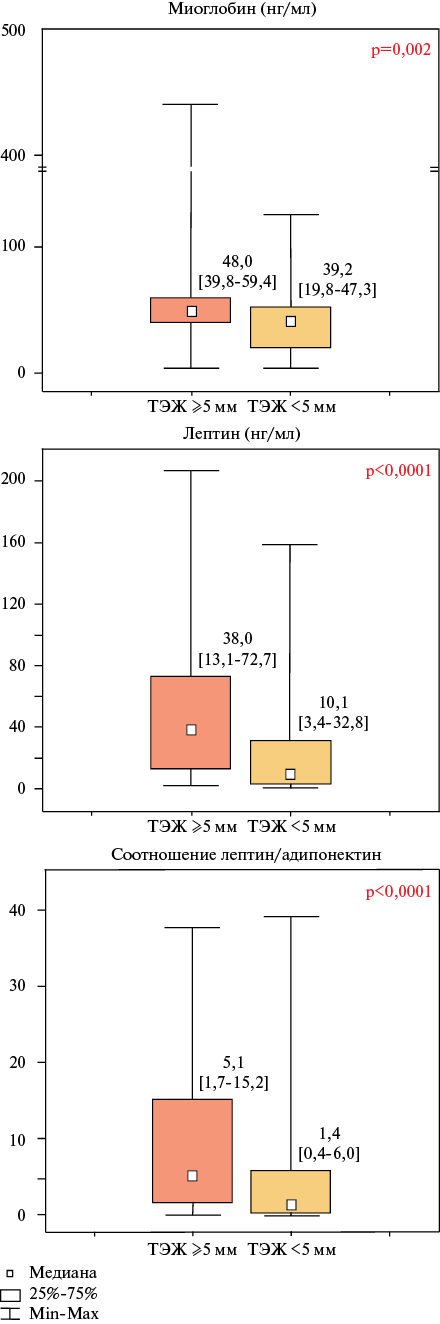
Рис. 2 Cывороточные концентрации миоглобина, лептина и соотношения лептин/адипонектин в зависимости от ТЭЖ у больных с ОДСНсФВ.
Примечание: ТЭЖ — толщина эпикардиального жира.
Обсуждение
Анализ БТШ у пациентов с ожирением и ОДСНсФВ, выполненный в настоящем исследовании, продемонстрировал статистически значимо более низкий уровень БТШ70 у этих больных относительно лиц без ожирения. Согласно имеющимся в литературе данным, роль высокомолекулярных шаперонов, к которым относится БТШ70, при ожирении достаточно неоднозначна: описаны как их гиперсекреция на фоне ожирения, как следствие декомпенсации развивающегося клеточного стресса, так и снижение их концентрации, которое может быть связано с ослаблением эффективности механизмов ответа на клеточный стресс (heat shock response) у больных с ожирением [15][18][19].
Полученные в настоящем исследовании данные о статистически значимо более высоких концентрациях низкомолекулярного, так называемого "малого" БТШ27, у больных ОДСНсФВ с морбидным ожирением согласуются с результатами исследований других авторов, согласно которым гиперсекреция данного шаперона является фактором, связанным с выраженностью ожирения и неблагоприятным течением ХСН [14][20].
В настоящем исследовании получены данные о статистически значимых более высоких концентрациях лептина и миоглобина у больных с гипертрофией ЭЖТ. Как описано в литературе, гипертрофированная ЭЖТ не только оказывает прямое механическое воздействие на миокард, но и способствует его ремоделированию за счет высвобождения медиаторов воспаления; одним из таких медиаторов является лептин, избыточная секреция которого как раз характерна для гипертрофированных адипоцитов [8][21]. В свою очередь, повышение уровней миоглобина у пациентов с ОДСНсФВ и гипертрофией ЭЖТ может свидетельствовать о предрасположенности таких пациентов к процессам, связанным с поражением миокарда.
В настоящем исследовании не было получено статистически значимых различий в уровнях ММП2, ММП9 и ТИМП-1 в зависимости от наличия и выраженности ожирения, а также ТЭЖ. В литературе представлены результаты изучения маркеров ремоделирования межклеточного матрикса и их связи с другими клиническими характеристиками больных ХСН с различной ФВ, главным образом, при компенсированном течении заболевания. Так, в исследовании, проведенном Kobusiak-Prokopowicz M, et al., анализировали уровни ММП2 и ТИМП-2 у больных ХСН и хронической болезнью почек, на фоне которой наблюдалось повышение концентраций изучаемых соединений [12]. В исследовании, проведенном отечественными авторами, были получены достоверные корреляции между концентрацией ТИМП-1 и эхокардиографическими признаками гипертрофии левого желудочка. В исследовании Pan W, et al. на выборке из 113 больных ХСН с различной ФВ было показано, что уровни ММП2 и ММП9 статистически значимо выше в плазме крови больных ХСН со сниженной ФВ, относительно больных с умеренно низкой и сохраненной ФВ [13]. В работе Wu CK, et al. на выборке из 77 пациентов с компенсированной ХСНсФВ была выявлена связь гиперсекреции NT-proBNP, ММП2, ТИМП-1 и галектина-3 с более выраженным миокардиальным фиброзом, оцененным по данным магнитно-резонансной томографии [22].
В современной отечественной и зарубежной литературе представлен ряд работ, посвященных изучению достаточно широкого спектра биохимических маркеров и их сочетаний у больных ХСН. Так, в исследовании, проведенном на китайской популяции больных ОДСНсФВ было показано, что ряд биохимических показателей, включая NT-proBNP, тропонин Т, фактор дифференцировки роста-15 (GDF-15), фактор некроза опухоли-альфа, биомаркер эндотелиальной дисфункции эндоглин, а также ММП2, ММП9 и ТИМП-1 были независимыми предикторами 2-летнего риска смерти от всех причин [11]. В работе Yu M, в качестве биохимического фактора, связанного с 30-дневной выживаемостью больных ОДСН различных фенотипов были проанализированы значения индекса атерогенности плазмы крови, рассчитанного как десятичный логарифм (log10) отношения уровня триглицеридов к уровню холестерина липопротеинов высокой плотности, при этом высокие уровни данного показателя были ассоциированы с менее благоприятным прогнозом [23]. В работе Нарусова О. Ю. и др. изучалась возможность использования пептида копептина в качестве прогностического маркера риска неблагоприятных исходов у пациентов с декомпенсацией СН III и IV функциональных классов (ФК), при этом концентрации копептина при поступлении >42,48 пмоль/л и при выписке >28,31 пмоль/л были ассоциированы с неблагоприятным прогнозом [24]. В исследовании Теплякова А. Т. и др. оценивали возможность использования ТИМП-1 в качестве маркера степени тяжести и риска неблагоприятных сердечно-сосудистых событий у пациентов с ОДСН с различной ФВ, при этом уровни ТИМП-1 статистически значимо ассоциировались с более высоким ФК ХСН: II ФК — 275,9 нг/мл, III ФК — 637,2 нг/мл и IV ФК — 1295,8 нг/мл [25].
Обращает на себя внимание, что, несмотря на важную роль, которую играет ожирение в патогенезе ХСН, в большинстве исследований, посвященных анализу биомаркеров при ОДСНсФВ, этот фактор и его связь с концентрацией биохимических показателей, практически не анализировались [26]. В настоящем сравнительном исследовании выявлены различия в концентрациях лептина, адипонектина и их соотношения у больных ОДСНсФВ в зависимости от наличия ожирения.
Ранее в ряде работ была описана гиперсекреция лептина и снижение концентрации адипонектина на фоне ожирения [9][10], однако применительно к ОДСНсФВ таких работ нет — похожие исследования адипоцитокинов проводились только при компенсированной ХСН. Так, в работе Faxen UL, et al. сравнивались уровни лептина и адипонектина у больных ХСН с сохраненной и сниженной ФВ, при этом уровень лептина у больных ХСН был повышен относительно группы контроля, однако различий между фенотипами заболевания выявлено не было. Показано, что концентрации лептина положительно коррелировали с ИМТ, тогда как концентрации адипонектина — отрицательно [27], что согласуется с результатами, полученными в настоящем исследовании. В работе Ramirez MF, et al. анализировалась взаимосвязь ассоциированных с ожирением биомаркеров (лептин, адипонектин, ИЛ-6) и толерантности к физической нагрузке у больных с компенсированной ХСНсФВ, при этом повышенные уровни лептина были связаны со снижением переносимости физической нагрузки [28].
Обобщая результаты настоящего исследования и данные мировой и отечественной литературы, можно предположить, что маркеры ремоделирования межклеточного матрикса являются факторами, потенциально ассоциированными с особенностями клинического течения ХСН, при этом не зависящими от выраженности ожирения. Данная закономерность вполне согласуется с современными представлениями о действии ММП [29], активация которых в большей степени ассоциирована с процессами нарушения протеостаза и регулируется сложной системой ингибиторов и транскрипционных факторов, напрямую не подверженных влиянию хронического воспаления, ассоциированного с ожирением.
Перспективы дальнейших исследований биохимических особенностей ОДСНсФВ при ожирении и без него включают более детальное исследование биомаркеров воспаления включая исследование концентраций белков инфламмасом и транспортируемых ими ИЛ, исследование циркулирующих уровней и активности ассоциированных с воспалением ферментов (нейтрофильная эластаза, ферменты группы каспаз), а также сравнительный анализ с другими группами больных, например, с компенсированной ХСНсФВ и другими фенотипами ХСН.
Ограничения исследования. Одним из ограничений исследования является относительно небольшой объем выборки, что не позволило с достаточной статистической мощностью провести анализ всех клинико-анамнестических факторов, способных оказать потенциальное влияние на концентрации исследуемых аналитов. Другим ограничением является постановка диагноза ожирения по ИМТ, поскольку у пациентов с ОДСНсФВ масса тела может быть увеличена за счет застойных явлений. Однако дополнительно проведенный сравнительный анализ концентраций биомаркеров в зависимости от толщины ЭЖТ позволяет частично преодолеть данное ограничение, поскольку определение этого показателя является одним из способов оценки выраженности висцерального ожирения.
Заключение
Ожирение у больных с ОДСНсФВ ассоциировано с изменениями концентраций основных показателей адипоцитокинового комплекса, таких как лептин, адипонектин и их соотношение, при этом данные факторы также зависят от степени гипертрофии ЭЖТ. Биомаркеры клеточного стресса — БТШ — на фоне ожирения показали разнонаправленные тенденции, БТШ27 имел более высокие уровни при морбидном ожирении, тогда как более высокая секреция БТШ70 наблюдалась у больных ОДСНсФВ без ожирения. Таким образом, исследованный в работе биохимический профиль больных ОДСНсФВ характеризуется рядом особенностей, связанных с ожирением, что может свидетельствовать о его вовлеченности в патогенез ХСН и патофизиологические процессы, происходящие при декомпенсации данного заболевания.
Отношения и деятельность. Исследование проводилось в рамках государственного задания "Разработка информационно-аналитической системы для прогнозирования и улучшения исходов путем оптимизации подходов к ведению пациентов с декомпенсированной сердечной недостаточностью с сохраненной фракцией выброса с использованием мультимаркерной стратегии и методов искусственного интеллекта" (2025-2027гг, регистрационный номер И125011901994-4).
Список литературы
1. Поляков Д. С., Фомин И. В., Беленков Ю. Н. и др. Хроническая сердечная недостаточность в Российской Федерации: что изменилось за 20 лет наблюдения? Результаты исследования ЭПОХА-ХСН. Кардиология. 2021;61(4):4-14. doi:10.18087/cardio.2021.4.n1628.
2. Виноградова Н. Г., Поляков Д. С., Фомин И. В. Анализ смертности у пациентов с ХСН после декомпенсации при длительном наблюдении в условиях специализированной медицинской помощи и в реальной клинической практике. Кардиология. 2020; 60(4):91-100. doi:10.18087/cardio.2020.4.n1014.
3. Cho D, Yoo B. Current Prevalence, Incidence, and Outcomes of Heart Failure with Preserved Ejection Fraction. Heart Fail Clin. 2021;17(3):315-26. doi:10.1016/j.hfc.2021.03.002.
4. Powell Wiley T, Ngwa J, Kebede S, et al. Impact of Body Mass Index on Heart Failure by Race/Ethnicity From the Get With The Guidelines — Heart Failure (GWTG–HF) Registry. JACC Heart Fail. 2018;6(3):233-42. doi:10.1016/j.jchf.2017.11.011.
5. Фомин И. В. Хроническая сердечная недостаточность в российской Федерации: что сегодня мы знаем и что должны делать. Российский кардиологический журнал. 2016;(8):7-13. doi:10.15829/1560-4071-2016-8-7-13.
6. Ларина В. Н., Ойноткинова О. Ш., Ларин В. Г. и др. Сердечная недостаточность с сохраненной фракцией выброса левого желудочка: комплексный фенотип-ориентированный подход к диагностике и коррекции. Кардиология и сердечнососудистая хирургия. 2022;15(6): 627-36. doi:10.17116/kardio202215061627.
7. Сафиуллина А. А., Ускач Т. М., Сайпудинова К. М., Терещенко С. Н., Чазова И. Е. Сердечная недостаточность и ожирение. Терапевтический архив. 2022;94(9):1115-21. doi:10.26442/00403660.2022.09.201837.
8. Джиоева О. Н., Тимофеев Ю. С., Метельская В. А. и др. Роль эпикардиальной жировой ткани в патогенезе хронического воспаления при сердечной недостаточности с сохраненной фракцией выброса. Кардиоваскулярная терапия и профилактика. 2024;23(3):3928. doi:10.15829/1728-8800-2024-3928.
9. Paillaud E, Poisson J, Granier C, et al. Serum Leptin Levels, Nutritional Status, and the Risk of Healthcare-Associated Infections in Hospitalized Older Adults. Nutrients. 2022;14(1):226. doi:10.3390/nu14010226.
10. Kurose S, Onishi K, Takao N, et al. Association of serum adiponectin and myostatin levels with skeletal muscle in patients with obesity: A cross-sectional study. PLoS One. 2021;16(1): e0245678. doi:10.1371/journal.pone.0245678.
11. Gao Y, Bai X, Lu J, et al. Prognostic Value of Multiple Circulating Biomarkers for 2-Year Death in Acute Heart Failure With Preserved Ejection Fraction. Front Cardiovasc Med. 2021; 8:779282. doi:10.3389/fcvm.2021.779282.
12. Kobusiak-Prokopowicz M, Krzysztofik J, Kaaz K, et al. MMP-2 and TIMP-2 in Patients with Heart Failure and Chronic Kidney Disease. Open Med (Wars). 2018;13:237-46. doi:10.1515/med-2018-0037.
13. Pan W, Yang D, Yu P, Yu H. Comparison of predictive value of NTproBNP, sST2 and MMPs in heart failure patients with different ejection fractions. BMC Cardiovasc Disord. 2020;20(1):208. doi:10.1186/s12872-020-01493-2.
14. Traxler D, Lainscak M, Simader E, et al. Heat shock protein 27 acts as a predictor of prognosis in chronic heart failure patients. Clin Chim Acta. 2017;473:127-32. doi:10.1016/j.cca.2017.08.028.
15. De Lemos Muller CH, Schroeder HT, Rodrigues-Krause J, Krause M. Extra and intra cellular HSP70 levels in adults with and without metabolic disorders: A systematic review and metaanalysis. Cell Stress Chaperones. 2023;28(6):761-71. doi:10.1007/s12192-023-01368-3.
16. McDonagh T, Metra M. 2021 Рекомендации ESC по диагностике и лечению острой и хронической сердечной недостаточности. Российский кардиологический журнал. 2023;28(1):5168. doi:10.10.15829/1560-4071-2023-5168.
17. Хроническая сердечная недостаточность. Клинические рекомендации 2020. Российский кардиологический журнал. 2020;25(11):4083. doi:10.15829/1560-4071-2020-4083.
18. Драпкина О. М., Ашихмин Я. И., Ивашкин В.Т. Роль шаперонов в патогенезе сердечно-сосудистых заболеваний и кардиопротекции. Российские медицинские вести. 2008;13(1):56-69.
19. Tutor AW, Lavie CJ, Kachur S, et al. Updates on obesity and the obesity paradox in cardiovascular diseases. Prog Cardiovasc Dis. 2023;78:2-10. doi:10.1016/j.pcad.2022.11.013.
20. Tavallaie S, Rahsepar AA, Abdi H, et al. Association between indices of body mass and antibody titers to heat-shock protein-27 in healthy subjects. Clin Biochem. 2012;45(1-2):144-7. doi:10.1016/j.clinbiochem.2011.09.022.
21. Pugliese NR, Paneni F, Mazzola M, et al. Impact of epicardial adipose tissue on cardiovascular haemodynamics, metabolic profile, and prognosis in heart failure. Eur J Heart Fail. 2021;23:1858-71. doi:10.1002/ejhf.2337.
22. Wu CK, Su MM, Wu YF, et al. Combination of Plasma Biomarkers and Clinical Data for the Detection of Myocardial Fibrosis or Aggravation of Heart Failure Symptoms in Heart Failure with Preserved Ejection Fraction Patients. J Clin Med. 2018;7(11):427. doi:10.3390/jcm7110427.
23. Yu M, Yang H, Kuang M, et al. Atherogenic index of plasma: a new indicator for assessing the short-term mortality of patients with acute decompensated heart failure. Front Endocrinol (Lausanne). 2024;15:1393644. doi:10.3389/fendo.2024.1393644.
24. Нарусов О. Ю, Скворцов А. А., Протасов В. Н. и др. Прогностическое значение копептина у больных с декомпенсацией сердечной недостаточности. Кардиологический вестник. 2017;12(3):30-8.
25. Тепляков А. Т., Гракова Е.В., Калюжин В.В. и др. Новые возможности в диагностике декомпенсированной сердечной недостаточности: клиническое значение факторов роста VEGF, PDGF-AB, FGF basic, тканевого ингибитора матриксных металлопротеиназ 1 и липопротеин-ассоциированной фосфолипазы А2. Сибирский журнал клинической и экспериментальной медицины. 2015;30(2):50-60.
26. Obokata M, Reddy YNV, Pislaru SV, et al. Evidence supporting the existence of a distinct obese phenotype of heart failure with preserved ejection fraction. Circulation. 2017;136:6-19. doi:10.1161/CIRCULATIONAHA.116.026807.
27. Faxén UL, Hage C, Andreasson A, et al. HFpEF and HFrEF exhibit different phenotypes as assessed by leptin and adiponectin. Int J Cardiol. 2017;228:709-16. doi:10.1016/j.ijcard.2016.11.194.
28. Ramirez MF, Lau ES, Parekh JK, et al. Obesity-Related Biomarkers Are Associated With Exercise Intolerance and HFpEF. Circ Heart Fail. 2023;16(11):e010618. doi:10.1161/CIRCHEARTFAILURE.123.010618.
29. de Almeida LGN, Thode H, Eslambolchi Y, et al. Matrix Metalloproteinases: From Molecular Mechanisms to Physiology, Pathophysiology, and Pharmacology. Pharmacol Rev. 2022;74(3): 712-68. doi:10.1124/pharmrev.121.000349.
Об авторах
Ю. С. ТимофеевРоссия
Юрий Сергеевич Тимофеев — к.м.н., с.н.с., руководитель лаборатории изучения биохимических маркеров риска хронических неинфекционных заболеваний им. Н. В. Перовой отдела фундаментальных и прикладных аспектов ожирения.
Москва
В. А. Метельская
Россия
Виктоиия Алексеввна Метельская — д.б.н., профессор, г.н.с..
Москва
А. А. Иванова
Россия
Анна Александровна Иванова — м.н.с.
Москва
Н. И. Дубовская
Россия
Наталия Игоревна Дубовская — лаборант-исследователь.
Москва
Ел. А. Рогожкина
Россия
Елизавета Александровна Рогожкина — м.н.с.
Москва
Т. Ю. Веденикин
Россия
Тимофей Юрьевич Веденикин — зав. отделением анестезиологии-реанимации № 03 для лечения больных кардиологического профиля.
Москва
Р. А. Замятин
Россия
Роман Александрович Замятин — аспирант.
Москва
А. Л. Борисова
Россия
Анна Львовна Борисова — н.с., руководитель лаборатории.
Москва
О. Н. Джиоева
Россия
Ольга Николаевна Джиоева — д.м.н., в.н.с., руководитель лаборатории.
Москва
О. М. Драпкина
Россия
Оксана Михайловна Драпкина — д.м.н., профессор, академик РАН, директор.
Москва
Дополнительные файлы
Что известно о предмете исследования?
- Острая декомпенсация сердечной недостаточности с сохраненной фракцией выброса (ОДСНсФВ) является тяжелым жизнеугрожающим состоянием, для которого характерна высокая частота госпитализаций и риск летальных исходов, при этом ожирение рассматривается как один из важнейших факторов риска развития заболевания и связано с тяжестью его течения.
- В литературе описан ряд биохимических маркеров, которые применяются для оценки ключевых патофизиологических и молекулярно-биологических процессов, характерных для сердечной недостаточности и ожирения: белков теплового шока (БТШ), адипоцитокинов, матриксных металлопротеиназ, однако особенности их секреции у больных ОДСНсФВ с различным индексом массы тела остаются недостаточно изученными.
Что добавляют результаты исследования?
- Впервые одномоментно исследован комплекс кардиомаркеров, адипоцитокинов, БТШ и биомаркеров ремоделирования межклеточного матрикса у пациентов с ОДСНсФВ в зависимости от индекса массы тела, степени ожирения, толщины эпикардиальной жировой ткани.
- Показано, что пациенты с ОДСНсФВ и ожирением имеют более низкие уровни БТШ70 и адипонектина и более высокие уровни лептина и соотношения лептин/адипонектин, а гиперсекреция БТШ27 характерна для морбидного ожирения. Более высокие уровни миоглобина и лептина при ОДСНСсФВ связаны с гипертрофией эпикардиальной жировой ткани.
Рецензия
Для цитирования:
Тимофеев Ю.С., Метельская В.А., Иванова А.А., Дубовская Н.И., Рогожкина Е.А., Веденикин Т.Ю., Замятин Р.А., Борисова А.Л., Джиоева О.Н., Драпкина О.М. Биохимический профиль сыворотки крови пациентов с декомпенсированной сердечной недостаточностью с сохраненной фракцией выброса в зависимости от наличия ожирения. Кардиоваскулярная терапия и профилактика. 2025;24(7):4453. https://doi.org/10.15829/1728-8800-2025-4453. EDN: TEWGYU
For citation:
Timofeev Yu.S., Metelskaya V.A., Ivanova A.A., Dubovskaya N.I., Rogozhkina E.A., Vedenikin T.Yu., Zamyatin R.A., Borisova A.L., Dzhioeva O.N., Drapkina O.M. Serum biochemical profile in patients with decompensated heart failure with preserved ejection fraction depending on obesity. Cardiovascular Therapy and Prevention. 2025;24(7):4453. (In Russ.) https://doi.org/10.15829/1728-8800-2025-4453. EDN: TEWGYU























































