Перейти к:
Субклинические депрессия и тревога как дополнительный фактор риска сердечно-сосудистых осложнений у больных с низким и умеренным риском (по данным десятилетнего наблюдения)
https://doi.org/10.15829/1728-8800-2021-2762
Аннотация
Цель. Оценить вклад тревоги (Anxiety, А) и депрессии (Depression, D) в повышение риска развития сердечно-сосудистых осложнений (ССО) у пациентов с риском по SCORE (Systematic Coronary Risk Evaluation) <5% по данным 10-летнего наблюдения.
Материал и методы. В работу включено 190 больных с риском по SCORE <5%, обследованных в 2009-2010гг. Помимо стандартного обследования проводилось анкетирование по госпитальной шкале HADS (Hospital Anxiety and Depression Scale) для оценки А и D. В 2019г проведен телефонный обзвон для выявления ССО за прошедшее время: смерть от сердечно-сосудистых заболеваний (ССС), острые инфаркты миокарда, нестабильная стенокардия, острые нарушения мозгового кровообращения, реваскуляризации. Отклик — 86,3%.
Результаты. ССО имели место у 17 (10,2%) пациентов и включали: 3 ССС, 6 случаев острого инфаркта миокарда, 4 случая нестабильной стенокардии, 12 реваскуляризаций. Перенесшие и не перенесшие ССО различались только по уровню D — 7 (5; 7) vs 5,0 (4; 5) баллов (р=0,0001). D >6 баллов повышала вероятность ССО — отношение шансов (ОШ) 2,9 (1,1-7,7). У лиц с D >6 и/или A >7 шанс ССО увеличивался — ОШ 4,9 (1,4-17,9). Сочетание нарушения двух и более параметров липидного спектра, систолическое артериальное давление >130 мм рт.ст. и D >6 и/или A >7 увеличивало риск ССО — ОШ 7,3 (2,48-21,36).
Заключение. Депрессия, в т.ч. субклиническая, ассоциируется с повышением риска ССО у больных с риском по SCORE <5%.
Для цитирования:
Смирнова М.Д., Свирида О.Н., Фофанова Т.В., Бланова З.Н., Яровая Е.Б., Агеев Ф.Т., Бойцов С.А. Субклинические депрессия и тревога как дополнительный фактор риска сердечно-сосудистых осложнений у больных с низким и умеренным риском (по данным десятилетнего наблюдения). Кардиоваскулярная терапия и профилактика. 2021;20(4):2762. https://doi.org/10.15829/1728-8800-2021-2762
For citation:
Smirnova M.D., Svirida O.N., Fofanova T.V., Blankova Z.N., Yarovaya E.B., Ageev F.T., Boytsov S.A. Subclinical depression and anxiety as an additional risk factor for cardiovascular events in low- and moderate-risk patients: data from 10-year follow-up. Cardiovascular Therapy and Prevention. 2021;20(4):2762. (In Russ.) https://doi.org/10.15829/1728-8800-2021-2762
Депрессия (Depression, D) и тревога (Anxiety, А) в настоящее время признаны независимыми факторами риска (ФР) развития и ухудшения прогноза сердечно-сосудистых заболеваний (ССЗ) [1-4]. Исследование INTERHEART [1], в котором были проанализированы данные больных из 52 стран мира, показало, что только психосоциальные факторы, включая A и D, были ответственны за 32,5% случаев острого инфаркта миокарда (ОИМ), причем эти факторы были так же важны, как курение и даже более значимы, чем артериальная гипертония (АГ) и сахарный диабет. Используемые в настоящее время системы стратификации риска, в т.ч. шкала SCORE (Systematic Coronary Risk Evaluation) — основной инструмент определения величины риска в странах Европы и России, опирающиеся на такие “классические” ФР, как возраст, пол, АГ, повышенный уровень холестерина (ХС), курение и т.п., не лишены такого существенного недостатка как недооценка истинной вероятности развития сердечно-сосудистых осложнений (ССО). В частности, шкала SCORE не учитывает психологический статус пациента. Особенно это актуально для пациентов с низким и умеренным риском, определяемым по критериям этой системы. Назрела необходимость создания эффективного и удобного для практического применения способа прогнозирования ССО у этой категории больных, позволяющего осуществить более персонализированный подход с учетом психологического статуса пациента, что позволит своевременно применять комплекс лечебно-профилактических мероприятий.
Цель исследования — оценить вклад A и D в повышение риска развития ССО у пациентов с риском по SCORE <5% по данным 10-летнего наблюдения.
Материал и методы
В исследовании использовалась база “Программы разработки новых методов и технологий профилактики, диагностики и лечения ССЗ, связанных с атеросклерозом, в лечебных учреждениях Западного административного округа (ЗАО) г. Москвы”, проходившего в 2009-2010гг на базе НИИ клинической кардиологии им. А.Л. Мясникова. Скрининг больных проводился участковыми терапевтами в 12 поликлиниках ЗАО г. Москвы с августа по декабрь 2009г. В исследование включали всех пациентов >35 лет, обратившихся к участковому терапевту в связи с любым заболеванием и подписавших информированное согласие на участие в исследовании. Критериями невключения были сердечная, печеночная, дыхательная недостаточность, хроническая болезнь почек 4-5 стадий, системные заболевания соединительной ткани, известные онкологические, психические, острые воспалительные и инфекционные заболевания. Всем больным перед включением в программу проводили стратификацию риска по шкале SCORE. В исследование включено 190 пациентов низкого/умеренного риска (SCORE <5%), которые помимо стандартного клинического обследования, проходили анкетирование по госпитальной шкале HADS (Hospital Anxiety and Depression Scale). Все больные были анкетированы с помощью опросника HADS по двум подшкалам: А и D. При интерпретации данных учитывался суммарный показатель по каждой подшкале, который расценивался как норма при сумме баллов от 0 до 7, субклинически выраженная тревога/депрессия A/D (сумма баллов 8-10) и клинически выраженная тревога/депрессия A/D (≥11 баллов).
В 2019-2020гг был проведен телефонный опрос пациентов с заполнением разработанного авторами вопросника, отражающего количество, характер и время возникновения ССО за прошедшее время: смерть от любых причин, смерть от ССЗ (ССС), фатальные и нефатальные ОИМ, нестабильная стенокардия, острые нарушения мозгового кровообращения (ОНМК), случаи реваскуляризации миокарда. Также рассматривалась комбинированная конечная точка (ССО = ССС + ОИМ + нестабильная стенокардия + ОНМК + реваскуляризация). Удалось получить данные 166 больных (отклик составил 86,3%): 37 мужчин и 129 женщин. 77 больных предоставили документацию, подтверждающую ССО (при очном обращении).
Статистический анализ. Проводили с помощью пакетов статистических программ Statistica 10 и SPSS 20. Непрерывные переменные, распределение которых было близко к нормальному, представлялись как среднее (M) ± стандартное отклонение (SD), при отличии распределения переменной от нормального приводились медиана (Mе) и 95% доверительный интервал (ДИ), максимальное и минимальное значения. Для проверки гипотез о средних в двух группах применялся t-критерий Стьюдента или его непараметрический аналог критерий Манна-Уитни. Зависимость признаков в таблице сопряженности 2×2 исследовалась с помощью двустороннего точного критерия Фишера. Для нахождения отрезной точки по исследуемым показателям применялся ROC-анализ. Отрезная точка соответствовала значению, для которого значения чувствительности и специфичности были максимально близки. Cравнение кривых выживаемости проводилось с помощью лог-рангового критерия. Отношение шансов (ОШ) и соответствующий 95% ДИ вычислялись с помощью модели бинарной логистической регрессии. Если ДИ не включал единицу, то ОШ считалось статистически значимым. Уровень значимости для проверки гипотез принимали равным 0,05.
Результаты
На момент включения в исследование средний возраст больных составлял 51,8±8,2 лет. Уровень офисного артериального давления (АД) на первом визите был для систолического (САД) 130,0 (128,2; 133,0) мм рт.ст. и диастолического (ДАД) 80,0 (81,1; 84,0) мм рт.ст., частота сердечных сокращений (ЧСС) 70,0 (69,5; 72,3) уд./мин. Уровень общего ХС был 6,07 (5,89; 6,29) ммоль/л, триглицеридов (ТГ) 1,36 (1,49; 1,79) ммоль/л, ХС липопротеинов низкой плотности (ХС ЛНП) 3,77 (3,61; 3,97) ммоль/л, ХС липопротеинов высокой плотности (ХС ЛВП) 1,37 (1,38; 1,51) ммоль/л, глюкозы 5,22 (5,27; 5,68) ммоль/л. Уровень А составил 7 (7; 8) баллов, D — 5 (5; 6) баллов. Доля больных без выраженных признаков A (0-7 баллов по шкале) — 53,7% (88 чел.), D (0-7 баллов) — 76,2% (125 чел.). Доля больных с клинически выраженной A (>11 баллов) — 10,4% (17 чел.), с клинически выраженной D (>11 баллов) — 3,6% (6 чел.). Уровни A и D были взаимосвязаны (r=0,504, p<0,0001).
За истекшие 10 лет ССО имели место у 17 (10,2%) пациентов, у которых произошли 3 ССС, 6 ОИМ, 4 случая нестабильной стенокардии, 12 транслюминальных баллонных ангиопластик коронарных артерий, 6 ОНМК. Ишемическая болезнь сердца (ИБС) была диагностирована у 11 пациентов — 10 случаев ОКС: ОИМ и нестабильная стенокардия, 1 случай диагностики стабильной стенокардии напряжения с проведением транслюминальной баллонной ангиопластики коронарных артерий. При сравнении исходных данных (таблица 1, рисунок 1) был установлено, что группы больных, перенесших CCО (ССО+) и не перенесших ССО (ССО-) различались только по уровню депрессии D — 7 (6; 8) vs 5,0 (5; 6) баллов (р=0,0001) (рисунок 1). Больные были сопоставимы по полу и возрасту. По показателям липидного профиля, уровням глюкозы, САД и ДАД, ЧСС, статусу курения, уровню А — 9 (7; 10) vs 7 (6; 8) баллов (р=0,12), различий также не выявлено.
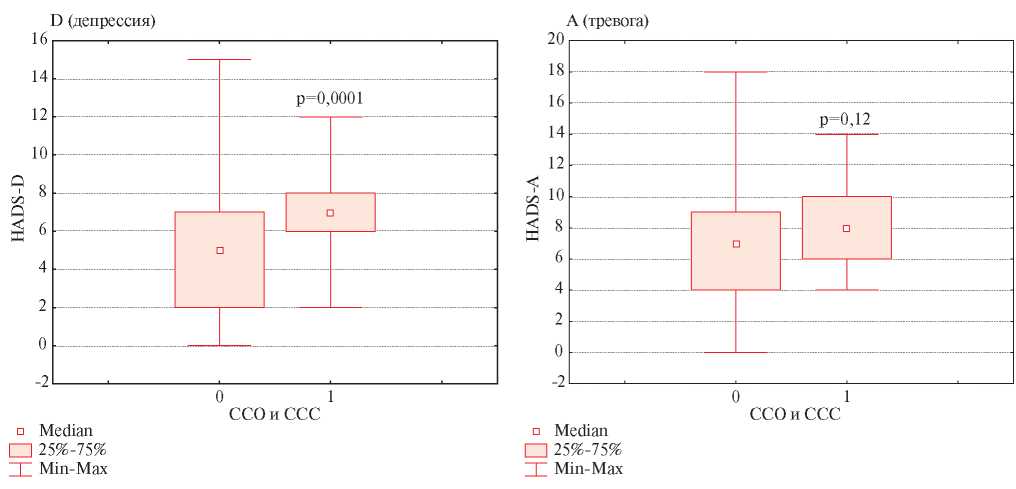
Рис. 1 Исходный психологический статус у пациентов, перенесших (ССО+) и не перенесших (ССО-) ССО + ССС по данным 10-летнего наблюдения.
Примечание: ССО — сердечно-сосудистые осложнения, ССС — смерть по сердечно-сосудистым причинам.
Таблица 1
Исходные клинические характеристики больных низкого/умеренного риска, перенесших (ССО+) и не перенесших (ССО-) ССО по данным 10-летнего наблюдения

Примечание: ДАД — диастолическое артериальное давление, ИМТ — индекс массы тела, ОТ — окружность талии, САД — систолическое артериальное давление, ССО — сердечно-сосудистые осложнения, ТГ — триглицериды, ХС — холестерин, ХС ЛВП — холестерин липопротеидов высокой плотности, ХС ЛНП — липопротеидов низкой плотности, ЧСС — частота сердечных осложнений.
У умерших по ССС пациентов уровень D исходно был выше, чем у выживших (рисунок 2). Несмотря на малое количество умерших, расхождение показателей было статистически значимым (р=0,04).
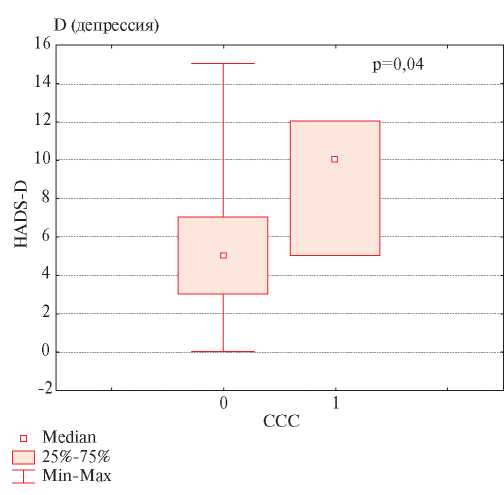
Рис. 2 Исходный уровень D (HADS — D) умерших по сердечно-сосудистым причинам (1) и выживших (0) пациентов.
По результатам ROC-анализа определена “отрезная точка” уровня D по шкале HADS, соответствующая 6 баллам. S под кривой =0,698, σ=0,050, 95% доверительный интервал (ДИ): 0,599-0,796, что является показателем хорошего качества исследуемой модели.
Уровень D по шкале HADS показал себя независимым предиктором развития ССО в модели, включающей возраст, пол, уровень АД и ХС. Уровень депрессии >6 баллов повышал вероятность ССО в 2,9 раз — отношение шансов (ОШ) 2,9; 95% ДИ: 1,1-7,7. Для А провести ROC-анализ не удалось из-за недостаточной мощности выборки, поэтому за отрезную точку взяли 7 баллов, что соответствует нижней границе суммарного значения баллов, расцениваемого как “субклиническая тревога”. По значениям уровней А (>7) и D (>6) был сформирован интегральный признак, объединяющий эти шкалы.
Для проведения анализа выживаемости пациенты были разделены на две группы. В первую включались те лица, у которых значения как A, так и D по шкале HADS не превышали отрезных значений, во вторую — все остальные. У лиц с D >6 и/или A >7 шанс возникновения ССО или ССС возрастает в ~5 раз по сравнению с пациентами с отсутствием психологических проблем — ОШ 4,9 (1,4-17,9). Причем кривые Каплана-Мейера, отражающие время, свободное от осложнений, начали расходиться уже через год наблюдения (р=0,008) (рисунок 3). Поправка на пол и возраст не проводилась в связи с тем, что сравниваемые группы по этим параметрам не различались.
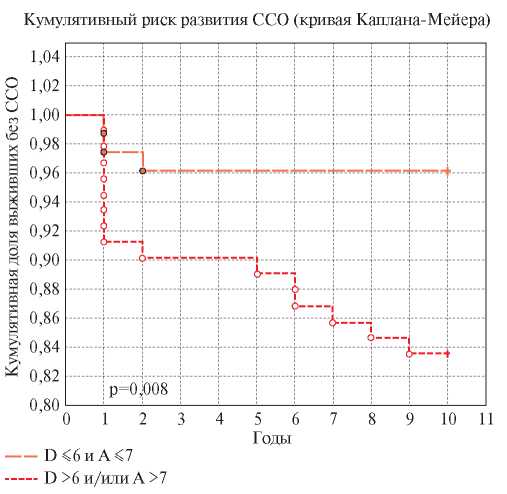
Рис. 3 Кумулятивный риск развития ССО в зависимости от их психологического статуса (кривая Каплана-Мейера).
Примечание: ССО — сердечно-сосудистые осложнения, A — Anxiety (тревога), D — Depression (депрессия).
С целью разработки алгоритма оценки вероятности развития ССО у больных низкого/умеренного риска провели многофакторный анализ предикторов развития ССО у больных с риском по SCORE <5% (рисунок 4). Как показал анализ, нарушение у таких пациентов двух и более параметров липидного спектра (ХС ЛНП >3,0 ммоль/л и ХС ЛВП <0,9 ммоль/л, ТГ >1,5 ммоль/л) увеличивало 10-летний риск ССО на 36%, однако изменения не достигли статистически значимости. При выявлении на приеме у этого пациента САД, соответствующего критериям “высоконормального” или повышенного АД (САД >130 мм рт.ст.), риск ССО увеличивается уже достоверно, на 89%. У пациентов с нарушением двух и более параметров липидного спектра, САД >130 мм рт.ст. и наличием D и/или A, даже субклинических (отрезные значения приведены выше) вероятность развития ССО (включая ССС) увеличивается в более чем в 7 раз — ОШ 7,28 (95% ДИ: 2,48-21,36).
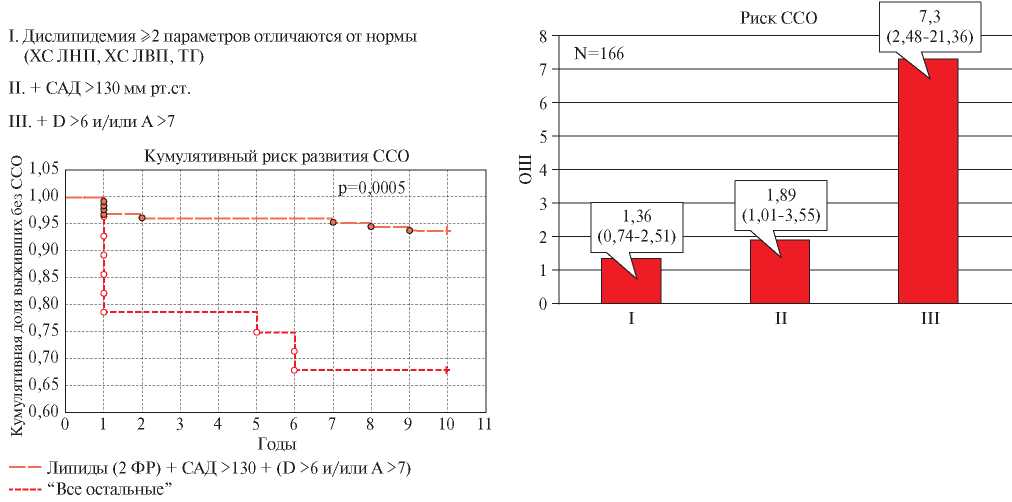
Рис. 4 Алгоритм стратификации риска развития ССО у больных с риском по SCORE <5%.
Примечание: ОШ — отношение шансов, САД — систолическое артериальное давление, ССО — сердечно-сосудистые осложнения, ТГ — триглицериды, ФР — факторы риска, ХС ЛВП — холестерин липопротеидов высокой плотности, ХС ЛНП — липопротеидов низкой плотности, A — Anxiety (тревога), D — Depression (депрессия).
Среди 19 больных, у которых отсутствовали все рассматриваемые в модели ФР, не было ни одного, перенесшего ССО за 10 лет наблюдения. В подгруппах пациентов с 1 или 2 ФР, ССО перенесли по 4 человека (8,3% и 7,2%, соответственно), в подгруппе пациентов со всеми 3 ФР — 9 (32,4%) человек (p=0,001).
Обсуждение
В ходе телефонных контактов удалось получить данные напрямую или, в случае смерти пациента, через их родственников у 166 пациентов, что составило 86% пациентов, проходивших анкетирование в 2009г. Число конечных точек за 10 лет наблюдения было, как и прогнозировалось, невелико. Тем не менее, те или иные ССО за 10 лет получили ~10% больных. Фатальные осложнения произошли у 1,8% (что соответствовало ожидаемым величинам), а ИБС впервые была диагностирована у 6,7% участников исследования. Небольшое количество конечных точек не позволило проанализировать предикторы каждой из них по отдельности. Однако мощности исследования хватило для анализа предикторов развития комбинированной конечной точки (ССО).
Когорта больных, включенных в исследование, была достаточно однородна по степени выраженности “классических” ФР, заведомо невысокой, что объясняет отсутствие их влияния на прогноз. В такой ситуации рельефно выделяется роль психологических факторов. Для их оценки была использована шкала HADS, разработанная Zigmond AS и Snaith RP еще в 1983г [5]. Это шкала представляется оптимальной для использования в условиях амбулаторного приема врачами общей практики, терапевтами, кардиологами в связи с ее краткостью, простотой и удобством как заполнения, так и интерпретации. В свое время она была создана, апробирована и рекомендована к использованию именно как экспрессскрининг уровня A и D в условиях общемедицинской практики, а не психиатрического приема [5].
При однофакторном анализе единственным фактором, из изученных авторами, влияющим на риск ССО, оказался уровень D по шкале HADS. Причем в настоящем исследовании речь идет именно о субклинической D, поскольку клинически выраженная D, т.е. на уровне диагноза, была только у 3,6% пациентов. Роль D как ФР ССО доказана целым рядом проспективных исследований различной продолжительности и мощности; причем длительность некоторых из них составляла ≥30 лет [2-4][6-8]. Выявление при включении в исследование признаков D ассоциировалось, независимо от “классических” ФР, с увеличением риска развития ИБС от 1,5 до 4,5 раз, причем эффект был “дозозависимым”: чем выше был уровень D, согласно используемым шкалам, тем выше был риск ИБС [6-8]. Влияние даже однократного депрессивного эпизода сохранялось >40 лет [4]. У мужчин среднего возраста симптомы D по шкале BDI (Beck Depression Inventory) увеличивали сердечно-сосудистый риск в 2,9 раз, по сравнению с расчетным по шкале SCORE и в 2,2 раза по сравнению с Фремингемской шкалой. Для женщин эти показатели были 1,4 и 1,3, соответственно [9].
В другом большом популяционном исследовании D по данным 10-летнего наблюдения увеличивала относительный риск смерти для мужчин 44-45 лет, как по всем причинам, так и ССС, на 52% (p<0,01). Вклад D был выше, чем вклад ожирения и дислипидемии, хотя и ниже, чем курения, АГ и сахарного диабета [10]. Интересно, что в настоящем исследовании уровень D оказывал влияние на 10-летний прогноз, несмотря на очень небольшую долю участников с клинически выраженной D. Отрезная точка оказалась даже немного ниже “официального” уровня субклинической D (6 баллов по сравнению с ≥7, как указывается в ключе к шкале). Тем важнее активно выявлять таких пациентов методом анкетирования. Не являясь пациентами психиатра, они, как выяснилось, требуют внимания кардиолога. В то же время, у одной из умерших больных D была 12 баллов (клинически выраженная), а медиана D у больных, перенесших ССС, оказалась равной 10,0 (рисунок 2).
Что касается A, то сведения о ее влиянии на возникновение и течение ССЗ весьма противоречивы. С одной стороны, по данным 7-летнего наблюдения, риск развития ОИМ был выше у пациентов не только c D (ОШ 1,39), но и с паническими атаками (ОШ 1,43), “неуточненными тревожными расстройствами” (ОШ 1,34), и посттравматическим расстройством (ОШ 1,25) без клинической симптоматики D. Модели были скорректированы с учетом различных ФР ОИМ и социально-демографических факторов [11]. В большом Швейцарском когортном исследовании (50 тыс. юношей призывного возраста) [12] наличие тревожной симптоматики повышало риск ИБС по данным почти 40-летнего наблюдения в >2 раза, а ОИМ в 2,5 раза, независимо от всех “классических” ФР. В других, таких же масштабных исследованиях, влияние A, выявленное при однофакторном анализе, нивелировалась при включении в модель “классических” ФР [11][13][14]. Мало того, в некоторых работах, вопреки ожиданию, влияние А оказалось позитивным. Так, в проспективном когортном исследовании с участием ~5 тыс. пациентов было продемонстрировано снижение общей смертности у тревожных пациентов на 23% в общей группе и на 26% в подгруппе больных ИБС за 5 лет наблюдения [15]. По данным еще одного исследования [16] текущее тревожное расстройство снижало 10-летний риск ССС — ОШ 0,58 (95% ДИ: 0,38-0,90), у больных очень высокого сердечно-сосудистого риска, тогда как D ожидаемо увеличивала его на 57%. Эти парадоксальные результаты, можно объяснить более ранней и частой обращаемостью к врачам и большей приверженностью терапии больных с тревожными расстройствами [17]. В настоящем исследовании A не оказывала самостоятельного влияния на прогноз, но усугубляла влияние D. Пациенты, не имеющие ни субклинической A, ни субклинической D, т.е. пациенты с благоприятным психологическим статусом, имели риск ССО и ССС в ~5 раз ниже, чем лица с такими психологическими проблемами.
Сочетание “классических” и “новых” ФР демонстрирует кумулятивный эффект в плане повышения вероятности ССО у больных с риском ССС по SCORE <5%. Такой комплексный подход представляется наиболее перспективным. В недавно опубликованном исследовании [18] описана попытка “перекалибровки” шкалы SCORE для восточноевропейских стран с добавлением семи поведенческих и психосоциальных ФР: образования, занятости, семейного положения, D, индекса массы тела, физической активности и использования антигипертензивных препаратов. Это модель позволила улучшить прогнозирование ССС, при этом преимущества реклассификации были наибольшими у участников с промежуточным риском, который, как выяснилось, исходно недооценивался. Однако использование столь большого числа факторов, может затруднить работу врача первичного звена, к которому, прежде всего, и обращаются такие пациенты.
Cочетание таких “классических” ФР, как дислипидемия и повышение САД с субклиническими A и/или D увеличивает риск у таких больных более чем в 7 раз. Под дислипидемией в представленной модели подразумевают нарушения не одного, а двух и более параметров, пусть и не очень выраженных. Необходимо подчеркнуть, что речь идет о “высоконормальном” АД: значимо уже повышение его уровня >130 мм рт.ст. Таким образом, для вычленения из общей популяции больных с более высоким индивидуальным риском предлагается использовать только 2 дополнительных фактора: A и D, уровень которых определяется при заполнении простейшей анкеты.
Ограничения исследования. Исследование имело несколько ограничений. Прежде всего, это небольшое количество больных. Согласно протоколу “Программы разработки новых методов и технологий профилактики, диагностики и лечения ССЗ, связанных с атеросклерозом, в лечебных учреждениях ЗАО г. Москвы”, в субисследовании с анкетированием HADS участвовало не более четверти больных. В дальнейшем планируем провести более масштабное исследование, направленное на оценку влияния именно психологических факторов на прогноз больных низкого/умеренного риска ССО. Второе, в рамках настоящего исследования невозможно было оценить наличие и характер терапии, получаемой пациентами.
Заключение
По данным 10-летнего наблюдения ССО наблюдаются у 10,2% пациентов с исходно низким или умеренным риском ССС (SCORE <5%). Для своевременного выявления таких больных следует одновременно учитывать не только “классические”, но и “новые” ФР, которые демонстрирует кумулятивный эффект в плане повышения вероятности развития ССО. Сочетание таких “классических” ФР, как дислипидемии и повышение САД >130 мм рт.ст., с “новыми” ФР: D, даже субклинической, и/или A, увеличивало риск развития ССО у больных в 7,3 раза. Таким образом, новый подход к выявлению больных с более высоким риском ССО, чем это считалось ранее, включающий использование комбинации простых и недорогих методов (определение липидного профиля крови, измерение АД и заполнение опросника HADS) позволит точнее выявлять ту когорту больных, которые нуждаются в более тщательном наблюдении и, возможно, лечении. Однако для подтверждения значимости выявленных ассоциаций требуется проведение более масштабных исследований.
Список литературы
1. Yusuf S, Hawken S, Ounpu S, et al. on behalf of the INTERHEART Study Investigators. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART Study): case-control study. Lancet. 2004;364(9438):937-52. doi:10.1016/S0140-6736(04)17018-9.
2. Погосова Г. В. Депрессия — фактор риска развития ИБС. Кардиология. 2012;12:4-11.
3. Ariyo AA, Haan M, Tangen CM, et al. Depressive symptoms and risks of coronary heart disease and mortality in elderly Americans Cardiovascular Health Study Collaborative Research Group. Circulation. 2000;102:1773-9. doi:10.1161/01.CIR.102.15.1773.
4. Ford DE, Mead LA, Chang PP, et al. Depression predicts cardiovascular disease in men: the Precursors Study. Arch Intern Med. 1998;158(13):1422-6. doi:10.1001/archinte.158.13.1422.
5. Zigmond AS, Snaith RP. The hospital anxiety anddepression scale. Acta Psychiatr Scand. 1983;67(6):361-70. doi:10.1111/j.1600-0447.1983.tb09716.
6. Ferketich AK, Schwartzbaum JA, Frid DJ, Moeschberger ML. Depression as an antecedent to heart disease among women and men in the NHANES I study. National Health and Nutrition Examination Survey. Arch Intern Med. 2000;160:1261-8. doi:10.2165/00023210-200216020-00004.
7. Brown JM, Stewart JC, Stump TE, et al. Risk of Coronary Heart Disease Events Over 15 Years among Older Adults with Depressive Symptoms. Am J Geriatr Psychiatry. 2011;19:721-9. doi:10.1097/JGP.0b013e3181faee19.
8. Ahto M, Isoaho R, Puolijoki H, et al. Stronger symptoms of depression predict high coronary heart disease mortality in older men and women. Int J Geriatr Psychiatry. 2007;22:757-63. doi:10.1002/gps.1735.
9. Koponen H, Jokelainen J, Keinänen-Kiukaanniemi S, Vanhala M. Depressive symptoms and 10-year risk for cardiovascular morbidity and mortality. World J Biol Psychiatry. 2010;11(6):834-9. doi:10.3109/15622975.2010.486842.
10. Ladwig KH, Baumert J, Marten-Mittag B, et al. for the KORA Investigators. Room for depressed and exhausted mood as a risk predictor for allcause and cardiovascular mortality beyond the contribution of the classical somatic risk factors in men. Atherosclerosis. 2017;257:224-31. doi:10.1016/j.atherosclerosis.2016.12.003.
11. Scherrer JF, Chrusciel T, Angelique Zeringue A, et al. Anxiety Disorders Increase Risk for Incident Myocardial Infarction in Depressed and Nondepressed Veterans Administration Patients. Am Heart J. 2010;159:772-9. doi:10.1016/j.ahj.2010.02.033.
12. Janszky I, Ahnve S, Lundberg I, et al. Early-onset depression, anxiety and risk of subsequent coronary heart disease. 37-year follow-up of 49,321 young Swedish men. J Am Coll Cardiol. 2010;56:31-7. doi:10.1016/j.jacc.2010.03.034.
13. Albert CM, Chae CU, Rexrode KM, et al. Phobic anxiety and risk of coronary heart disease and sudden cardiac death among women. Circulation. 2005;111:480. doi:10.1161/01.CIR.0000153813.64165.5D.
14. Kawachi I, Colditz GA, Ascherio A, et al. Prospective study of phobic anxiety and risk of coronary heart disease in men. Circulation 1994;89:1992-7. doi:10.1161/01.cir.89.5.1992.
15. Meyer T, Buss U, Herrmann-Lingen C. Role of cardiac disease severity in the predictive value of anxiety for allcause mortality. Psychosom Med. 2010;72:9-15. doi:10.1097/PSY.0b013e3181c64fc0.
16. Ivanovs R, Kivite A, Ziedonis D, et al. Association of Depression and Anxiety With the 10-Year Risk of Cardiovascular Mortality in a Primary Care Population of Latvia Using the SCORE System. Front Psychiatry. 2018;9:276. doi:10.3389/fpsyt.2018.00276.
17. Агеев Ф. Т., Фофанова Т. В., Деев А. Д. Применение фелодипина в амбулаторной практике: оценка клинической эффективности и приверженности к лечению у больных с артериальной гипертонией. Кардиология. 2009:1(49):30-3.
18. Tillmann T, Läll K, Dukes O, Veronesi G, et al. Development and validation of two SCORE - based cardiovascular risk predictionmodels for Eastern Europe: amulticohort study. Eur Heart J. 2020;41:3325-33. doi:10.1093/eurheartj/ehaa571.
Об авторах
М. Д. СмирноваРоссия
Мария Дмитриевна Смирнова — доктор медицинских наук, старший научный сотрудник отдела амбулаторных лечебно-диагностических технологий.
Москва, Тел.: +7 (926) 165-11-39
О. Н. Свирида
Россия
Ольга Николаевна Свирида — кандидат медицинских наук, младший научный сотрудник отдела амбулаторных лечебно-диагностических технологий.
Москва
Т. В. Фофанова
Россия
Татьяна Вениаминовна Фофанова — доктор медицинских наук, старший научный сотрудник отдела амбулаторных лечебно-диагностических технологий.
Москва
З. Н. Бланова
Россия
Зоя Николаевна Бланова — кандидат медицинских наук, н.с. отдела амбулаторных лечебно-диагностических технологий.
Москва
Е. Б. Яровая
Россия
Елена Борисовна Яровая — доктор медицинских наук, профессор кафедры теории вероятностей механико-математического факультета, отделение математики.
Москва
Ф. Т. Агеев
Россия
Фаиль Таипович Агеев — профессор, доктор медицинских наук, руководитель отдела амбулаторных лечебно-диагностических технологий.
Москва
С. А. Бойцов
Россия
Сергей Анатольевич Бойцов — доктор медицинских наук, профессор, член-корр. РАН, генеральный директор.
Москва
Дополнительные файлы
Рецензия
Для цитирования:
Смирнова М.Д., Свирида О.Н., Фофанова Т.В., Бланова З.Н., Яровая Е.Б., Агеев Ф.Т., Бойцов С.А. Субклинические депрессия и тревога как дополнительный фактор риска сердечно-сосудистых осложнений у больных с низким и умеренным риском (по данным десятилетнего наблюдения). Кардиоваскулярная терапия и профилактика. 2021;20(4):2762. https://doi.org/10.15829/1728-8800-2021-2762
For citation:
Smirnova M.D., Svirida O.N., Fofanova T.V., Blankova Z.N., Yarovaya E.B., Ageev F.T., Boytsov S.A. Subclinical depression and anxiety as an additional risk factor for cardiovascular events in low- and moderate-risk patients: data from 10-year follow-up. Cardiovascular Therapy and Prevention. 2021;20(4):2762. (In Russ.) https://doi.org/10.15829/1728-8800-2021-2762
JATS XML

























































