Перейти к:
Пятилетний результат имплантации биодеградируемых стентов Absorb по методике бифуркационного стентирования
https://doi.org/10.15829/1728-8800-2021-2864
Аннотация
В представленном клиническом наблюдении описывается пятилетний результат бифуркационного стентирования передней межжелудочковой ветви и крупной диагональной ветви стентами BVS (bioabsorbable vascular stent) Absorb по данным селективной коронарографии и оптической когерентной томографии. На примере видна не только успешная имплантация биодеградируемых стентов в область бифуркации, но и полное восстановление сосудистой стенки артерии с формированием неокарины. С помощью оптической когерентной томографии удалось детально изучить все этапы изменения сосудистой стенки артерии изнутри. Данное клиническое наблюдение заставляет по-новому взглянуть на биодеградируемые стенты BVS Absorb и не исключает возможности возвращения этих видов стентов в клиническую практику в будущем. В настоящее время производство и использование биодеградируемых стентов BVS Absorb приостановлено, однако они заняли определенную нишу в эндоваскулярном лечении пациентов с ишемической болезнью сердца.
Ключевые слова
Для цитирования:
Иоселиани Д.Г., Асадов Д.А., Фоменко В.В., Азаров А.В., Семитко С.П. Пятилетний результат имплантации биодеградируемых стентов Absorb по методике бифуркационного стентирования. Кардиоваскулярная терапия и профилактика. 2021;20(4):2864. https://doi.org/10.15829/1728-8800-2021-2864
For citation:
Ioseliani D.G., Asadov D.A., Fomenko V.V., Azarov A.V., Semitko S.P. Five-year outcomes of implantation of Absorb biodegradable stents using the bifurcation stenting technique: a case report. Cardiovascular Therapy and Prevention. 2021;20(4):2864. (In Russ.) https://doi.org/10.15829/1728-8800-2021-2864
Стентирование коронарных артерий (КА), наряду с хирургическими методами реваскуляризации миокарда, заняло лидирующее положение в лечении ишемической болезни сердца. Главными осложнениями стентирования в отдаленные сроки остается развитие in-stent стеноза и тромбоза стента. Причин этих нежелательных явлений стентирования несколько, но главными являются чрезмерная пролиферация неоинтимальной ткани, обусловленная воспалительной реакцией в ответ на внедрение “инородного” тела, и низкая биосовместимость импланта с интимой сосуда [1].
Широкое использование в клинической практике стентов с лекарственным покрытием существенно снизило частоту нежелательных результатов, но полностью решить проблему не удалось. Это послужило основанием для разработки так называемых биосовместимых стентов, состоящих из материалов, максимально совместимых с тканями пациентов [2]. К тому же, выполняя свою основную функцию жесткого каркаса, эти стенты со временем полностью деградируют, а вместе с ними исчезает субстрат для дальнейшего существования в этом месте воспалительной реакции. Не менее важен и тот факт, что с исчезновением стента восстанавливается вазомоторная функция артерии в месте стентирования, которая значительно страдает, вплоть до полного ее исчезновения, в период нахождения стента в просвете сосуда [3].
Первым массовым биодеградируемым коронарным стентом стал стент BVS (bioabsorbable vascular stent) Absorb. Было проведено несколько рандомизированных клинических исследований, изучавших безопасность и эффективность биосовместимых биодеградируемых стентов семейства ABSORB. По результатам анализа исследования Absorb III, включавшего в себя 3389 пациентов, оказалось, что имплантация стентов семейства BVS Absorb по сравнению со стентами на металлической основе, к сожалению, связана с высоким риском неблагоприятных сердечно-сосудистых событий (11,7 vs 8,1%, р=0,006) и частотой возникновения тромбоза стента (2,4 vs 0,6%, р=0,001) в первые три года после их имплантации [4]. Метаанализ исследований, включивших суммарно 5583 пациента, показал повышенный риск неблагоприятных сердечно-сосудистых событий в группе BVS Absorb: частота тромбоза — 9,6 vs 7,2%, р=0,003; летальность — 2,4 vs 0,7% (р<0,00001). В связи с такими неутешительными результатами компания производитель BVS Absorb “Abbott Laboratories” сообщила о прекращении производства и продаж данного продукта с мая 2017г на европейском медицинском рынке, и с сентября 2017г на американском медицинском рынке. На тот момент эти стенты были установлены ~150 тыс. пациентам [5].
Следует отметить, что, несмотря на прекращение производства и продажи стента BVS Absorb, вопросы в отношении их эффективности у разной категории больных остались изученными недостаточно полно, возможно была, в какой то степени, недооценка его положительных качеств. Несмотря на то, что производство этих стентов прекращено, целесообразно тщательно изучать отдаленные результаты стентирования с использованием BVS. В этом отношении особый интерес представляет анализ отдаленных результатов стентирования при сложных поражениях КА, к примеру, при бифуркационных стенозах и окклюзиях КА.
По мнению большинства специалистов, единой стратегии в отношении лечения такого рода поражений венечных сосудов не существует. На основании документов 14-го заседания Европейского бифуркационного клуба не рекомендуется использовать технику стентирования с одновременной имплантацией двух стентов методом SKS (simultaneous kissing stents) по следующим причинам: возможность деформации стентов и, как следствие, отсутствие уверенности получения хороших результатов; повышенная вероятность неполного покрытия стенок сосуда балками стента; опасность острого или подострого тромбоза стента; повышенная возможность формирования протяженной двухслойной (за счет балок двух стентов) неокарины; при стентировании по типу SKS образуется примерно в 47% случаев и в большинстве случаев стенозирует, тем самым, просвет артерий [6]. На том же заседании Европейского бифуркационного клуба были приведены неоспоримые доказательства необходимости использования методов внутрисосудистой визуализации при выполнении бифуркационного стентирования. Предпочтение в этом плане отдается методу оптически когерентной томографии (ОКТ), которая обеспечивает превосходную визуализацию.
В соответствии с изложенным представляется интересным представить на обсуждение клинический случай множественного стентирования КА тремя биодеградируемыми стентами, в т.ч. с бифуркационным стентированием передней межжелудочковой ветви (ПМЖВ) левой КА (ЛКА) и диагональной ветви (ДВ) ЛКА, двумя биодеградируемыми стентами BVS Absorb у больного с хронической формой ишемической болезни сердца. Случай этот интересен еще и тем, что на разных сроках после стентирования этому больному выполнялся коронароангиографический контроль с использованием ОКТ. Последнее исследование было выполнено спустя 5 лет после имплантации стентов.
Пациент М., 67 лет, поступил в “Научно-практический центр интервенционной кардиоангиологии” Департамента здравоохранения города Москвы (далее НПЦ ИК ДЗМ) 09.10.2014г с жалобами на жгуче-давящие боли за грудиной продолжительностью ~30 мин, возникающие при умеренных физических нагрузках, проходящие самостоятельно. Из анамнеза известно, что в марте 2013г больной перенес острый инфаркт миокарда (ОИМ) передней стенки левого желудочка (ЛЖ) с подъемом сегмента ST, был госпитализирован в одну из московских клиник, где ему в экстренном порядке была выполнена селективная коронароангиография (КАГ) с одномоментной баллонной ангиопластикой и стентированием проксимального сегмента ПМЖВ стентом Xience V 3,5×16 мм, с хорошим ангиографическим и клиническим эффектом. После выписки из стационара в течение года пациент чувствовал себя хорошо, приступов стенокардии не отмечал. В июне 2014г у него развился длительный интенсивный ангинозный приступ, в связи с чем он был госпитализирован в одну из городских больниц Москвы. На электрокардиограмме (ЭКГ) по сравнению с предыдущими ЭКГ — без существенных изменений. Больному была выполнена селективная КАГ, которая показала: правый тип коронарного кровообращения. Ствол ЛКА обычно развит, не поражен. В проксимальном отделе ПМЖВ ЛКА визуализируется стент без признаков деформации и стенозирования. В среднем сегменте, примерно в области отхождения от нее ДВ ЛКА, ПМЖВ ЛКА стенозирована до 75% (Medina 0:1:1). ДВ ЛКА хорошо развита, в устье сужена до 75-80% (рисунок 1). Огибающая артерия/ветвь (ОВ) ЛКА в среднем сегменте, в области отхождения от нее ветви тупого края (ВТК) ЛКА, стенозирована до 75% (рисунок 2). ВТК малого диаметра, в устье стенозирована ~50%. Правая коронарная артерия (ПКА) диффузно изменена, без гемодинамически значимого стенозирования. По неизвестным причинам рентгенэндоваскулярное вмешательство не выполнялось. Пациенту было рекомендовано выполнение стентирования ветвей ЛКА в плановом порядке. Медикаментозная терапия, с учетом наличия у больного в течение нескольких лет артериальной гипертензии, включала в себя нипертен 2,5 мг 1 раз/сут. (утром), эналаприл 2,5 мг 2 раза/сут., кардиомагнил 75 мг/сут., бриллинта 60 мг 2 раза/сут. Статины не принимал.
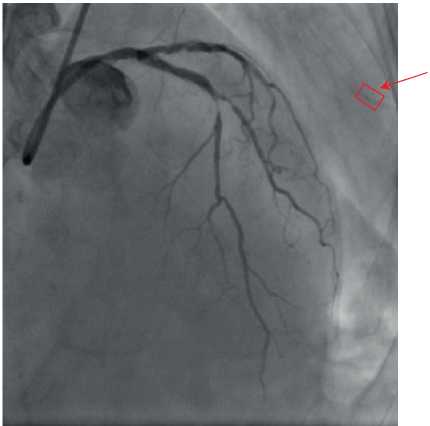
Рис. 1 Селективная коронарограмма ЛКА (LAO 45○/CAUD 25○).
Ниже стента визуализируется бифуркационное поражение ПМЖВ ДВ ЛКА.
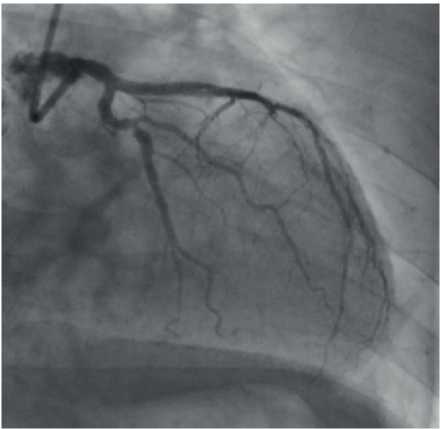
Рис. 2 Селективная коронарограмма ЛКА (RAO 20○/CAUD 35○).
На границе проксимальной средней трети ОВ (дистальнееВТК) стеноз >80%.
В октябре 2014г пациент был госпитализирован в НПЦ ИК ДЗМ для обследования и проведения, как ему и было рекомендовано, рентгенэндоваскулярной процедуры на КА. В период нахождения в стационаре пациент был обследован. По результатам лабораторных данных на момент поступления все показатели оставались в пределах нормы — мочевина 7,4 ммоль/л, креатинин 88 мкмоль/л, холестерин 4,1 ммоль/л, глюкоза 4,2 ммоль/л. Суточное монтирование ЭКГ показало, что у больного синусовый ритм с колебанием частоты сердечных сокращений от 45 уд./мин до 130 уд./мин (в среднем — 76 уд./мин), без существенных нарушений ритма. Регистрировались связанные с физической нагрузкой эпизоды депрессии сегмента ST по 1 каналу до 2,0 мм с продолжительностью до 3 мин. Тредмил-тест не проводили в связи с невозможностью отмены антигипертензивной терапии. По данным эхокардиографии были выявлены умеренные нарушения локальной сократимости ЛЖ по типу гипокинезии по передней стенке ЛЖ, однако глобальная сократительная функция ЛЖ при этом была удовлетворительной. Фракция выброса ЛЖ составила 60%. Также отмечена недостаточность митрального клапана 1 ст., и недостаточность трикуспидального клапана 2 ст.
На основании клинико-лабораторных данных и результатов КАГ было принято решение о проведении рентгенэдоваскулярной процедуры стентирования ПМЖВ ЛКА, ДВ ЛКА и ОВ ЛКА. Процедура была выполнена 13 октября 2014г. Она заключалась в баллонной дилятации с последующим бифуркационным стентированием по типу SKS ПМЖВ ЛКА и ДВ ЛКА двумя стентами Absorb 2,5×18 мм (рисунки 3, 4), затем были выполнены баллонная ангиопластика и стентирование среднего сегмента ОВ ЛКА стентом Absorb размером 3,0×28 мм. Процедура и ближайший послеоперационный период протекали без осложнений, и пациент был выписан из Центра под наблюдение врачей поликлиники по месту жительства. Рекомендован прием двойной дезагрегантной терапии и повторное обследование с проведением контрольной КАГ спустя 6 мес.
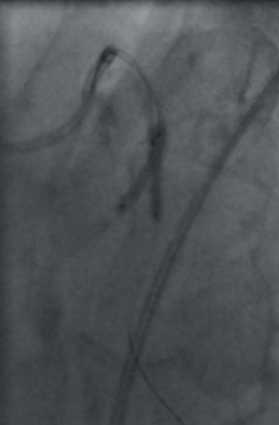
Рис. 3 Одномоментное “киссинг” стентирование ПМЖВ ДВ ЛКА биорезорбируемыми стентами (комментарии в тексте).
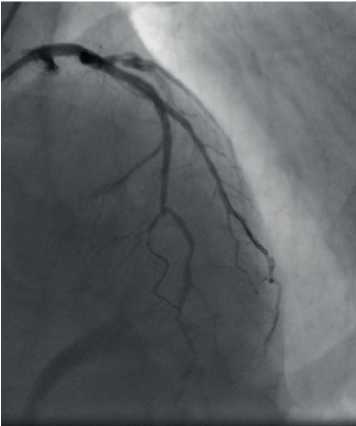
Рис. 4 Непосредственный удовлетворительный ангиографический результат стентирования.
Через 2 года после последней лечебной рентгенэндоваскулярной процедуры пациент был повторно приглашен в НПЦ ИК ДЗМ для обследования, включая селективную КАГ и ОКТ. Жалоб при поступлении не предъявлял, в течение прошедших двух лет чувствовал себя удовлетворительно, без приступов стенокардии. Больному была выполнена селективная КАГ, которая не выявила какой-либо динамики относительно предыдущей КАГ. Биодеградируемые стенты, имплантированные ранее в ПМЖВ, ДВ и ОВ ЛКА, были проходимы в полном объеме, без ангиографических признаков стенозирования. Отмечалось формирование неокарины, которая ангиографически выглядела как неконтрастируемое рентгенонегативное образование в просвете артерии в области бифуркации (рисунки 5, 6).
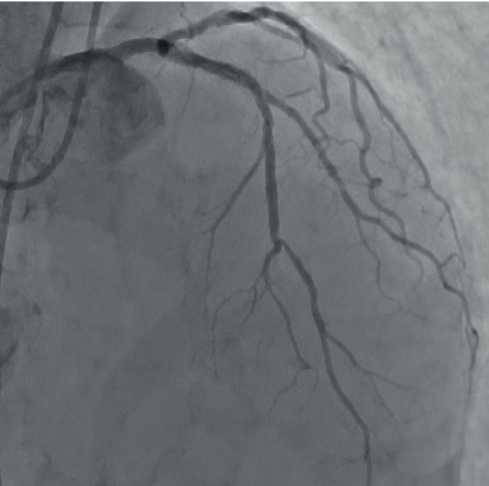
Рис. 5 Контрольная КАГ ЛКА через 2 года после эндоваскулярной процедуры в проекции RAO/LAO 0○, Сran 30○.
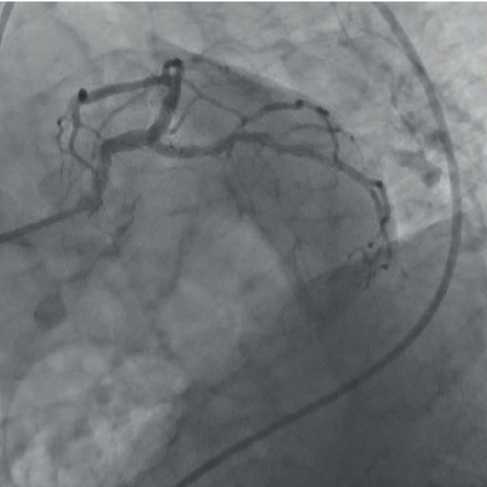
Рис. 6 Контрольная КАГ ЛКА через 2 года после эндоваскулярной процедуры в проекции LAO 42○, Саud 30○. Удовлетворительный ангиографический результат.
С целью детального изучения результатов стентирования больному была проведена ОКТ ПМЖВ и ДВ. Сканирование выполняли с использованием системы Ilumien (St. Jude, США) и оптического датчика DragonFly C7 с одновременным введением рентгенконтрастного вещества автоматическим инжектором Medrad Provis Mark 5 в объеме 20 мл со скоростью 4 мл/с. В результате исследования была получена продольная реконструкция изображения просвета сосуда на всем протяжении, значимых стенозирующих изменений сосуда не наблюдалось. Балки стента хорошо визуализированы, стент полностью равномерно эндотелизирован без какой-либо существенной деформации балок с признаками частичной резорбции. Профиль просвета артерии удовлетворительный, без признаков диссекции. Анализ данных сканирования проводили от дистальных участков ПМЖВ ЛКА к проксимальным. На продольной реконструкции геометрия артерий сохранена, сформирована протяженная полимерная неокарина. Длина неокарины 12 мм (расчет по шкале продольной реконструкции). Проксимальнее этой области наблюдаются металлические балки ранее имплантированного стента Xience V без стенозирующих изменений (рисунок 7).
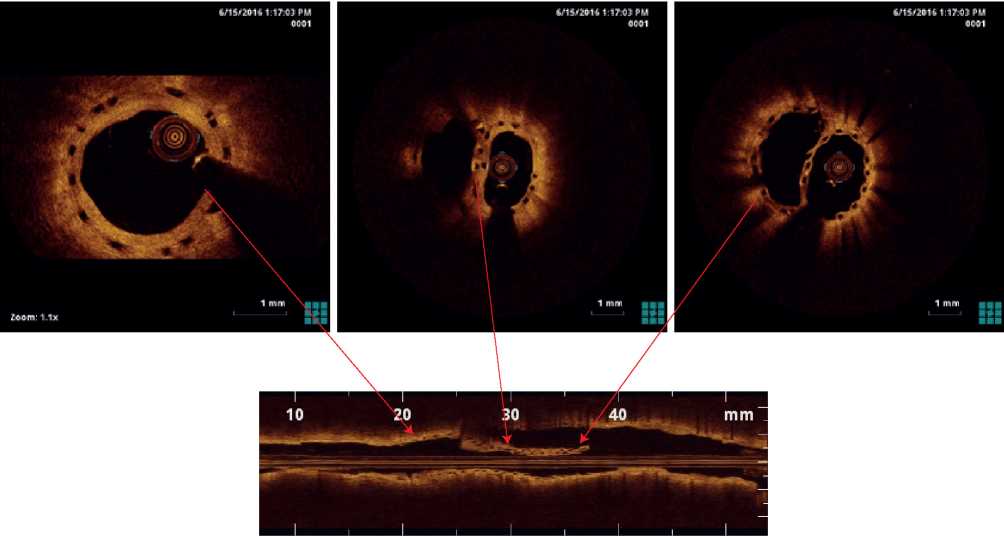
Рис. 7 ОКТ-контроль через 2 года после имплантации стентов Absorb. Протяженная неокарина.
Больной был выписан под наблюдение амбулатории с рекомендацией приема двойной дезагрегантной терапии.
Спустя 5 лет, несмотря на отсутствие жалоб, больной согласился на госпитализацию в Центр для контрольного обследования. Жалоб, как и ранее, не предъявлял, приступов стенокардии не отмечал, физическую нагрузку переносил удовлетворительно. Больному была выполнена селективная КАГ, по данным которой ПМЖВ ЛКА, ДВ ЛКА и ОВ ЛКА умеренно диффузно изменены, стентированные сегменты без потери просвета. Неконтрастирумое рентгенонегативное образование между ПМЖВ и ДВ (неокарина) не визуализируется (рисунки 8, 9).
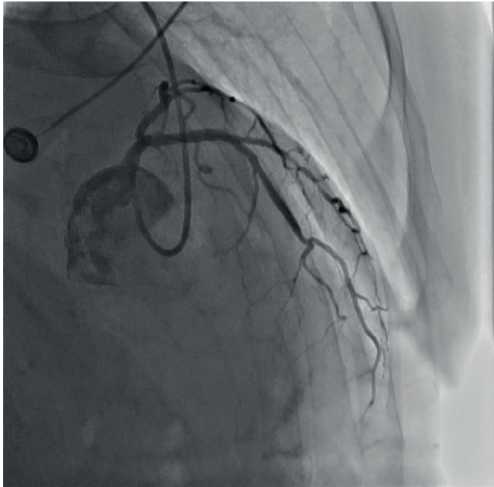
Рис. 8 Контрольная КАГ ЛКА через 5 лет после стентирования процедуры в проекции RAO 55○, Сran 25○.
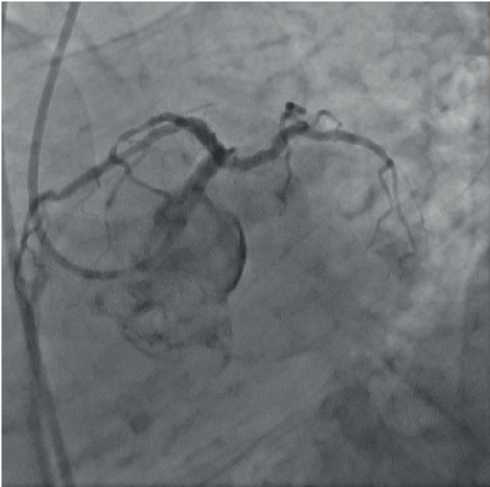
Рис. 9 Контрольная КАГ ЛКА через 5 лет после стентирования в проекции LAO 42○, Саud 30○.
Больному была выполнена ОКТ ветвей ЛКА, по данным которой ранее имплантированные биодеградируемые стенты не обнаружены, визуализируются лишь металлические (платиновые) метки, оставшиеся от них. В средней трети ПМЖВ ДВ определяются однородные участки умеренной гиперплазии внутренней выстилки с восстановленной геометрией просвета артерии без рестенозирования. От зоны дистальной кромки металлического стента Xience V (область проксимальных кромок биоразлагаемых стентов) на протяжении 12 мм визуализируется неокарина гребневидной формы, которая сформирована из интимальной ткани. Сегмент имплантации Absorb — без признаков стенозирования (рисунок 10). Толщина неокарины составляет 0,4 мм (в широкой части) и 0,21 мм (в тонкой части) (рисунок 11).
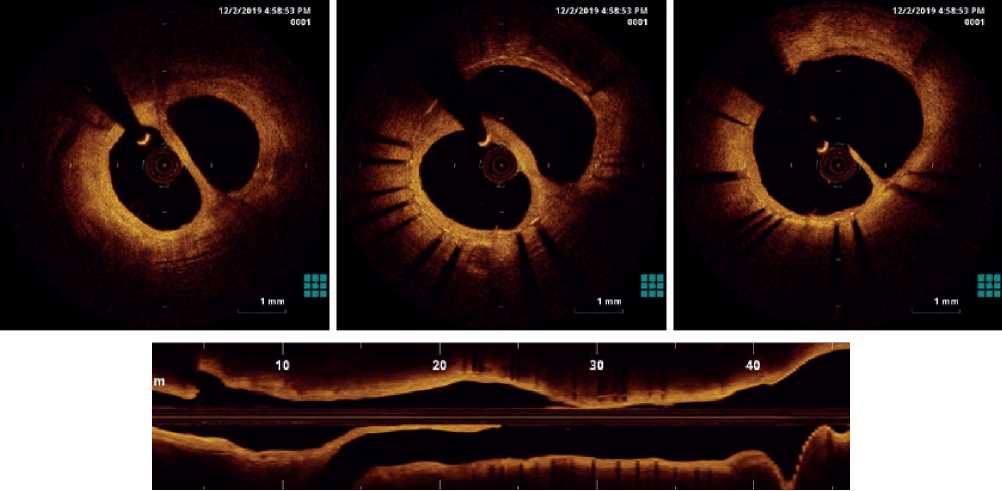
Рис. 10 Продольная реконструкция ОКТ ПМЖВ и ДВ с признаками сформированной неокарины из интимальной ткани. Мембранная карина в зоне контакта двух absorb (~12 мм).
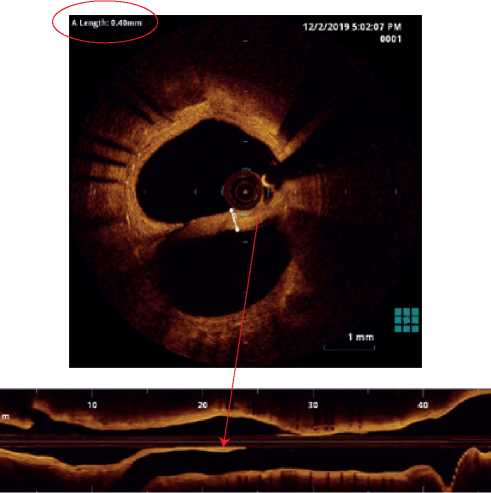
Рис. 11 Расчётная толщина мембраны неокарины 0,4 мм (в самой широкой части) и 0,21 мм (в тонкой части).
Ближе к основанию визуализируется дефект неокарины, а также признаки фиброкальциноза стенки сосуда. На отдельных участках артериальной стенки лоцированы скопления фиброзной ткани и единичные липидные пятна, не суживающие просвет сосуда. Протяженность неокарины из ДВ составляет 9 мм. Геометрия ПМЖВ и ДВ в области протяженного соприкосновения сохранена, артерии без существенных деформаций. Артериальная стенка в границах проксимального стентированного участка и перекреста с новой бифуркацией — с признаками состоявшегося заживления, без патологических интимальных и субинтимальных отложений (рисунок 12).
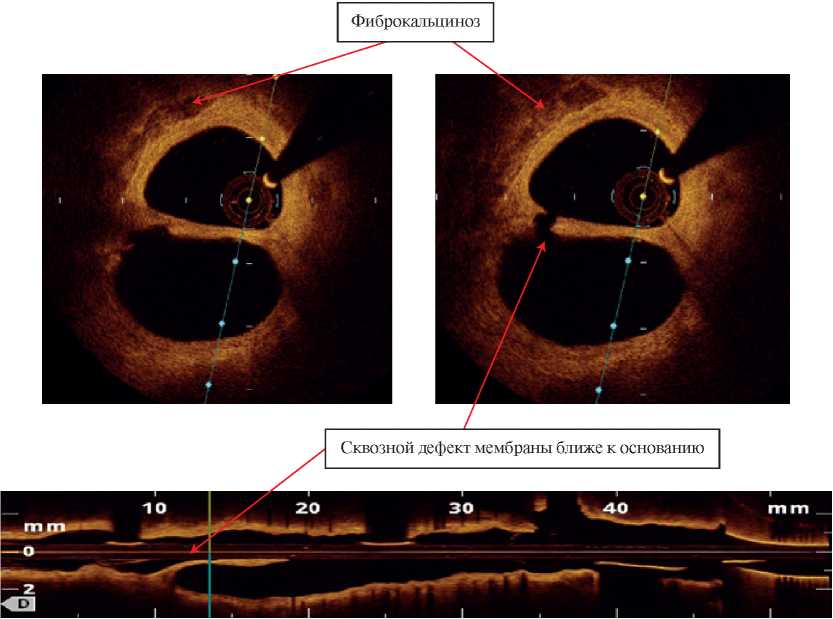
Рис. 12 ОКТ-скан из ДВ. Сквозной дефект неокарины и участки фиброкальциноза в стентированном Absorb сегменте.
Имплантированный в проксимальном сегменте ПМЖВ стент с металлическим каркасом XIENCE V (со 100% рассеиванием световых волн) равномерно расправлен (индекс симметричности стента SSI =0,88), полностью эндотелизирован без признаков рестеноза (индекс неоинтимальной гиперплазии NIH index =0,9). В устье ПМЖВ определяется единичный кальциевый локус с распространением до устья ствола ЛКА, без сужения просвета (рисунок 13).
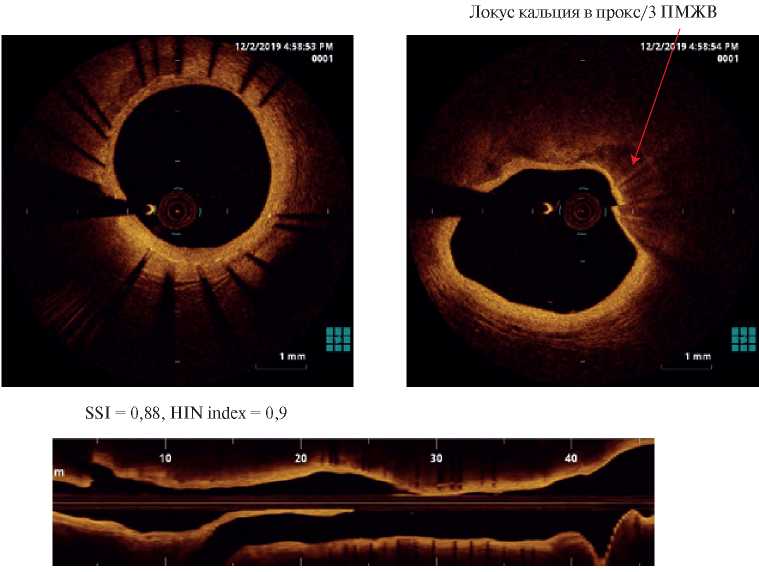
Рис. 13 Стент Xience в проксимальном сегменте ПМЖВ.
При ОКТ ОВ в области имплантации стента BVS absorb сосуд выглядит с полностью состоявшимся заживлением, балки стента не визуализируются, по-видимому, ввиду их резорбции. В проксимальном и дистальном участках стентированного сегмента просматриваются платино-иридиевые метки стента, вмурованные в стенку артерии (ярко освещенные инородные структуры со 100% отражением света и хорошо различимой световой тенью). В том же срезе неизмененная гистологическая картина артерии с четкой дифференцировкой слоев артериальной стенки, выстланная неоинтимальной тканью, единичными участками липидно-фиброзных включений, без гемодинамически значимого стенозирования (рисунок 14).
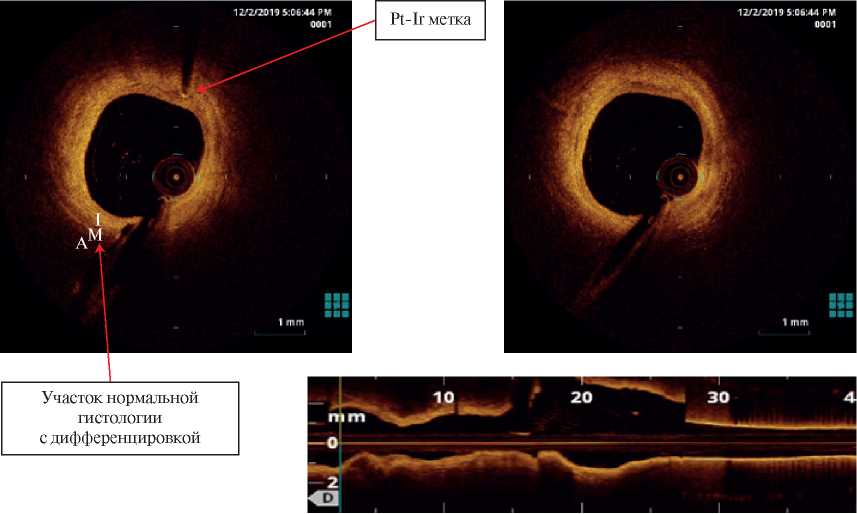
Рис. 14 ОКТ ОВ. (I — intima; M — media; A — adventitia). Платино-иридиевые метки в медии ОВ (пояснения в тексте).
Заключение
С момента создания и успешного применения первого стента исследователи не переставали искать способ нивелировать негативное влияние перманентного присутствия металлического каркаса в живой ткани. Наиболее биосовместимым полимерным материалом, обладающим необходимыми физическими свойствами, является полимер PLLA, из которого изготовлен стент Absorb.
Примечательно, что Absorb в представленном клиническом случае с момента имплантации и на протяжении 5 лет сохранил свою полную биосовместимость. Отмечается сохраненная геометрия КА в области бифуркации, что свидетельствует о равномерной резорбции и сохранении радиальной жесткости на весь необходимый для заживления период. Этот фактор можно рассматривать как ключевой в процессе физиологического заживления стентированной бифуркации в представленном клиническом случае.
В целом имплантация каркасов из полимерных материалов способствует более физиологическому заживлению. Протрузия балок стента Absorb (значительно крупнее аналогичных у лекарственных стентов) в просвете артерии становится триггером неоинтимальной пролиферации. Завершается процесс формированием слоя неонтимы, который состоит из соединительной ткани и гладкомышечных клеток, которые надежно покрывают атеросклеротическую бляшку. В литературе сообщается, что неонтима после установки стентов Absorb обеспечивает стабилизацию бляшек [7], а, значит, в призме формирования мембранной неокарины может рассматриваться как довольно прочная структура с низкой степенью вероятности надрыва и дислокации.
Absorb благодаря своей биосовместимости сам по себе является мощным фактором физиологического сосудистого ремоделирования. Указанные свойства скаффолдов позволяют в будущем рассматривать их в качестве сосудомодулирующих имплантов и имеют перспективу отказа от токсичных в определенной мере цитостатических препаратов.
Имплантация биодеградируемых стентов методом SKS в литературе не описана. Иные техники бифуркационного стентирования одним или двумя биодеградируемыми стентами встречаются отдельными сообщениями и никакие исследования по ним не проводились.
Все вышесказанное позволяет полагать, что отзыв биодеградируемых стентов и отказ от их применения является лишь временной мерой, направленной на углубление доклинических исследований.
Список литературы
1. Карпов Ю. А., Самко А. Н., Буза В. В. Коронарная ангиопластика и стентирование. Медицинское информационное агентство. Москва, 2010. сс. 263-273. ISBN: 978-5-8948-1819-1.
2. Асадов Д. А., Сухоруков О. Е., Кузнецова И. Э. и др. Чрескожные коронарные вмешательства с использованием лекарственных стентов: прошлое настоящее и будущее (обзор данных литературы). Международный Журнал интервенционной кардиоангиологии. 2013;32:45-50.
3. Асадов Д. А., Сухоруков О. Е., Кузнецова И. Э. и др. Перспективы применения биодеградируемых стентов в лечении атеросклеротических заболеваний сосудов (обзор данных литературы) Международный Журнал интервенционной кардиоангиологии. 2013;32:51-6.
4. Kereiakes DJ, Ellis SG, Metzger C, et al. 3-Year clinical outcomes with Everolimus-Eluting Bioresorbable coronary Scaffolds: The ABSORB III Trial. J Am Coll Cardiol. 2017;70(23):2875-7. doi:10.1016/j.jacc.2017.10.010.
5. Kimura T, Kozuma K, Tanabe K, et al. A randomized trial evaluating everolimus-eluting Absorb bioresorbable scaffolds vs. everolimus-eluting metallic stents in patients with coronary artery disease: ABSORB Japan. Eur Heart J. 2015;36(47):3332-42. doi:10.1093/eurheartj/ehv435.
6. Lassen JF, Holm NR, Stankovic G, et al. Percutaneous coronary intervention for coronary bifurcation disease: consensus from the first 10 years of the European Bifurcation Club meetings. Eurointervention. 2014;10:545-60. doi:10.4244/EIJV10I5A97.
7. Vahl TP, Gaisor P, Gongora CA, et al. Four-year polymer biocompatibility and vascular healing profile of a novel ultrahigh molecular weight amorphous PLLA bioresorbable vascular scaffold: an OCT study in healthy porcine coronary arteries. Eurointervention. 2016;12:1510-18. doi:10.4244/EIJ-D-16-00308.
Об авторах
Д. Г. ИоселианиРоссия
Давид Георгиевич Иоселиани — академик РАН, доктор медицинских наук, профессор, зав. кафедрой интервенционной кардиоангиологии
Д. А. Асадов
Россия
Джамиль Арифович Асадов — кандидат медицинских наук, доцент кафедры интервенционной кардиоангиологии, врач рентгенохирургических методов диагностики и лечения
Москва, Тел.: +7 (910) 453-73-53
В. В. Фоменко
Россия
Виктория Владимировна Фоменко — врач рентгенохирургических методов диагностики и лечения
А. В. Азаров
Россия
Алексей Викторович Азаров — кандидат медицинских наук, доцент кафедры интервенционной кардиоангиологии, зав. отделением рентгенохирургических методов диагностики и лечения
С. П. Семитко
Россия
Сергей Петрович Семитко — доктор медицинских наук, профессор кафедры интервенционной кардиоангиологии, директор центра
Рецензия
Для цитирования:
Иоселиани Д.Г., Асадов Д.А., Фоменко В.В., Азаров А.В., Семитко С.П. Пятилетний результат имплантации биодеградируемых стентов Absorb по методике бифуркационного стентирования. Кардиоваскулярная терапия и профилактика. 2021;20(4):2864. https://doi.org/10.15829/1728-8800-2021-2864
For citation:
Ioseliani D.G., Asadov D.A., Fomenko V.V., Azarov A.V., Semitko S.P. Five-year outcomes of implantation of Absorb biodegradable stents using the bifurcation stenting technique: a case report. Cardiovascular Therapy and Prevention. 2021;20(4):2864. (In Russ.) https://doi.org/10.15829/1728-8800-2021-2864
JATS XML

























































