Перейти к:
Фокусированное ультразвуковое исследование сосудов. Консенсус российских экспертов
https://doi.org/10.15829/1728-8800-2022-3333
Аннотация
Стандартные протоколы ультразвукового исследования включают исследования всех сосудов анализируемой области, во всех режимах сканирования, с полным набором измерений, и требуют высокой квалификации специалистов и больших временных затрат. Однако для ряда клинических задач достаточно выполнения фокусированного протокола ультразвукового исследования, т.е. ориентированного на решение конкретной проблемы и, следовательно, сокращенного по времени, тем самым позволяющего увеличить число обследуемых. Оценка сердечно-сосудистого риска с помощью выявления атеросклеротических бляшек в сонных и бедренных артериях, скрининг на наличие аневризмы аорты, выявление проксимального тромбоза глубоких вен нижних конечностей – это те направления в медицине, где фокусированные протоколы ультразвукового исследования могут повысить долю обследуемых и способствовать своевременной диагностике и профилактике заболеваний. Доступность фокусированного ультразвукового исследования и развитие образовательных структур позволят расширить круг специалистов, способных выполнять подобные исследования (кардиологи, терапевты, врачи общей практики, сосудистые хирурги). Сегодня существует много вопросов по организации проведения фокусированных протоколов в клинической практике. Данный консенсусный документ направлен на повышение информированности широкого круга специалистов о задачах, принципах проведения и применении фокусированного УЗИ.
Для цитирования:
Балахонова Т.В., Ершова А.И., Ежов М.В., Барбараш О.Л., Берштейн Л.Л., Богачев В.Ю., Воевода М.И., Генкель В.В., Гуревич В.С., Дупляков Д.В., Имаев Т.Э., Коновалов Г.А., Космачева Е.Д., Лобастов К.В., Митькова М.Д., Никифоров В.С., Ротарь О.П., Сучков И.А., Явелов И.С., Митьков В.В., Акчурин Р.С., Драпкина О.М., Бойцов С.А. Фокусированное ультразвуковое исследование сосудов. Консенсус российских экспертов. Кардиоваскулярная терапия и профилактика. 2022;21(7):3333. https://doi.org/10.15829/1728-8800-2022-3333
For citation:
Balakhonova T.V., Ershova A.I., Ezhov M.V., Barbarash O.L., Bershtein L.L., Bogachev V.Yu., Voevoda M.I., Genkel V.V., Gurevich V.S., Duplyakov D.V., Imaev T.E., Konovalov G.A., Kosmacheva E.D., Lobastov K.V., Mitkova M.D., Nikiforov V.S., Rotar O.P., Suchkov I.A., Yavelov I.S., Mitkov V.V., Akchurin R.S., Drapkina O.M., Boytsov S.A. Focused vascular ultrasound. Consensus of Russian experts. Cardiovascular Therapy and Prevention. 2022;21(7):3333. (In Russ.) https://doi.org/10.15829/1728-8800-2022-3333
ВВЕДЕНИЕ
Ультразвуковое исследование (УЗИ) сосудов — незаменимый диагностический инструмент в кардиологии, неврологии, сосудистой хирургии. Пациентам, имеющим клинические признаки сосудистой патологии, обычно проводится стандартное УЗИ соответствующего сосудистого бассейна врачами ультразвуковой или функциональной диагностики. В то же время в мировой клинической практике уже давно применяются короткие (фокусированные, сокращенные) протоколы УЗИ, сфокусированные на конкретной задаче или клинической ситуации (УЗИ непосредственно в месте (во время) оказания медицинской помощи (Pointofcare ultrasound (POCUS)), фокусированное УЗИ сердца (Focused cardiac ultrasound (FoCUS)), фокусированное УЗИ при травме (Focused assessment with sonography in trauma (FAST)). Эти протоколы целенаправленны, ориентированы на решение конкретной проблемы, имеют ограниченную сферу применения, значительно упрощены, сокращены по времени относительно полного протокола, воспроизводимы, содержат качественные и полуколичественные параметры [1][2]. Фокусированное УЗИ имеет множество достоинств в повседневной клинической практике, включая повышение своевременности и точности диагностики, а также предоставление информации о прогнозе пациента и течении заболевания в динамике [2]. УЗИ в месте оказания медицинской помощи основано на систематическом применении метода в качестве дополнения к обычному физикальному обследованию, что способствует улучшению диагностических возможностей врача [3]. Фокусированное УЗИ ввиду его относительной простоты может быть проведено врачами, не являющимися профильными специалистами в области ультразвуковой диагностики. При этом важно заметить, что фокусированный протокол УЗИ не заменяет полные исследования, проводимые врачами ультразвуковой или функциональной диагностики. Фокусированное УЗИ используется в четко определенных клинических ситуациях, и его навыки обычно приобретаются в течение короткого периода обязательного обучения [2]. Использование кратких протоколов УЗИ значительно расширилось за последние несколько лет, во многом вследствие значительного расширения возможностей и уменьшения размера современных ультразвуковых аппаратов, применения в т.ч. портативных устройств, которые способны обеспечивать изображение высокого качества [4]. Кроме того, в некоторых работах была показана экономическая эффективность применения фокусированных протоколов [5].
Фокусированные протоколы разработаны и для исследования сосудов (Focsed Vascular UltraSound, FOVUS [6]). Они имеют разные клинические цели. В частности, предложен фокусированный протокол исследования сонных (СА) и бедренных (БА) артерий для оценки сердечно-сосудистого риска (ССР) (определение наличия атеросклеротических бляшек (АСБ)) [7], разработан фокусированный протокол исследования глубоких вен нижних конечностей для исключения проксимального тромбоза глубоких вен (ТГВ) при таком жизнеугрожающем состоянии, как тромбоэмболия легочной артерии (ТЭЛА) [8], рекомендуется скрининг на наличие бессимптомной патологии (аневризмы брюшной аорты (АБА) с помощью определения ее диаметра) [9]. Таким образом, будучи направленным не только на оценку ССР, но и своевременную диагностику жизнеугрожающих состояний, фокусированное исследование сосудов может быть полезным инструментом в руках не только врачей ультразвуковой и функциональной диагностики, но и, например, кардиологов1 и анестезиологов-реаниматологов2.
Утвержденный в 2018г профессиональный стандарт “Врач-кардиолог”, согласно которому в компетенции специалиста указанного профиля включены не только понимание и интерпретация данных трансторакальной эхокардиографии и УЗИ сосудов, но и проведение указанных исследований3, способствует более активному внедрению фокусированных УЗИ в клиническую практику врача-кардиолога.
Представленный документ посвящен задачам и особенностям использования скринингового фокусированного УЗИ СА, БА, брюшного отдела аорты, а также фокусированного УЗИ глубоких вен нижних конечностей. Документ создан с целью внедрения фокусированного УЗИ сосудов в практическую деятельность, прежде всего, врачей-кардиологов, врачей ультразвуковой и функциональной диагностики, врачей анестезиологов-реаниматологов, сердечно-сосудистых хирургов, что представляется очень актуальным, т.к. способствует ранней и своевременной диагностике сосудистой патологии.
ОБОРУДОВАНИЕ ДЛЯ ПРОВЕДЕНИЯ ФОКУСИРОВАННЫХ УЗИ
Согласно конструктивному исполнению, медицинские ультразвуковые диагностические системы (ультразвуковые аппараты, ультразвуковые приборы, ультразвуковые сканеры) делятся на передвижные и переносные (портативные). Согласно качеству получаемой диагностической информации и функциональным возможностям, ультразвуковые сканеры делятся на аппараты среднего, высокого или экспертного класса4. Ультразвуковые сканеры всех типов могут использоваться для проведения фокусированного УЗИ сосудов. Передвижные ультразвуковые сканеры обычно имеют более низкую мобильность и высокую стоимость. Оборудование подобного класса в России сосредоточено в кабинетах и отделениях ультразвуковой и функциональной диагностики.
В настоящее время все шире используются портативные ультразвуковые сканеры, которые по набору диагностических технологий не уступают передвижным ультразвуковым системам. Основное преимущество портативных сканеров — их мобильность, которая позволяет выполнять УЗИ в любом месте, вне зависимости от того, где находится пациент. На мировом рынке представлено большое количество портативных ультразвуковых сканеров высокого и экспертного класса, которыми можно заменить передвижную ультразвуковую систему в определенных условиях [10]. При УЗИ сосудов на подобных портативных ультразвуковых приборах имеется возможность автоматических или полуавтоматических измерений средней и максимальной толщины комплекса интима-медиа (ТИМ) (под максимальной ТИМ подразумевается в т.ч. измерение высоты АСБ). Полуавтоматический метод измерения ТИМ предусматривает то, что исследователь может скорректировать вручную неверно распознанные системой границы стенки. Методы автоматического оконтуривания стенки артерии позволяют быстро провести измерение ТИМ, высоты АСБ, повысить производительность обследования и увеличить пропускную способность кабинета. В процессе формирования отчета в ряде ультразвуковых сканеров по полученным данным оценивается риск сердечно-сосудистых событий (ССС) для каждого отдельного пациента согласно Манхеймским таблицам и Фрамингемской шкале риска [10]. Портативные ультразвуковые системы доступны существенно более широкому кругу врачей-специалистов в приемных, плановых, экстренных отделениях, операционных и мобильных бригадах. В неотложной и экстренной ситуациях портативные ультразвуковые аппараты могут быть использованы для качественной и количественной оценки при дифференциальной диагностике с вариантами ответа “да/нет”.
На мировом рынке существует большое количество ультрапортативных (карманных, планшетных, handheld, ultramobile) ультразвуковых диагностических приборов, которые можно условно разделить на две большие группы: проводные (датчик соединен гибким многожильным кабелем с устройством отображения получаемой информации) и беспроводные (передача информации от датчика осуществляется по каналам WiFi или BlueTooth). В качестве устройств отображения используются планшеты или смартфоны, а основные узлы устройства ультразвукового сканирования, обработки информации и формирования акустических изображений для разных режимов работы в разных моделях могут располагаться полностью или частично в корпусе датчика или корпусе планшета или смартфона. Основной недостаток этих приборов — малое количество стандартных программ и специализированных программных измерений [10].
Исследование с использованием портативных ультразвуковых сканеров может проводиться непрофильными специалистами, но, что принципиально важно заметить, только при наличии специальной подготовки и сдачи теоретического и практического экзаменов. Принципиально важно подчеркнуть, что каждый из описанных ниже фокусированных протоколов УЗИ сосудов должен применяться четко в рамках представленной в документе цели.
ФОКУСИРОВАННОЕ УЗИ СА И БА
Место фокусированного УЗИ СА и БА
Дуплексное сканирование (ДС), или УЗИ5, артерий — это неинвазивный, доступный, хорошо воспроизводимый метод, позволяющий определять функциональные и структурные нарушения артериальной стенки, с высокой точностью выявлять начальные изменения стенки в виде утолщения и нарушения структуры комплекса интима-медиа, определять наличие и морфологию АСБ, ее осложнения, оценивать выраженность атеросклеротических изменений. Клинические рекомендации последних лет, как европейские, так и российские, свидетельствуют об информативности неинвазивных УЗИ именно СА и БА с целью стратификации ССР независимо от возраста и других факторов риска (ФР) [11][12]. Так, согласно рекомендациям 2019г по ведению пациентов с дислипидемиями Европейского общества кардиологов (ESC) и Европейского общества по изучению атеросклероза (EAS), наличие АСБ в СА и/или БА, выявленное при УЗИ, следует рассматривать как модификатор низкого или умеренного ССР (класс рекомендаций — IIa, уровень доказательности — B), а наличие значимой АСБ в СА (стеноз ≥50%, АСБ с признаками нестабильности) свидетельствует об очень высоком ССР у пациента [12]. В соответствии с Российскими рекомендациями по диагностике и коррекции нарушений липидного обмена с целью профилактики и лечения атеросклероза наличие значимой АСБ любой локализации указывает на очень высокий ССР, АСБ в некоронарных артериях со стенозом 25-49% — на высокий ССР [11]. Согласно рекомендациям по ультразвуковой оценке АСБ СА 2020г Американского общества эхокардиографии (ASE), рекомендуется проводить фокусированное УЗИ СА и на основании высоты АСБ стратифицировать ССР: отсутствие АСБ или высота АСБ <1,5 мм — низкий ССР, 1,5 мм≤ высота АСБ <2,5 мм — умеренный ССР, высота АСБ ≥2,5 мм — высокий ССР [13].
Может создаваться впечатление, что в противовес вышеперечисленным документам звучат рекомендации комиссии США по профилактическим мероприятиям (US Preventive Services Task Force (USPSTF)) 2021г [14], согласно которым скрининг на наличие асимптомного стеноза каротидных артерий в общей популяции не приносит пользы и, напротив, может нанести вред. Основным аргументом, обусловливающим эти рекомендации, выступает отсутствие доказательств преимуществ и безопасности хирургического лечения асимптомного атеросклероза по сравнению с консервативной тактикой. И в этом кроется главное смысловое отличие рекомендаций USPSTF от вышеперечисленных: они посвящены не оценке ССР, а скринингу на наличие значимого атеросклероза (стеноз ≥50%) среди лиц без инсульта или транзиторной ишемической атаки в анамнезе [14].
До недавнего времени в диагностической практике не было таких исследований, как фокусированное УЗИ СА или УЗИ БА, были только стандартные ДС (УЗИ) экстракраниального отдела брахиоцефальных артерий (БЦА) и ДС (УЗИ) артерий нижних конечностей [15].
Стандартный протокол ДС экстракраниального отдела БЦА имеет следующие показания: любые формы сосудисто-мозговой недостаточности, шумы над сосудами шеи, отсутствие или асимметрия пульса или артериального давления на руках, состояние после каротидной эндатерэктомии или стентирования, анамнестические данные о патологии каротидного и/или вертебрального бассейнов, наличие пульсирующих образований на шее, предоперационная подготовка пациентов к операциям с применением искусственного кровообращения или длительной гипотензией, а также наличие ФР развития атеросклероза (двух и более или одного в значительной степени выраженного) [16]. Стандартный протокол ДС экстракраниального отдела БЦА включает определение наличия, степени выраженности атеросклероза, оценку структуры и поверхности АСБ, характеристику кровотока и хода не только СА, но и позвоночных, подключичных артерий и брахиоцефального ствола [17]. При этом используют В-режим, режимы цветового картирования и импульсноволновой допплерографии. Протокол также содержит автоматическое измерение средней ТИМ СА [18]. При ДС можно также количественно оценивать эхогенность АСБ путем анализа медианы серой шкалы (grey-scale median, GSM). Уже накоплены данные о том, что АСБ с низкой эхогенностью в СА является предиктором коронарных событий [19]. Однако на сегодняшний день недостаточно данных о воспроизводимости анализа медианы серой шкалы для внедрения метода оценки эхогенности в рутинную клиническую практику.
Показания для стандартного протокола ДС (УЗИ) артерий нижних конечностей следующие: признаки ишемии нижних конечностей, переломы нижних конечностей, исключение артериовенозной мальформации после пункции, оценка эффективности реконструктивных операций на артериях нижних конечностей. ДС артерий нижних конечностей включает оценку хода, просвета, стенок и гемодинамических характеристик всех основных артерий нижних конечностей [17].
Результаты стандартного протокола отвечают на большое количество клинических вопросов, что не требуется при конкретной задаче, поставленной в текущих клинических рекомендациях, — оценить ССР. Более того, стандартное УЗИ экстракраниального отдела БЦА и артерий нижних конечностей требует высокой квалификации специалистов и больших временных затрат. Так, стандартный протокол ДС экстракраниального отдела БЦА может занимать до 45 мин [7]. Вероятно, с учетом и временных, и трудовых затрат, согласно Российским рекомендациям по организации проведения диспансеризации определенных групп взрослого населения 2017г, проведение ДС экстракраниального отдела БЦА по стандартному протоколу включено только во второй этап диспансеризации и проводится у мужчин в возрасте от 45 до 72 лет и женщин в возрасте от 54 до 72 лет при наличии комбинации трех ФР развития хронических неинфекционных заболеваний (повышенный уровень артериального давления, гиперхолестеринемия, избыточная масса тела или ожирение) либо по направлению врача-невролога при впервые выявленном указании или при подозрении на ранее перенесенное острое нарушение мозгового кровообращения лицам в возрасте 75-90 лет, не находящимся по этому поводу под диспансерным наблюдением [20].
Предложение сократить стандартный протокол УЗИ артерий в соответствии с конкретными задачами появилось достаточно давно. Так, в работе Lavenson GS, et al. (2004) было предложено быстрое исследование СА с помощью цветового и импульсноволнового допплеровских методов [5]. Целью протокола было выявить наличие/отсутствие АСБ в СА, и если АСБ имеются, то указать процент стеноза — >50% или <50%. В случае подозрения на наличие АСБ, сужающей просвет сосуда более чем на 50%, пациента направляли на стандартное обследование. Такой подход к выявлению пациентов со значимыми АСБ показал высокую чувствительность (93%), специфичность (87%) и экономическую эффективность: при проведении исследований у 6073 пожилых (>60 лет) людей будет предотвращено 30 инсультов и, как следствие, сэкономлено ~2 млн долларов. В исследовании Hogberg D, et al. (2016) также был предложен фокусированный протокол УЗИ СА [21]. Исследователи предложили протокол УЗИ внутренних СА без оценки скоростных показателей, за счет чего было значительно сокращено время исследования при сохранении высокой информативности исследования. Чувствительность, специфичность, прогностическая ценность положительного результата и прогностическая ценность отрицательного результата для выявления лиц с АСБ, сужающими просвет артерии >20%, с помощью предложенного подхода составили 91%, 97%, 31% и 97%, а для лиц с АСБ, сужающими просвет артерий >50%, — 90%, 97%, 11% и 100%, соответственно.
В последние годы все чаще в литературе можно встретить такие понятия, как фокусированное УЗИ сосудов (FOVUS), фокусированное УЗИ СА (focused carotid ultrasound) или УЗИ у постели больного (POCUS) [6][13][22], внедряющиеся в практику врачей многих специальностей. Так, согласно рекомендациям по ультразвуковой диагностике у постели больного (POCUS) Европейской федерации внутренних болезней (European Federation of Internal Medicine (EFIM)), ультразвуковая оценка АСБ СА входит в расширенные компетенции врача-терапевта [2].
В 2019г российскими специалистами был разработан сокращенный протокол ДС СА для оценки доклинического атеросклероза и последующего уточнения ССР [7]. Было предложено внедрить протокол УЗИ СА для определения только факта наличия АСБ в каротидном бассейне (сокращенный протокол 1). Этот протокол требует незначительных временных затрат (уменьшает продолжительность исследования на 72% по сравнению со стандартным протоколом) и не требует высокой квалификации специалиста, проводящего исследование. С учетом текущих на тот момент клинических рекомендаций и документов о диспансеризации, было предложено проведение УЗИ СА по сокращенному протоколу 1 лицам с низким или умеренным ССР в возрасте от 40 лет, лицам с артериальной гипертензией, гиперхолестеринемией (общий холестерин >7,5 ммоль/л и/или холестерин липопротеидов низкой плотности >4,9 ммоль/л), ранним сердечно-сосудистым заболеванием (ССЗ) атеросклеротического генеза в семейном анамнезе и/или хронической болезнью почек в возрасте 2739 лет [7].
При выявлении хотя бы одной АСБ при проведении УЗИ СА по сокращенному протоколу 1 предполагалось более углубленное исследование с измерением степени стеноза в месте локации каждой из имеющихся АСБ, описанием их морфологии: сокращенный протокол 2, который позволяет сократить продолжительность исследования, по сравнению со стандартным УЗИ экстракраниального отдела БЦА, на 32% [7]. При сокращенном протоколе 2 оценивали степень выраженности и структуру АСБ в полном объеме и измеряли ТИМ общей СА в автоматическом режиме. Сокращенный протокол 2 рекомендовалось проводить врачу ультразвуковой или функциональной диагностики. Если при этом выявляли АСБ со стенозом ≥50%, было рекомендовано расширить исследование до объема стандартного протокола ДС БЦА, т.к. в этом случае повышается вероятность выявить значимый атеросклероз в бассейнах других артерий.
С целью оценки пользы применения фокусированного УЗИ СА и новой градации бляшек, разработанной ASE, было проведено проспективное исследование по оценке исходов у пациентов, подвергшихся коронароангиографии, в зависимости от максимальной высоты АСБ [23]. За участниками наблюдали в течение 1,3-5,1 года (средний период наблюдения 3,6±1,7 года) для выявления ССС. Крупные ССС (смерть, инфаркт миокарда, инсульт и транзиторная ишемическая атака) были ассоциированы с максимальной высотой АСБ. У участников исследования с высотой АСБ ≥1,5 мм чаще развивалась стабильная стенокардия, они чаще переносили аортокоронарное шунтирование. Анализ выживаемости Каплана-Мейера продемонстрировал достоверное расхождение кривых, отражающих комбинированную конечную точку (смерть, инфаркт миокарда, инсульт и транзиторная ишемическая атака), при разделении исследуемых в зависимости от высоты АСБ (<1,5 мм и ≥1,5 мм) (p=0,02). Авторы работы сделали выводы о том, что фокусированное УЗИ СА, являясь быстрым и удобным методом, может служить инструментом для прогнозирования серьезных ССС [23].
Для проведения фокусированного УЗИ артерий могут быть использованы портативные ультразвуковые системы. Mantella LE, et al. (2019) показали высокую корреляцию при измерении высоты (r=0,84, p<0,0001) и площади (r=0,94, p<0,0001) АСБ СА с помощью портативного и передвижного ультразвукового сканера, что свидетельствует о возможности точной и быстрой оценки АСБ у постели больного, способствующей улучшению стратификации ССР [24]. При УЗИ в сосудистом режиме в портативных приборах может быть реализована возможность автоматических или полуавтоматических измерений (автоматического оконтуривания стенки артерии), что позволяет быстро провести измерение ТИМ, высоты АСБ, повысить производительность обследования и увеличить пропускную способность кабинета. Полуавтоматический метод измерения ТИМ предусматривает то, что исследователь может скорректировать неверно распознанные границы стенки вручную [25].
Фокусированное УЗИ сосудов не заменяет стандартные протоколы, но позволяет быстро и эффективно решать ряд клинических задач, охватывая при этом большее число обследуемых (таблица 1).
Таблица 1
Сравнительная оценка стандартного УЗИ экстракраниальных отделов БЦА и артерий нижних конечностей и фокусированного УЗИ СА и БА

Примечание: АСБ — атеросклеротическая бляшка, БА — бедренные артерии, БЦА — брахиоцефальные артерии, СА — сонная артерия, ССР — сердечно-сосудистый риск, УЗИ — ультразвуковое исследование.
Проведение фокусированного УЗИ артерий может показаться простым, однако оно требует обязательного обучения. Эти требования сформулированы в регламентирующих документах для фокусированного УЗИ в кардиологии (FOCUS) [21][22]. Для фокусированного УЗИ СА и БА необходимы дополнительная разработка и конкретизация по количеству исследований, выполненных самостоятельно и под наблюдением преподавателя, являющегося специалистом в области ультразвуковой диагностики заболеваний сосудов. Соблюдение этих требований позволит избежать как гипердиагностики, так и недооценки существующих у пациента изменений сосудистой стенки.
Общие принципы проведения фокусированного УЗИ СА и БА
Фокусированное УЗИ СА
Специальная предварительная подготовка пациента к проведению фокусированного УЗИ СА не требуется. Исследование проводится в положении пациента лежа на спине.
Данный протокол включает исследование общих и внутренних СА на всем протяжении с обеих сторон. Исследование СА начинают в области ключицы, затем следуют по ходу общей СА в направлении бифуркации и далее получают изображение внутренней СА. Исследование проводится в 2-х продольных (переднем и латеральном) и поперечном сечениях с использованием В-режима и режима цветового допплеровского картирования. Использование режима цветового допплеровского картирования необходимо для выявления АСБ низкой эхогенности или АСБ с преобладанием компонентов низкой эхогенности.
Задачами фокусированного УЗИ СА являются:
- выявление факта наличия АСБ,
- измерение максимального стеноза СА,
- измерение максимальной высоты АСБ из всех выявленных АСБ.
Согласно Манхеймскому консенсусу 2011г, АСБ — это (1) структура, выступающая в просвет артерии на 0,5 мм или 50% по сравнению с величиной ТИМ прилегающих участков стенки сосуда, или (2) структура, выступающая в просвет сосуда более чем на 1,5 мм [25]. Согласно рекомендациям ASE 2020г, о наличии АСБ можно сделать выводы: (1) если имеется любое очаговое утолщение, предположительно атеросклеротического генеза, проникающее в просвет любого сегмента СА (АСБ выпуклого типа), (2) в случае диффузного атеросклероза стенки сосуда, когда ТИМ СА составляет ≥1,5 мм на протяжении СА (АСБ диффузного типа) [13]. Градация АСБ в зависимости от формы и толщины представлена на рисунке 1.

Рис. 1 Градация АСБ в зависимости от формы и толщины (Адаптировано из Johri AM, et al. (2020) [13].
Примечание: АСБ — атеросклеротическая бляшка.
При обнаружении АСБ (или подозрении на наличие АСБ) необходимо определить толщину стенки сосуда. Измерение проводят в продольном сечении, при этом курсор устанавливают на внутренний край (по отношению к просвету артерии) первой гиперэхогенной линии (линия раздела сосуд-кровь) и на внутренний край второй гиперэхогенной линии (линия раздела адвентиция-медиа) (рисунок 2). Отрезок, образованный между двумя точками, должен проходить под прямым углом к касательной к внешнему контуру артерии сосуда. Измерение высоты АСБ проводят вдоль самого выступающего участка бляшки. В заключение фокусированного УЗИ СА вносят максимальное значение из всех максимальных высот имеющихся у пациента АСБ. Пример протокола фокусированного УЗИ СА представлен на рисунке 3.
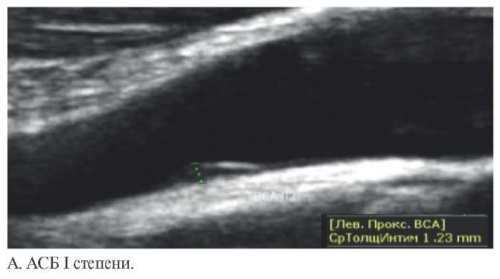
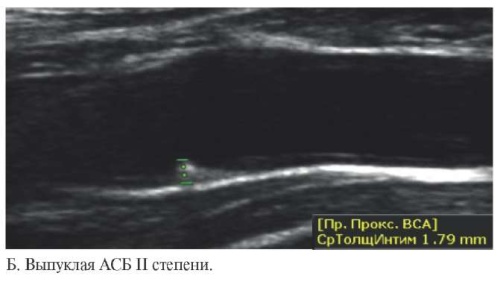
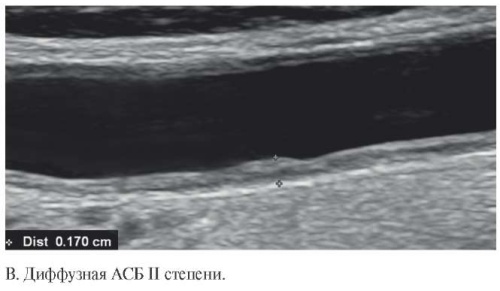
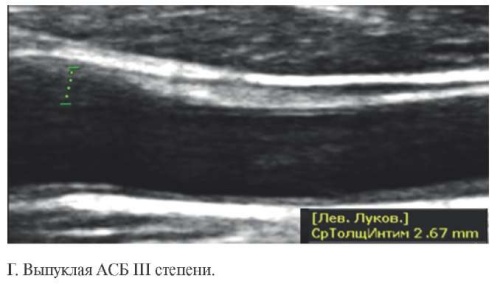
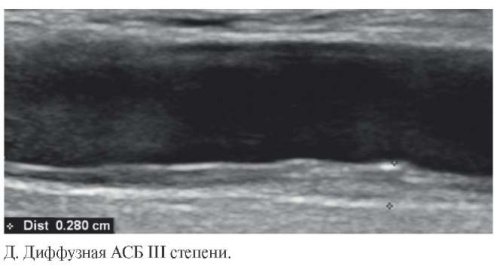
Рис. 2 Ультразвуковое изображение АСБ различных типов (А-Д, каллипером указана высота АСБ).

Рис. 3 Пример протокола фокусированного УЗИ СА.
Стеноз артерий при фокусированном УЗИ рекомендуется оценивать согласно ECST (European Carotid Surgery Trial) [17] (рисунок 4), т.е. непосредственно в зоне максимального развития атеромы, т.к. основной целью фокусированного УЗИ артерий является скрининг на наличие АСБ и оценка ССР, т.е. выявление в первую очередь АСБ с невысокой степенью стеноза. Согласно ESCT стеноз рассчитывается по формуле (С-B)/Сх100%, где С – внешний диаметр артерии в месте максимального сужения просвета АСБ, B — внутренний диаметр артерии в месте максимального сужения просвета АСБ. Измерение стеноза артерии рекомендуется проводить в поперечном сечении (рисунок 5). Метод NASСET, при котором остаточный просвет сосуда в стенозированной области сравнивается с диаметром внутренней СА после постбульбарной области, применяется для оценки степени стеноза во внутренней СА при определении показаний для хирургического вмешательства, а в этом случае пациенту показано проведение стандартного протокола ДС экстракраниального отдела БЦА.
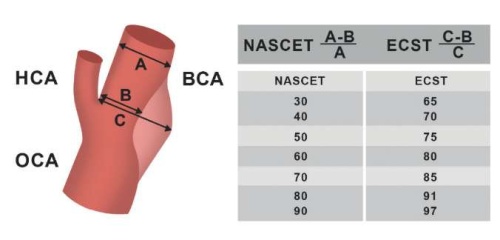
Рис. 4 Способы измерения стеноза СА [22].
Примечание: ВСА — восходящая сонная артерия, НСА — нисходящая сонная артерия, ОСА — общая сонная артерия.
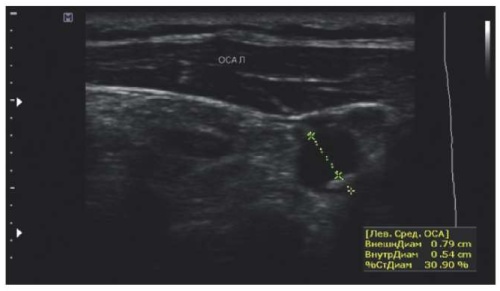
Рис. 5 Пример измерения стеноза общей СА согласно ESCT.
В протоколе фокусированного УЗИ СА следует указать максимальный стеноз СА (в процентах), т.е. наибольшее значение из всех стенозов, образованных имеющимися у пациента АСБ в правой и левой общих и внутренних СА (рисунок 5).
Надо иметь в виду, что место максимального сужения артерии и максимальной высоты АСБ может не совпадать (например, максимальный стеноз может быть получен в области концентрической АСБ, а максимальной по высоте АСБ будет локальная АСБ, располагающаяся вдоль одной из стенок артерии).
Фокусированное УЗИ БА
Специальная предварительная подготовка пациента к проведению фокусированного УЗИ БА не требуется. Исследование проводится в положении пациента лежа на спине.
Данный протокол включает исследование обеих общих БА на всем протяжении и проксимального сегмента (1,5 см) обеих поверхностных БА. Исследование начинают на уровне паховой связки, следуют по ходу общей БА, включая бифуркацию, и далее получают изображение проксимального сегмента поверхностной БА. Исследование проводится в продольном (переднем) и поперечном сечениях с использованием В-режима и режима цветового допплеровского картирования.
Задачами фокусированного УЗИ БА являются [11]:
- выявление факта наличия АСБ,
- измерение максимального стеноза БА.
Ввиду отсутствия отдельных регламентирующих документов в отношении оценки атеросклероза БА, определение АСБ в БА соответствует определению АСБ в СА.
Пример протокола фокусированного УЗИ БА представлен на рисунке 6.

Рис. 6 Пример протокола фокусированного УЗИ БА.
В случае технической сложности выполнения УЗИ СА и БА (затрудненная визуализация, наличие ультразвуковой тени в результате кальциноза и т.п.) пациент должен быть направлен на УЗИ по соответствующему стандартному протоколу, которое выполняется врачом ультразвуковой или функциональной диагностики.
Применение фокусированного УЗИ СА и БА
Учитывая рекомендации 2019г по ведению пациентов с дислипидемиями ESC и EAS [12], Российские рекомендации 2020г по диагностике и коррекции нарушений липидного обмена с целью профилактики и лечения атеросклероза [11], а также рекомендации 2020г по ультразвуковой оценке АСБ СА ASE [13], результаты фокусированного УЗИ СА и БА могут быть использованы для оценки ССР.
Важно заметить, что наличие любой АСБ как в СА, так и БА свидетельствует об атеросклеротическом процессе, и выявление атеросклероза любой степени выраженности ввиду его системного характера должно заставлять врача думать о вероятности наличия более высокого ССР, чем тот риск, который получен на основании фокусированного исследования СА и БА. Для уточнения риска необходим учет всех имеющихся ФР и модификаторов риска, а также контроль выраженности атеросклероза СА и БА в динамике. На данный момент аргументированно говорить о повышении риска возможно при выявлении АСБ в СА высотой ≥1,5 мм и/или с максимальным стенозом ≥25% или при выявлении АСБ в БА с максимальным стенозом ≥25% [11][13]. Можно предположить, что в более старшем возрасте атеросклероз малых градаций менее значим для оценки ССР. Однако четких научных данных о связи выраженности атеросклероза с ССР в зависимости от возраста нет.
Показания для проведения фокусированного УЗИ СА и БА:
- лица с низким или умеренным ССР в возрасте 40 лет и старше;
- лица в возрасте младше 40 лет, но с ФР (например, артериальная гипертензия, гиперхолестеринемия (общий холестерин >8 ммоль/л, холестерин липопротеидов низкой плотности >4,9 ммоль/л), отягощенный семейный анамнез и т.д.). Выраженная гиперхолестеринемия сама по себе указывает на наличие у пациента высокого ССР, результаты фокусированного УЗИ артерий могут привести к необходимости в переклассификации пациента в категорию очень высокого ССР;
- лица с высоким ССР в возрасте 40 лет и старше (как скрининговый метод для уточнения наличия и степени выраженности периферического атеросклероза).
Алгоритм принятия решений на основании результатов фокусированного УЗИ СА (рисунок 7):
- При отсутствии АСБ в СА пациенту должно быть рекомендовано повторное фокусированное УЗИ СА через 3 года.
- При наличии АСБ толщиной <1,5 мм и максимальном стенозе <25% полученные результаты УЗИ не влияют на стратификацию риска, пациенту должно быть рекомендовано повторное фокусированное УЗИ СА через 2 года.
- При наличии АСБ толщиной ≥1,5 мм и максимальном стенозе <25% у пациента как минимум высокий ССР.
- При наличии АСБ толщиной ≥1,5 мм, но <2,5 мм и максимальном стенозе <50% повторное фокусированное УЗИ СА рекомендуется проводить через 1 год, при отсутствии динамики атеросклеротического процесса частоту исследований можно сократить до 1 исследования в 2-3 года. При высоте АСБ ≥2,5 мм и стенозе <50% пациенту должно быть рекомендовано проведение стандартного ДС экстракраниального отдела БЦА с оценкой эхогенности выявленных АСБ, которое следует повторить через 1 год, при отсутствии динамики повторять 1 раз в 2-3 года.
- При выявлении максимального стеноза ≥50% (вне зависимости от высоты АСБ) пациента следует отнести к категории очень высокого ССР и направить на проведение стандартного ДС экстракраниального отдела БЦА (с оценкой эхогенности выявленных АСБ) с последующей ежегодной оценкой, частоту которой можно сократить до 1 раза в 2-3 года при отсутствии динамики атеросклеротического процесса. При появлении клинической симптоматики (транзиторной ишемической атаки или острого нарушения мозгового кровообращения) проводится стандартное ДС экстракраниального отдела БЦА в момент ее развития и далее в зависимости от принятого клинического решения.
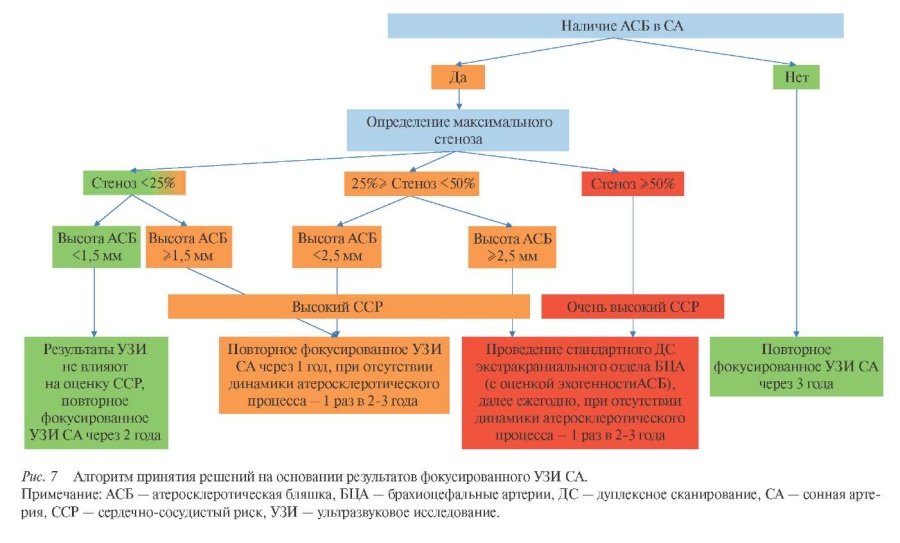
Рис. 7 Алгоритм принятия решений на основании результатов фокусированного УЗИ СА.
Примечание: АСБ — атеросклеротическая бляшка, БЦА — брахиоцефальные артерии, ДС — дуплексное сканирование, СА — сонная артерия, ССР — сердечно-сосудистый риск, УЗИ — ультразвуковое исследование.
Алгоритм принятия решений на основании результатов фокусированного УЗИ БА (рисунок 8):
- При отсутствии АСБ в БА пациенту должно быть рекомендовано повторное фокусированное УЗИ БА через 3 года.
- При наличии максимального стеноза <25% полученные результаты УЗИ не влияют на стратификацию риска, пациенту должно быть рекомендовано повторное фокусированное УЗИ БА через 2 года.
- При наличии максимального стеноза 2549% пациента следует стратифицировать в категорию высокого ССР, при этом повторное фокусированное УЗИ БА должно быть проведено через 1 год, при отсутствии динамики атеросклеротического процесса частоту исследований возможно снизить до 1 раза в 2-3 года.
- При выявлении максимального стеноза ≥50% пациента следует отнести к категории очень высокого ССР и направить на стандартное ДС артерий нижних конечностей с последующей ежегодной оценкой, частоту которой можно сократить до 1 раза в 2-3 года при отсутствии динамики атеросклеротического процесса.
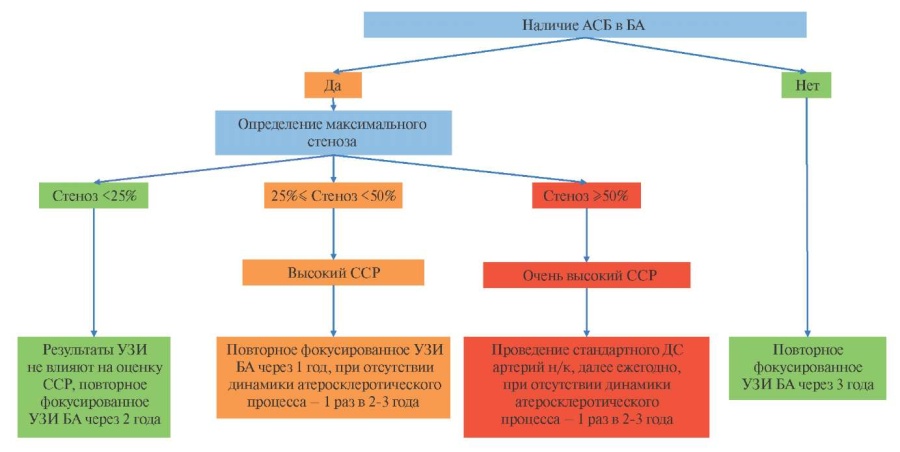
Рис. 8 Алгоритм принятия решений на основании результатов фокусированного УЗИ БА.
Примечание: АСБ — атеросклеротическая бляшка, БА — бедренные артерии, БЦА — брахиоцефальные артерии, ДС — дуплексное сканирование, ССР — сердечно-сосудистый риск, УЗИ — ультразвуковое исследование.
Результаты фокусированного УЗИ СА и БА должны быть оценены врачом-кардиологом. После консультации врача-кардиолога ССР может быть пересмотрен в большую сторону с учетом ФР и модификаторов риска.
Широкое внедрение фокусированного протокола УЗИ в клиническую практику позволит значительно сократить время обследования и повысить экономическую эффективность ранней диагностики атеросклероза, а также увеличить выявляемость лиц высокого ССР. Важным аспектом применения фокусированного протокола УЗИ СА и БА являются тщательность проведения исследования и выполнение только после специальной подготовки и сдачи соответствующих теоретического и практического экзаменов.
ФОКУСИРОВАННОЕ УЗИ БРЮШНОГО ОТДЕЛА АОРТЫ
Место фокусированного УЗИ брюшного отдела аорты
ДС (УЗИ) брюшного отдела аорты является методом выбора выявления и наблюдения за АБА у асимптомных пациентов. Специфичность и чувствительность ДС брюшного отдела аорты в выявлении АБА у асимптомных больных достигает 100% [26][27]. АБА — расширение участка аорты ≥3 см, обусловленное патологическим изменением соединительнотканных структур её стенок вследствие атеросклеротического процесса, воспалительного поражения, врождённой неполноценности или механических повреждений аортальной стенки. Большинство АБА протекают бессимптомно до момента разрыва. Риск разрыва в значительной степени зависит от размера АБА. При разрыве АБА риск смерти достигает 81% [28].
Чаще всего АБА развивается у мужчин. Метаанализ четырех рандомизированных исследований (>125 тыс. чел.) показал, что распространенность АБА среди мужчин старше 65 лет составляет в среднем 5,5% [29]. По данным систематического обзора 26 клинических исследований, распространенность АБА в общей популяции в Западной Европе составляет в среднем 244 случая на 100 тыс. населения, в Восточной Европе — 173 случая на 100 тыс. населения [29]. Наиболее часто АБА встречаются в возрасте 60-70 лет. Если размер АБА к 70-летнему возрасту не превышает 2,5 см, вероятность развития клинически значимой АБА очень мала [30].
В США скрининг мужчин в возрасте 65-75 лет был включен в национальную программу медицинского страхования “Медикэр” [31]. За 10 лет существования программы скрининга АБА в одном из штатов было обследовано 19649 человек, среди которых АБА была выявлена у 1232 (6,3%) пациентов.
Точных данных о распространенности АБА в России нет из-за бессимптомного течения, отсутствия обязательного скрининга и популяционных исследований на предмет наличия АБА.
Согласно результатам метаанализа 2010г, скрининг АБА у мужчин >65 лет связан с достоверным снижением риска смерти, ассоциированной с АБА, в течение ближайших 10 лет на 45% (р<0,05) [32]. В проведенном в Великобритании исследовании MASS (Multicentre Aneurysm Screening Study), результаты которого были опубликованы в 2012г, скрининг АБА у всех мужчин 65-74 лет был связан со снижением риска смерти, ассоциированной с АБА, на 42%, разрыва АБА — на 43%, смерти от всех причин — на 3% (р<0,05 для всех) [33]. По данным метаанализа 2019г (>175 тыс. мужчин >65 лет), скрининг АБА также приводил к значимому снижению риска смерти от всех причин на 3% и смерти, связанной с АБА, на 35% [34].
Американская коллегия кардиологов (ACC) и Американская ассоциация сердца (AHA) совместно рекомендуют однократный скрининг на АБА, включающий физикальный осмотр и УЗИ, у когда-либо куривших мужчин в возрасте от 65 до 75 лет или у мужчин 60 лет и старше, являющихся родственниками (братьями, сестрами или детьми) человека с АБА, и не рекомендуют скрининг на АБА у никогда не куривших мужчин или у женщин [35]. Американское общество сосудистой хирургии (Society for Vascular Surgery) рекомендует однократное УЗИ на наличие АБА всем мужчинам в возрасте от 65 до 75 лет с курением в анамнезе, мужчинам 55 лет и старше с семейным анамнезом АБА, а также женщинам 65 лет и старше, курящим или имеющим семейный анамнез АБА [36].
Согласно ESC, скрининг на наличие АБА с помощью УЗИ рекомендован всем мужчинам в возрасте старше 65 лет (класс рекомендаций — I, уровень доказательности — А), желательно проводить родственникам первой степени родства лиц с АБА (класс рекомендаций — IIa, уровень доказательности — B), можно рассмотреть у женщин старше 65 лет с курением в анамнезе (класс рекомендаций — IIb, уровень доказательности — C) и не рекомендован женщинам, ранее не курившим и не имеющим родственников с АБА [37].
Рекомендации Европейского общества сосудистой хирургии (ESVS) 2019г также рекомендуют скрининг АБА всем мужчинам ≥65 лет, а также мужчинам и женщинам старше 50 лет, имеющим родственников первой степени родства с АБА, с периодичностью каждые 10 лет (класс рекомендаций — IIb, уровень доказательности — C) [38]. Женщинам без отягощенного семейного анамнеза по АБА скрининг не рекомендован (класс рекомендаций — III, уровень доказательности — B).
Клинические рекомендации Национального института здоровья и клинического совершенствования (National Institute for Health and Care Excellence (NICE)) 2020г также рекомендуют скрининг АБА всем мужчинам 66 лет и старше, а кроме того и женщинам ≥70 лет при наличии хотя бы одного из таких ФР, как хроническая обструктивная болезнь легких, курение когда-либо в жизни, атеросклеротическое заболевание коронарных, церебральных или периферических артерий, АГ, гиперлипидемия, отягощенный семейный анамнез в отношении АБА6.
USPSTF в 2019г выпустила рекомендации, согласно которым однократный скрининг на АБА с помощью УЗИ рекомендован всем когда-либо курившим мужчинам в возрасте от 65 до 75 лет [9]. USPSTF рекомендует избирательный скрининг на АБА у никогда не куривших мужчин в возрасте от 65 до 75 лет и не рекомендует рутинный скрининг на АБА у женщин, никогда не куривших и не имеющих в семейном анамнезе АБА. USPSTF приходит к выводу, что недостаточно данных для оценки баланса между преимуществами и вредом скрининга на АБА с помощью УЗИ у женщин в возрасте от 65 до 75 лет, которые когда-либо курили либо имели АБА в семейном анамнезе. Основными ФР развития АБА считаются пожилой возраст, мужской пол, курение и семейный анамнез АБА [9]. Кроме того, диаметр брюшной аорты прямо коррелирует с количеством сердечно-сосудистых ФР и распространенностью атеросклеротического поражения периферических артерий, а наличие ИБС связано с увеличением риска наличия АБА в 2,29 раза (p<0,0001) [39][40]. С другой стороны, диаметр брюшной аорты при отсутствии АБА может являться самостоятельным маркером атеросклеротического поражения других сосудистых бассейнов [41].
Согласно рекомендациям Американского института ультразвуковой диагностики в медицине (American Institute of Ultrasound in Medicine (AIUM)) 2021г [42], скрининг на АБА показан: 1) когда-либо курившим мужчинам в возрасте 65 лет и старше; 2) женщинам в возрасте 65 лет и старше с ФР ССЗ; 3) лицам в возрасте 50 лет и старше с семейным анамнезом аневризмы аорты и/или периферических артерий; 4) лицам с наличием аневризмы периферических артерий; 5) лицам с другими ФР АБА. При диаметре аорты 3,0-3,9 см AIUM рекомендует контрольное УЗИ брюшного отдела аорты каждые 3 года, при диаметре аорты 4,0-4,9 см ежегодно, при диаметре 5,0-5,4 см — каждые 6 мес. [42].
ДС брюшного отдела аорты в нашей стране традиционно выполняют врачи ультразвуковой или функциональной диагностики. Проведение скринингового УЗИ на предмет диагностики АБА группам риска возможно в рамках стандартного УЗИ брюшного отдела аорты. При соответствующей оснащенности и после специального обучения врачи-кардиологи на амбулаторном приеме также могут проводить скрининговое УЗИ аорты, но по фокусированному протоколу. В таблице 2 представлено сравнение стандартного и фокусированного скринингового УЗИ брюшного отдела аорты на предмет диагностики АБА.
Таблица 2
Сравнительная оценка стандартного и фокусированного скринингового УЗИ брюшного отдела аорты на предмет диагностики АБА

Примечание: УЗИ — ультразвуковое исследование.
Общие принципы проведения фокусированного УЗИ на выявление АБА
Скрининговое фокусированное УЗИ брюшного отдела аорты осуществляют после 8-12-ч голодания. Исследование проводят с помощью конвексного датчика с примерным диапазоном частот 2-5 МГц в B-режиме с использованием цветового допплеровского картирования. Однако у пациентов с низкой массой тела возможно визуализировать аорту и линейным датчиком. При скрининговом фокусированном УЗИ брюшного отдела аорты необходимо исследовать аорту на участке от диафрагмы до бифуркации в продольном и поперечном срезах, в протоколе необходимо отразить качество визуализации супраренального и инфраренального отделов аорты. При затруднении визуализации какого-либо отдела аорты необходимо повторить исследование после тщательной подготовки, оптимальным будет направление такого пациента к врачу ультразвуковой или функциональной диагностики. При хорошем качестве визуализации измеряется передне-задний диаметр брюшного отдела аорты в поперечном сечении между наружными контурами стенки в месте максимального расширения (рисунок 9). В протоколе скринингового фокусированного УЗИ брюшного отдела аорты следует указать максимальный диаметр из всех полученных измерений (рисунок 10).
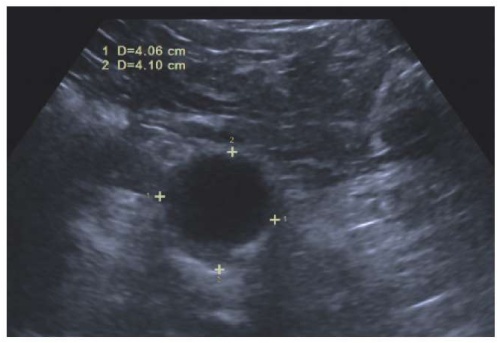
Рис. 9 Ультразвуковое изображение аневризмы брюшного отдела аорты (B-режим, поперечное сечение).

Рис. 10 Пример протокола скринингового фокусированного УЗИ на выявление АБА.
Применение скринингового фокусированного УЗИ на выявление АБА
Однократное скрининговое фокусированное УЗИ на выявление АБА рекомендуется:
- всем когда-либо курившим мужчинам в возрасте от 65 до 75 лет;
- мужчинам и женщинам в возрасте от 65 до 75 лет, являющимся родственниками первой степени родства больных с АБА.
“Когда-либо куривший” — это лицо, выкурившее 100 и более сигарет [36].
Ультразвуковое заключение “АБА” делают при расширении аорты ≥3 см [9][38][42]. При отсутствии адекватной визуализации аорты на протяжении или при выявлении диаметра брюшного отдела аорты ≥3 см пациента следует направить на проведение ДС брюшного отдела аорты по стандартному протоколу, которое будет осуществлять врач ультразвуковой или функциональной диагностики. При проведении скринингового фокусированного УЗИ на выявление АБА врачами ультразвуковой и функциональной диагностики они могут на месте расширить фокусированный протокол до стандартного, который включает в себя оценку протяженности аневризмы (в т.ч. распространение на грудную аорту или общие подвздошные артерии), расслоения, заполнения крупных висцеральных ветвей аорты из истинного или ложного просветов, наличие тромботических масс, состояния окружающих тканей и др.
Интерпретация результатов исследования может отличаться у женщин, а также у мужчин небольшого роста, когда расширением аорты будет считаться превышение диаметра аорты в 1,5 раза по сравнению с близлежащим участком [42].
ФОКУСИРОВАННОЕ УЗИ ВЕН НИЖНИХ КОНЕЧНОСТЕЙ
Место фокусированного УЗИ вен нижних конечностей
ТГВ нижних конечностей является основной причиной ТЭЛА [43]. По результатам метаанализа 13 исследований, объединивших данные о 10002 пациентах, распространенность ТГВ нижних конечностей у лиц с клиническими признаками, указывающими на вероятное наличие тромбоза, составила 19%. При этом у пациентов с высокой претестовой вероятностью ТГВ нижних конечностей выявляли ТГВ в 36-62% случаев. Тромбоз поверхностных вен у пациентов с ТГВ нижних конечностей и/или ТЭЛА выявляли примерно в 10% случаев [44].
Ежегодно в США регистрируются ~900 тыс. случаев венозных тромбоэмболических осложнений, от 150 тыс. до 250 тыс. госпитализаций, связанных с ТЭЛА, и от 60 тыс. до 100 тыс. случаев смерти, что делает ТЭЛА третьей по частоте причиной ССЗ [45]. Ежегодно в развитых странах Европы и Северной Америки регистрируется 39115 новых случаев ТЭЛА и 35-115 случаев ТГВ на 100 тыс. взрослого населения. Вероятность развития венозных тромбоэмболических осложнений закономерно увеличивается по мере старения. Так, в старческом возрасте (≥80 лет) частота венозных тромбоэмболических осложнений в 8 раз выше по сравнению с более молодыми (50-60 лет) [46].
В России наглядные эпидемиологические данные получены в г. Барнауле, где ежегодная частота госпитализируемых c венозными тромбоэмболическими осложнениями составляет 65,5 случая на 100 тыс. населения в год. В структуре госпитализации больных с венозными тромбоэмболическими осложнениями увеличивается число случаев ТЭЛА промежуточного и высокого рисков и растет количество больных с сафено-феморальным тромбозом [47].
Выделяют следующие виды тромбоза: обтурирующий, пристеночный, флотирующий. Данные об эмболоопасности флотирующих тромбов противоречивы. Согласно Гольдиной И. М. и др. (2014), только 55% тромбов в глубоких венах нижних конечностей являются эмболоопасными [48]. Знание о наличии флотации и длине свободной головки тромба может использоваться для индивидуальной оценки показаний к дополнительным вмешательствам после начала лечения антикоагулянтами [45]. Выявление флотирующих тромбов и метрическая оценка длины свободной головки тромба требует проведения стандартного УЗИ вен нижних конечностей врачом ультразвуковой или функциональной диагностики.
Современные рекомендации большинства клинических сообществ позиционируют УЗИ как метод первой линии в диагностике ТГВ и косвенный метод подтверждения ТЭЛА (при выявлении проксимального ТГВ нижних конечностей у больных с клиническим подозрением на наличие ТЭЛА) [8][47][48]. Исследование рекомендуется проводить пациентам с клиническим подозрением на наличие ТГВ нижних конечностей, пациентам с клиническим подозрением на наличие ТЭЛА (когда компьютерная томография-ангиопульмонография недоступна, противопоказана или ее отрицательный результат противоречит клинической симптоматике, характерной для ТЭЛА). Дополнительным аргументом в пользу выполнения УЗИ вен нижних конечностей может быть повышенная концентрация Д-димера в крови. Во время беременности у женщин повышается Д-димер, что делает УЗИ вен нижних конечностей наиболее значимым тестом у этой категории пациенток. При подозрении на венозный тромбоз УЗИ вен нижних конечностей является методом выбора. Важна роль повторного УЗИ при подозрении на рецидив или прогрессирование ТГВ. УЗИ вен нижних конечностей рекомендуется также проводить перед завершением терапии антикоагулянтами для получения диагностических критериев, на основании которых возможно выявление рецидива ТГВ, а также при поиске аргументов в пользу продления использования антикоагулянтов в случаях, когда оптимальная длительность лечения проксимального ТГВ нижних конечностей у конкретного больного неясна [8][47].
В рекомендованный в России объем УЗИ вен нижних конечностей обязательно должно входить исследование поверхностных и глубоких вен не только симптомной, но и контралатеральной конечности для исключения симультанного тромбоза, часто протекающего бессимптомно. Глубокие вены обеих нижних конечностей осматривают на всем протяжении, начиная от дистальных отделов голени до уровня паховой связки, а если не препятствует кишечный газ, то исследуют сосуды илиокавального сегмента [47]. Диагностическими критериями ТГВ являются несжимаемость вены, которую оценивают в поперечном сечении, и/или прямая визуализация тромба в просвете вены. Выполненное врачом ультразвуковой или врачом функциональной диагностики стандартное исследование позволяет выявить такие клинически значимые признаки тромбоза, как локализация, подвижность, размер, состояние головки тромба. Выполнение стандартного протокола предпочтительнее, если позволяет клиническая ситуация — пациент стабилен. Если состояние больного нестабильно, наличие или отсутствие проксимального тромбоза должно быть оценено незамедлительно (для максимально быстрого назначения патогенетической терапии, оптимальной маршрутизации пациента). При невозможности привлечь профильного специалиста в круглосуточном режиме, возможно проведение фокусированного УЗИ вен нижних конечностей [8][48] (таблица 3). Согласно согласованному документу рабочих групп Европейского общества кардиологов по аорте, периферическому кровообращению, малому кровообращению и функции правого желудочка, фокусированный протокол может включать только 2 области исследования с каждой стороны: общие бедренные и подколенные вены [8]. Согласно консенсусу Общества радиологов в области ультразвуковой диагностики (Society of Radiologists in Ultrasound Consensus Conference), фокусированный протокол УЗИ вен нижних конечностей может включать как 2 области исследования с каждой стороны (первая область — общие бедренные вены на 1-2 см выше и ниже сафенофеморального соустья, вторая область — подколенные вены до слияния вен голени), так и иметь расширенный формат (УЗИ от общей бедренной вены через бедренную вену и подколенную вену до слияния вен голени) [48]. По данным метаанализа 100 исследований 2005г, УЗИ проксимальных (бедренных и подколенных) глубоких вен нижних конечностей обладает чувствительностью 94,2%, тогда как для дистальных сегментов (на голени) — 63,5% при общей специфичности 93,8%. Использование цветового допплеровского картирования повышает чувствительность (до 96,4% и 75,2%, соответственно), но снижает специфичность (до 94,3%) [49]. По данным метаанализа 16 исследований 2013г, чувствительность и специфичность фокусированного ультразвукового протокола в отношении выявления проксимального тромбоза составили 96,1% и 96,8%, соответственно [50].
Таблица 3
Сравнительная оценка стандартного и фокусированного УЗИ вен нижних конечностей

Примечание: ТГВ — тромбоз глубоких вен, ТЭЛА — тромбоэмболия легочной артерии, УЗИ — ультразвуковое исследование.
Выполнение стандартного УЗИ вен нижних конечностей предпочтительно во всех клинических ситуациях при подозрении на ТГВ, поскольку позволяет оценить структурное состояние и гемодинамику на всем протяжении вен нижних конечностей и определить индивидуальную тактику лечения, включая выбор оптимальной антикоагулянтной терапии и определение потребности в дополнительном инвазивном лечении. Фокусированное УЗИ, включающее исследование проксимального отдела глубоких вен нижних конечностей, в свою очередь, позволяет быстро и своевременно начать терапию антикоагулянтами у пациентов с наиболее опасным, проксимальным, ТГВ (таблица 3). Важность фокусированного УЗИ при подозрении на венозные тромбоэмболические осложнения подчеркивает тот факт, что раннее начало терапии антикоагулянтами ассоциируется с достоверным снижением госпитальной и 30-дневной смертности [51].
Следует отметить, что выполнение фокусированного УЗИ вен нижних конечностей клиницистом возможно только после прохождения соответствующего обучения и сдачи теоретического и практического экзаменов.
Общие принципы проведения фокусированного УЗИ вен нижних конечностей
При проведении фокусированного УЗИ вен нижних конечностей рекомендуется динамическое исследование на всем протяжении венозного русла от общей бедренной вены через бедренную вену и подколенную вену до слияния вен голени.
Метод фокусированного УЗИ вен нижних конечностей основан на оценке в серошкальном режиме сканирования сжимаемости просвета вены при компрессии датчиком: стенки здоровой вены полностью спадаются при компрессии, при наличии необтурирующего тромбоза вена сжимается не до конца, обтурирующий тромбоз приводит к несжимаемости вены, при этом в просвете вены могут лоцироваться структуры различной эхогенности (рисунок 11 А). При подозрении на остро возникший тромбоз необходимо дополнить исследование кровотока в режимах цветового или энергетического допплеровского картирования, т.к. острый тромбоз в большинстве случаев имеет пониженную эхогенность (соответствующую по эхогенности свободному просвету вены), а также может обладать податливой структурой, способной сжиматься [48] (рисунок 11 Б). В случае обнаружения признаков флотации, данный факт следует отразить в протоколе (рисунок 12). Отсутствие признаков флотации при фокусированном УЗИ не позволяет исключить наличие флотирующего тромбоза.
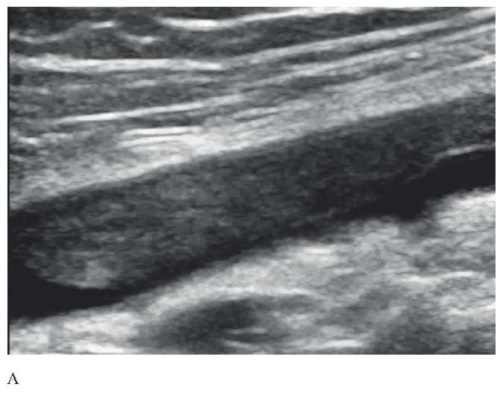
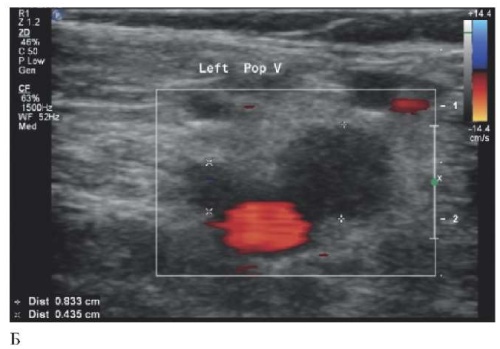
Рис. 11 Ультразвуковое изображение тромбоза левой подколенной вены. А — в просвете лоцируется гетерогенная структура, Б — отсутствие кровотока в режиме цветового допплеровского картирования.
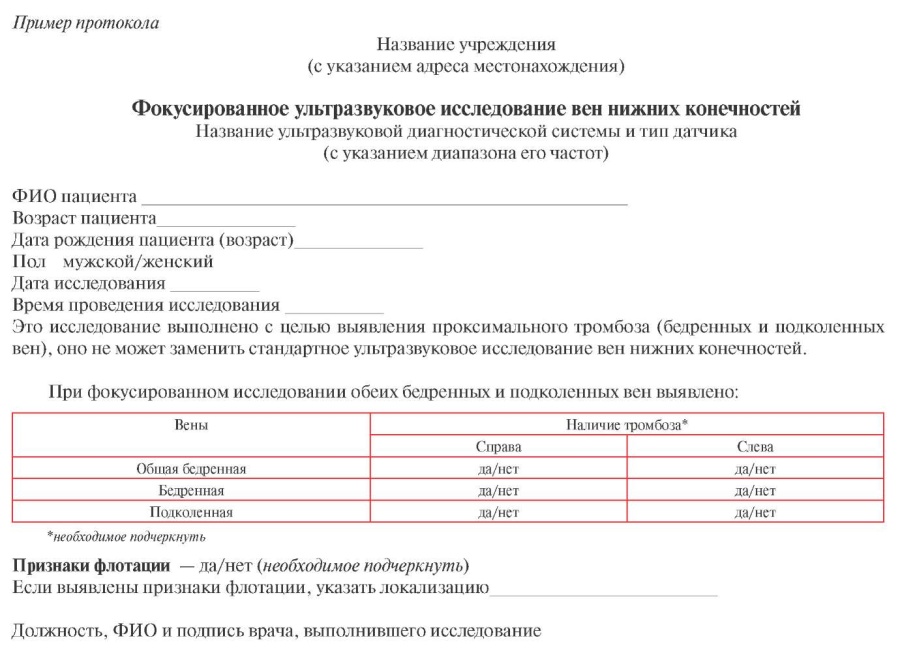
Рис. 12 Пример протокола фокусированного УЗИ вен нижних конечностей.
Применение фокусированного УЗИ вен нижних конечностей
Фокусированное УЗИ вен нижних конечностей показано при клиническом подозрении на ТЭЛА и/или средней или высокой претестовой вероятности ТГВ согласно индексу Wells [47], когда невозможно привлечь профильного специалиста в круглосуточном режиме. Дополнительным аргументом в пользу выполнения фокусированного УЗИ вен нижних конечностей может служить повышенная концентрация Д-димера в крови [52]. Алгоритм определения показаний к фокусированному УЗИ представлен на рисунке 13.
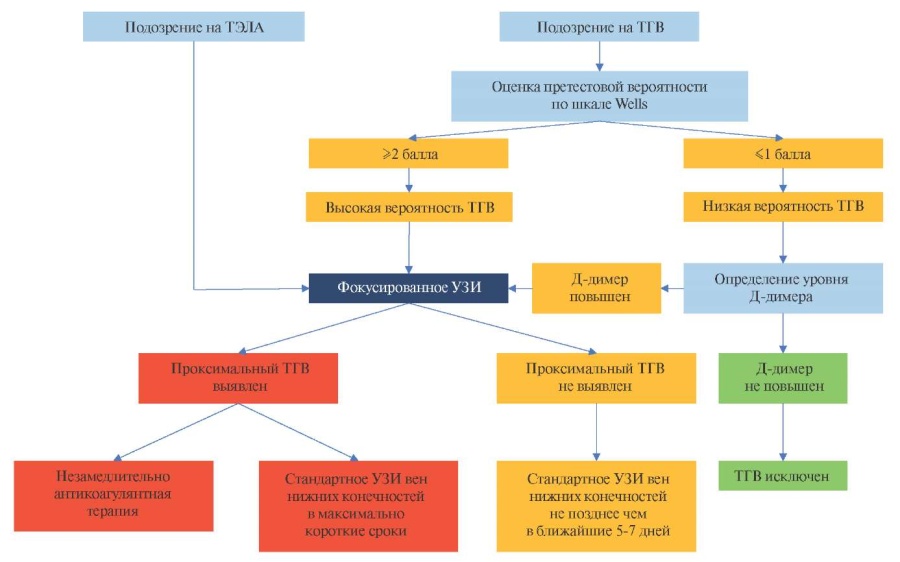
Рис. 13 Алгоритм принятия решений на основании результатов фокусированного УЗИ вен нижних конечностей.
Примечание: ТГВ — тромбоз глубоких вен, ТЭЛА — тромбоэмболия легочной артерии, УЗИ — ультразвуковое исследование.
Выявление проксимального ТГВ при фокусированном исследовании позволяет незамедлительно начать терапию антикоагулянтами с последующим определением тактики ведения пациента. Стандартное УЗИ вен нижних конечностей должно быть выполнено в максимально короткие сроки врачом ультразвуковой или функциональной диагностики. Достоинствами фокусированного протокола УЗИ вен нижних конечностей являются простота и быстрота его выполнения, доступность, высокая чувствительность и специфичность выявления проксимального ТГВ [50]. При отсутствии признаков проксимального ТГВ при фокусированном исследовании требуется проведение стандартного УЗИ вен нижних конечностей врачом ультразвуковой или функциональной диагностики не позднее ближайших 5-7 дней, поскольку фокусировванное УЗИ не позволяет исключить наличие изолированного ТГВ голени [48].
ЗАКЛЮЧЕНИЕ
Фокусированные ультразвуковые протоколы только внедряются в практическое здравоохранение, но уже сейчас, с развитием портативных технологий, расширяют диагностические возможности: позволяют увеличить количество обследованных и способствуют своевременному оказанию помощи. Использование этих протоколов определяет необходимость совершенствования образования врачей в области ультразвуковой диагностики.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Приказ Министерства труда и социальной защиты РФ от 14 марта 2018 г. № 140н “Об утверждении профессионального стандарта “Врач-кардиолог”. https://www.garant.ru/products/ipo/prime/doc/71833356/ (дата обращения 25.06.2021).
2. Приказ Министерства труда и социальной защиты РФ от 27 августа 2018 г. № 554н “Об утверждении профессионального стандарта “Врач — анестезиолог-реаниматолог”. http://www.consultant.ru/document/cons_doc_LAW_306918/ (дата обращения 21.11.21).
3. Приказ Министерства труда и социальной защиты РФ от 14 марта 2018 г. № 140н.
4. ГОСТ Р 56331-2014 “Изделия медицинские электрические. Изделия медицинские ультразвуковые диагностические. Технические требования для государственных закупок”, 2016.
5. Федеральный справочник инструментальных диагностических исследований. https://nsi.rosminzdrav.ru/#!/refbook/1.2.643.5.1.13.13.11.1471 (дата обращения 25.06.2021).
6. Abdominal aortic aneurysm: diagnosis and management. NICE guideline [NG156]. https://www.nice.org.uk/guidance/ng156 (19 March 2020).
Список литературы
1. Neskovic AN, Edvardsen T, Galderisi M, et al. FoСUS cardiac ultrasound: the European Association of Cardiovascular Imaging viewpoint. Cardiovascular Imaging. 2014;15:956-60. doi:10.1093/ehjci/jeu081.
2. Torres-Macho J, Aro T, Bruckner I, et al. Point-of-care ultrasound in internal medicine: A position paper by the ultrasound working group of the European federation of internal medicine. Eur J Intern Med. 2020;73:67-71. doi:10.1016/j.ejim.2019.11.016.
3. Narula J, Chandrashekhar Y, Braunwald E. Time to Add a Fifth Pillar to Bedside Physical Examination: Inspection, Palpation, Percussion, Auscultation, and Insonation. JAMA Cardiol. 2018;3(4):346-50. doi:10.1001/jamacardio.2018.0001.
4. Nielsen MB, Cantisani V, Sidhu PS, et al. The use of handheld ultrasound devices — an EFSUMB position paper. Ultraschall Med. 2019;40:30-9. doi:10.1055/a-0783-2303.
5. Lavenson GS, Pantera RL, Garza RM, et al. Development and implementation of a rapid, accurate, and cost-effective protocol for national stroke prevention screening. The American Journal of Surgery. 2004;188:638-43. doi:10.1016/j.amjsurg.2004.08.055.
6. Johri AM, Calnan CM, Matangi MF, et al. Focused Vascular Ultrasound for the Assessment of Atherosclerosis: A Proof-of-Concept Study. J Am Soc Echocardiogr. 2016;29(9):842-9. doi:10.1016/j.echo.2016.05.003.
7. Балахонова Т. В., Погорелова О. А., Трипотень М. И. и др. Сокращенный протокол ультразвукового дуплексного сканирования сонных артерий в оценке доклинического атеросклероза с целью уточнения сердечно-сосудистого риска. Российский кардиологический журнал. 2019;(5):62-8. doi:10.15829/1560-4071-2019-5-62-68.
8. Mazzolai L, Aboyans V, Ageno W, et al. Diagnosis and management of acute deep vein thrombosis: a joint consensus document from the European Society of Cardiology working groups of aorta and peripheral vascular diseases and pulmonary circulation and right ventricular function. Eur Heart J. 2018;39(47):4208-18. doi:10.1093/eurheartj/ehx003.
9. Owens DK, Davidson KW, Krist AH, et al. Screening for Abdominal Aortic Aneurysm: US Preventive Services Task Force Recommendation Statement. JAMA. 2019;322(22):2211-8. doi:10.1001/jama.2019.18928.
10. Балахонова Т. В., Трипотень М. И., Погорелова О. А. Ультразвуковые методы оценки толщины комплекса интима-медиа артериальной стенки. SonoAce Ultrasound. 2010;21:57-63.
11. Кухарчук В. В., Ежов М. В., Сергиенко И. В. и др. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации, VII пересмотр. Атеросклероз и дислипидемии. 2020;1(38):7-42. doi:10.34687/2219-8202.JAD.2020.01.0002.
12. Mach F, Baigent C, Catapano AL, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020;41(1):111-88. doi:10.1093/eurheartj/ehz455.
13. Johri AM, Nambi V, Naqvi TZ, et al. Recommendations for the Assessment of Carotid Arterial Plaque by Ultrasound for the Characterization of Atherosclerosis and Evaluation of Cardiovascular Risk: From the American Society of Echocardiography. J Am Soc Echocardiogr. 2020;33(8):917-3. doi:10.1016/j.echo.2020.04.021.
14. Krist AH, Davidson KW, Mangione CM, et al. Screening for Asymptomatic Carotid Artery Stenosis: US Preventive Services Task Force Recommendation Statement. JAMA. 2021;325(5):476-81. doi:10.1001/jama.2020.26988.
15. Митьков В. В., Митькова М. Д., Балахонова Т. В. и др. Ультразвуковое исследование сосудов: стандартизация терминологии. Ультразвуковая и функциональная диагностика. 2019;3:12-22. doi:10.24835/1607-0771-2019-3-12-22.
16. Рогоза А. Н., Балахонова Т. В., Чихладзе Н. М. и др. Современные методы оценки состояния сосудов у больных артериальной гипертонией. Пособие для практикующих врачей. М.: Атмосфера, 2008. p. 71. ISBN: 978-5-902123-31-6.
17. Атьков О. Ю., Балахонова Т. В., Горохова С. Г. Ультразвуковое исследование сердца и сосудов. М.: Эксмо, 2015. р. 456. ISBN: 978-5-699-55204-7.
18. Stein JH, Korcarz CE, Hurst RT, et al. Use of carotid ultrasound to identify subclinical vascular disease and evaluate cardiovascular disease risk: a consensus statement from the American society of echocardiography carotid intima-media thickness task force endorsed by the Society for vascular medicine. J Am Soc Echocardiogr. 2008;21:93-111. doi:10.1016/j.echo.2007.11.011.
19. Гучаева Д. А., Трипотень М. И., Погорелова О. А. и др. Эхогенность атеросклеротических бляшек в сонных артериях у больных с острым коронарным синдромом и ее влияние на прогноз сердечно-сосудистых событий. Российский кардиологический журнал. 2019;(5):30-6. doi:10.15829/1560-4071-2019-5-30-36.
20. Бойцов С. А., Драпкина О. М., Калинина А. М. и др. Организация проведения диспансеризации определенных групп взрослого населения. Методические рекомендации по практической реализации приказа Минздрава России от 26 октября 2017 г. №869н “Об утверждении порядка проведения диспансеризации определенных групп взрослого населения”. М.: 2017. c. 162. doi:10.17116/profmed2017medrek01v4.
21. Högberg D, Dellagrammaticasa D, Kragstermana B, et al. Simplified ultrasound protocol for the exclusion of clinically significant carotid artery stenosis. Upsala Journal of Medical Sciences. 2016;121:165-9. doi:10.1080/03009734.2016.1201177.
22. Via G, Hussain A, Wells M, et al. International evidence-based recommendations for focused cardiac ultrasound. Journal of the American Society of Echocardiography. 2014;27:683.e1-683.e33. doi:10.1016/j.echo.2014.05.001.
23. Johri AM, Lajkosz KA, Grubic N, et al. Maximum plaque height in carotid ultrasound predicts cardiovascular disease outcomes: a population-based validation study of the American society of echocardiography’s grade II-III plaque characterization and protocol. Int J Cardiovasc Imaging. 2021. doi:10.1007/s10554-020-02144-5.
24. Mantella LE, Colledanchise K, Bullen M, et al. Handheld versus conventional vascular ultrasound for assessing carotid artery plaque. Int J Cardiol. 2019;278:295-9. doi:10.1016/j.ijcard.2018.12.014.
25. Touboul PJ, Hennerici MG, Meairs S, et al. Mannheim carotid intima-media thickness and plaque consensus (2004-2006-2011). An update on behalf of the advisory board of the 3rd, 4th and 5th watching the risk symposia, at the 13th, 15th and 20th European Stroke Conferences, Mannheim, Germany, 2004, Brussels, Belgium, 2006, and Hamburg, Germany, 2011. Cerebrovasc Dis. 2012;34(4):290-6. doi:10.1159/000343145.
26. Aboyans V, Ricco JB, Bartelink MEL, et al. 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteriesEndorsed by: the European Stroke Organization (ESO) The Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J. 2018;39(9):763-816. doi:10.1093/eurheartj/ehx095.
27. Sparks AR, Johnson PL, Meyer MC. Imaging of abdominal Imaging of abdominal aortic aneurysms. Am Fam Physician. 2002;65(8):1565-70.
28. Reimerink JJ, van der Laan MJ, Koelemay MJ, et al. Systematic review and meta-analysis of population-based mortality from ruptured abdominal aortic aneurysm. Br J Surg. 2013;100(11):1405-13. doi:10.1002/bjs.9235.
29. Sampson UK, Norman PE, Fowkes FG, et al. Estimation of global and regional incidence and prevalence of abdominal aortic aneurysms 1990 to 2010. Glob Heart. 2014;9(1):159-70. doi:10.1016/j.gheart.2013.12.009.
30. Crow P, Shaw E, Earnshaw JJ, et al. A single normal ultrasonographic scan at age 65 years rules out significant aneurysm disease for life in men. Br J Surg. 2001;88(7):941-4. doi:10.1046/j.0007-1323.2001.01822.x.
31. Chun KC, Dolan KJ, Smothers HC, et al. The 10-year outcomes of a regional abdominal aortic aneurysm screening program. J Vasc Surg. 2019;70(4):1123-9. doi:10.1016/j.jvs.2019.01.053.
32. Takagi H, Goto SN, Matsui M, et al. A further meta-analysis of population-based screening for abdominal aortic aneurysm. J Vasc Surg. 2010;52:1103-8. doi:10.1016/j.jvs.2010.02.283.
33. Vallabhaneni SR. Final follow-up of the Multicentre Aneurysm Screening Study (MASS) randomized trial of abdominal aortic aneurysm screening. Br J Surg. 2012;99(12):1656. doi:10.1002/bjs.8941.
34. Ying AJ, Affan ET. Abdominal Aortic Aneurysm Screening: A Systematic Review and Meta-analysis of Efficacy and Cost. Ann Vasc Surg. 2019;54:298-303.e3. doi:10.1016/j.avsg.2018.05.044.
35. Hirsch AT, Haskal ZJ, Hertzer NR, et al. ACC/AHA 2005 guidelines for the management of patients with peripheral arterial disease (lower extremity, renal, mesenteric, and abdominal aortic): executive summary a collaborative report from the American Association for Vascular Surgery/Society for Vascular Surgery, Society for Cardiovascular Angiography and Interventions, Society for Vascular Medicine and Biology, Society of Interventional Radiology, and the ACC/AHA Task Force on Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Patients With Peripheral Arterial Disease) endorsed by the American Association of Cardiovascular and Pulmonary Rehabilitation; National Heart, Lung, and Blood Institute; Society for Vascular Nursing; TransAtlantic Inter-Society Consensus; and Vascular Disease Foundation. J Am Coll Cardiol. 2006 Mar 21;47(6):1239-312. doi:10.1016/j.jacc.2005.10.009.
36. Chaikof EL, Brewster DC, Dalman RL, et al. Society for Vascular Surgery. The care of patients with an abdominal aortic aneurysm: the Society for Vascular Surgery practice guidelines. J Vasc Surg. 2009;50(4)(suppl):S2-S49. doi:10.1016/j.jvs.2009.07.002.
37. Erbel R, Aboyans V, Boileau C, et al. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases: Document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC). Eur Heart J. 2014;35(41):2873-926. doi:10.1093/eurheartj/ehu281.
38. Wanhainen A, Verzini F, Van Herzeele I, et al. 2019 Clinical Practice Guidelines on the Management of Abdominal Aorto-iliac Artery Aneurysms. Eur J Vasc Endovasc Surg. 2019;57(1):8-93. doi:10.1016/j.ejvs.2018.09.020.
39. Glauser F, Mazzolai L, Darioli R, et al. Interaction between widening of diameter of abdominal aorta and cardiovascular risk factors and atherosclerosis burden. Intern Emerg Med. 2014;9(4):411-7. doi:10.1007/s11739-013-0941-y.
40. Altobelli E, Rapacchietta L, Profeta VF, et al. Risk Factors for Abdominal Aortic Aneurysm in Population-Based Studies: A Systematic Review and Meta-Analysis. Int J Environ Res Public Health. 2018;15(12):2805. doi:10.3390/ijerph15122805.
41. Genkel V, Kuznetcova A, Shaposhnik I. Relationship between the abdominal aortic diameter and carotid atherosclerosis in middle-aged patients without established atherosclerotic cardiovascular diseases. Int Angiol. 2021;40(2):131-7. doi:10.23736/S0392-9590.21.04493-X.
42. AIUM Practice Parameter for the Performance of Diagnostic and Screening Ultrasound Examinations of the Abdominal Aorta in Adults. J Ultrasound Med. 2021;40(5):E34-E38. doi:10.1002/jum.15668.
43. Konstantinides SV, Meyer G, Becattini C, et al. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS) The Task Force for the diagnosis and management of acute pulmonary embolism of the European Society of Cardiology (ESC). European Heart Journal. 2020;41:543-603. doi:10.1093/eurheartj/ehz405.
44. Bhatt M, Braun C, Patel P, et al. Diagnosis of deep vein thrombosis of the lower extremity: a systematic review and meta-analysis of test accuracy. Blood Adv. 2020;4(7):1250-64. doi:10.1182/bloodadvances.2019000960.
45. Rivera-Lebron B, McDaniel M, Ahrar K, et al. Diagnosis, Treatment and Follow Up of Acute Pulmonary Embolism: Consensus Practice from the PERT Consortium. Clin Appl Thromb Hemost. 2019;25:1076029619853037. doi:10.1177/1076029619853037.
46. Wendelboe AM, Raskob GE. Global Burden of Thrombosis: Epidemiologic Aspects. Circ Res. 2016;118(9):1340-7. doi:10.1161/CIRCRESAHA.115.306841.
47. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений. Флебология. 2015:4(2): 1-52.
48. Needleman L, Cronan JJ, Lilly MP, et al. Ultrasound for Lower Extremity Deep Venous Thrombosis: Multidisciplinary Recommendations From the Society of Radiologists in Ultrasound Consensus Conference. Circulation. 2018;137(14):1505-15. doi:10.1161/CIRCULATIONAHA.117.030687.
49. Goodacre S, Sampson F, Thomas S, et al. Systematic review and meta-analysis of the diagnostic accuracy of ultrasonography for deep vein thrombosis. BMC Med Imaging. 2005;5:6. doi:10.1186/1471-2342-5-6.
50. Pomero F, Dentali F, Borretta V, et al. Accuracy of emergency physician-performed ultrasonography in the diagnosis of deep-vein thrombosis: a systematic review and meta-analysis. Thromb Haemost. 2013;109(1):137-45. doi:10.1160/TH12-07-0473.
51. Smith SB, Geske JB, Maguire JM, et al. Early anticoagulation is associated with reduced mortality for acute pulmonary embolism. Chest. 2010;137(6):1382-90. doi:10.1378/chest.09-0959.
52. Kakkos SK, Gohel M, Baekgaard N, et al. Editor’s Choice — European Society for Vascular Surgery (ESVS) 2021 Clinical Practice Guidelines on the Management of Venous Thrombosis. Eur J Vasc Endovasc Surg. 2021;61(1):9-82. doi:10.1016/j.ejvs.2020.09.023.
Об авторах
Т. В. БалахоноваРоссия
Балахонова Татьяна В.
Москва.
А. И. Ершова
Россия
Ершова Александр Игоревна.
Москва.
М. В. Ежов
Россия
Ежов Марат В.
Москва.
О. Л. Барбараш
Россия
Барбараш Ольга Л.
Кемерово.
Л. Л. Берштейн
Россия
Берштейн Леонид Л.
Санкт-Петербург.
В. Ю. Богачев
Россия
Богачев Вадим Ю.
Москва.
М. И. Воевода
Россия
Воевода Михаил И.
Новосибирск.
В. В. Генкель
Россия
Генкель Вадим В.
Челябинск.
В. С. Гуревич
Россия
Гуревич Виктор С.
Санкт-Петербург.
Д. В. Дупляков
Россия
Дупляков Дмитрий В.
Самара.
Т. Э. Имаев
Россия
Имаев Тимур Э.
Москва.
Г. А. Коновалов
Россия
Коновалов Геннадий А.
Москва.
Е. Д. Космачева
Россия
Космачева Елена Д.
Краснодар.
К. В. Лобастов
Россия
Лобастов Кирилл В.
Москва.
М. Д. Митькова
Россия
Митькова Мина Д.
Москва.
В. С. Никифоров
Россия
Никифоров Виктор С.
Санкт-Петербург.
О. П. Ротарь
Россия
Ротарь Оксана П.
Санкт-Петербург.
И. А. Сучков
Россия
Сучков Игорь А.
Рязань.
И. С. Явелов
Россия
Явелов Игорь С.
Москва.
В. В. Митьков
Россия
Митьков Владимир В.
Москва.
Р. С. Акчурин
Россия
Акчурин Ренат С.
Москва.
О. М. Драпкина
Россия
Драпкина Оксана М.
Москва.
С. А. Бойцов
Россия
Бойцов Сергей А.
Москва.
Дополнительные файлы
Рецензия
Для цитирования:
Балахонова Т.В., Ершова А.И., Ежов М.В., Барбараш О.Л., Берштейн Л.Л., Богачев В.Ю., Воевода М.И., Генкель В.В., Гуревич В.С., Дупляков Д.В., Имаев Т.Э., Коновалов Г.А., Космачева Е.Д., Лобастов К.В., Митькова М.Д., Никифоров В.С., Ротарь О.П., Сучков И.А., Явелов И.С., Митьков В.В., Акчурин Р.С., Драпкина О.М., Бойцов С.А. Фокусированное ультразвуковое исследование сосудов. Консенсус российских экспертов. Кардиоваскулярная терапия и профилактика. 2022;21(7):3333. https://doi.org/10.15829/1728-8800-2022-3333
For citation:
Balakhonova T.V., Ershova A.I., Ezhov M.V., Barbarash O.L., Bershtein L.L., Bogachev V.Yu., Voevoda M.I., Genkel V.V., Gurevich V.S., Duplyakov D.V., Imaev T.E., Konovalov G.A., Kosmacheva E.D., Lobastov K.V., Mitkova M.D., Nikiforov V.S., Rotar O.P., Suchkov I.A., Yavelov I.S., Mitkov V.V., Akchurin R.S., Drapkina O.M., Boytsov S.A. Focused vascular ultrasound. Consensus of Russian experts. Cardiovascular Therapy and Prevention. 2022;21(7):3333. (In Russ.) https://doi.org/10.15829/1728-8800-2022-3333
JATS XML

























































