Перейти к:
Особенности реваскуляризации миокарда и анализ конечных точек через год наблюдения у больных с острыми и хроническими формами ишемической болезни сердца в зависимости от наличия или отсутствия сахарного диабета
https://doi.org/10.15829/1728-8800-2022-3394
Аннотация
Цель. Анализ особенностей реваскуляризации миокарда у больных острой и хронической формами ишемической болезни сердца (ИБС) и с различным гликемическим статусом, а также оценка осложнений через год наблюдения.
Материал и методы. В проспективное сравнительное клиническое исследование включены 202 больных обоего пола с острыми и хроническими формами ИБС. В зависимости от гликемического статуса и формы ИБС больные были распределены в четыре группы: острые формы ИБС и сахарного диабета 2 типа (СД2); острые формы ИБС без СД2 (контрольная группа); хронические формы ИБС и СД2; хронические формы ИБС без СД2 (контрольная группа). В зависимости от клинического состояния и результатов коронарной ангиографии пациентам проводили различные виды реваскуляризации миокарда: баллонная ангиопластика без стентирования, стентирование, коронарное шунтирование, стентирование + коронарное шунтирование. Через год после выписки со всеми пациентами связывались для оценки осложнений и конечных точек, к числу которых относили повторный инфаркт миокарда, острое нарушение мозгового кровообращения, повторную госпитализацию, повторную реваскуляризацию и смерть. Проведена оценка суммарного показателя конечных точек.
Результаты. До 80% больным острыми и хроническими формами ИБС вне зависимости от гликемического статуса была проведена реваскуляризация, в основном — стентирование. Частота стентирования среди лиц без СД2 с острой и хронической формами ИБС была достоверно выше по сравнению с больными СД2. Абсолютное число пациентов с коронарным шунтированием, в т.ч. в сочетании со стентированием было больше в группах с СД2. В группах без СД2 количество пациентов с одним стентом оказалось в 2-2,5 раза выше по сравнению с группами, имеющими СД2 — острые формы ИБС (p=0,041) и хронические формы ИБС (p=0,017). По частоте имплантации ≥2 стентов группы не различались. В течение 1 года после выписки среди лиц с острой и хронической формами ИБС и СД2 наблюдается больше госпитализаций и повторных вмешательств. По количеству нефатальных и фатальных осложнений группы между собой не различались, хотя абсолютные цифры этих показателей оказались выше у больных с СД2. Суммарные показатели конечных точек у лиц с СД2 вне зависимости от формы ИБС были в 2 раза выше по сравнению с соответствующими контрольными группами (p<0,001).
Заключение. Большинство пациентов с острой и хронической формами ИБС вне зависимости от гликемического статуса подверглись реваскуляризации миокарда. У пациентов без СД2 преобладало стентирование, чаще всего одной коронарной артерии. Больным СД2 наряду со стентированием проводилось коронарное шунтирование, а также сочетание этих двух процедур. Через год наблюдения число осложнений у больных СД2 оказалось в 2 раза больше по сравнению с пациентами без СД2, что подчеркивает важность проведения вторичной профилактики, включая комплексную медикаментозную коррекцию.
Ключевые слова
Для цитирования:
Мамедов М.Н., Марданов Б.У., Кокожева М.А., Шукуров Ф.Б., Ахундова Х.Р., Куценко В.А. Особенности реваскуляризации миокарда и анализ конечных точек через год наблюдения у больных с острыми и хроническими формами ишемической болезни сердца в зависимости от наличия или отсутствия сахарного диабета. Кардиоваскулярная терапия и профилактика. 2022;21(10):3394. https://doi.org/10.15829/1728-8800-2022-3394
For citation:
Mamedov M.N., Mardanov B.U., Kokozheva M.A., Shukurov F.B., Akhundova H.R., Kutsenko V.A. Analysis of myocardial revascularization and endpoints after a 1-year follow-up of patients with acute and chronic coronary artery disease, depending on diabetes presence. Cardiovascular Therapy and Prevention. 2022;21(10):3394. (In Russ.) https://doi.org/10.15829/1728-8800-2022-3394
Введение
Сочетание сахарного диабета 2 типа (СД2) с ишемической болезнью сердца (ИБС) является одной из часто встречаемых форм коморбидности в клинической практике [1]. По данным клинико-эпидемиологических исследований за последние годы среди лиц с острой и хронической формами ИБС число больных СД2, в частности, с впервые выявленной ее формой, увеличилось [2][3]. Было отмечено омоложение СД2 [4]. Метаанализ 26 исследований с участием 1325493 человек из 30 стран продемонстрировал, что заболеваемость СД2 в более молодом возрасте ассоциировано с более высоким риском развития осложнений сердечно-сосудистых заболеваний и смерти [5].
В литературе описан ряд клинических проявлений ИБС и функционально-анатомических особенностей сердечно-сосудистой системы при СД2, что обусловлено ролью нарушений углеводного обмена в развитии атеросклероза. Ангиографические исследования показали, что у пациентов с СД2 более вероятно наличие стеноза ствола левой коронарной артерий (ЛКА) и многососудистого поражения коронарного русла с более диффузным поражением мелких ветвей [6][7]. Кроме того, пациенты с СД2 имеют бо́льшую атеросклеротическую нагрузку и повышенное количество богатых липидами бляшек с вероятностью разрыва [8][9]. Среди больных СД2 безболевая ишемия миокарда встречается чаще по сравнению с лицами без нарушений углеводного обмена [10][11].
Для ведения пациентов с СД2 и ИБС разработаны международные клинические рекомендации, которые по мере накопления данных крупных исследований регулярно обновляются. Согласно последним европейским рекомендациям, выполнение реваскуляризации миокарда посредством чрескожного коронарного вмешательства (ЧКВ) или коронарного шунтирования (КШ) более эффективно снижает тяжесть клинических симптомов, уменьшает потребность в антиангинальных средствах, а также улучшает переносимость физических нагрузок и увеличивает качество жизни по сравнению с медикаментозным лечением в краткосрочной и долгосрочной перспективе [12-14]. Прогнозируемая хирургическая смертность, анатомические особенности поражения коронарных артерий (КА) и возможность выполнения полной реваскуляризации являются важными критериями в ходе выбора лечебной тактики между ЧКВ или КШ. Принятие решения о предпочтительном методе лечения (консервативное лечение, ЧКВ или КШ) осуществляется при оценке соотношения риск-польза от вмешательства, уточнении рисков развития перипроцедурных осложнений, а также изменений качества жизни, долгосрочного прогноза в отношении смерти, вероятности развития инфаркта миокарда (ИМ) или потребности в повторной реваскуляризации [15].
Необходимо отметить, что оценка краткосрочного прогноза жизни пациентов также является важным показателем оценки тактики лечения и ее реализации.
Цель настоящего исследования — анализ особенностей реваскуляризации миокарда у больных острой и хронической формами ИБС и с различным гликемическим статусом, а также оценка осложнений через год наблюдения.
Материал и методы
В проспективное сравнительное клиническое исследование были включены 202 больных обоего пола с острыми (ИМ без подъема SТ, нестабильная стенокардия) и хроническими формами ИБС (стабильная ИБС, в т.ч. перенесенным ИМ), госпитализированных в кардиологические отделения НИИ скорой помощи им. Н. В. Склифосовского (г. Москва) с 2018 по 2019гг. В зависимости от гликемического статуса и формы ИБС больные были распределены в четыре группы:
- первая группа (n=50) (средний возраст 56,6±0,96 лет, мужчины/женщины 34/16) — пациенты с острой формой ИБС и СД2;
- вторая (контрольная) группа (n=52) (средний возраст 58,7±1,01 лет, мужчины/женщины 37/15) — пациенты с острой формой ИБС без СД2;
- третья группа (n=49) (средний возраст 57,9±1,04 лет, мужчины/женщины 35/14) — пациенты с хронической формой ИБС и СД2;
- четвертая (контрольная) группа (n=51) (60,2±0,9 лет, мужчины/женщины 34/17) — пациенты с хронической формой ИБС без СД2.
Критерии невключения:
- возраст <35 и >75 лет;
- СД2 1 типа;
- бронхиальная астма и хронические обструктивные заболевания легких с дыхательной недостаточностью I-III ст.;
- заболевания системы кроветворения и коллагенозы;
- онкологические заболевания;
- эндогенные психические заболевания;
- участие в любом другом исследовании в течение 30 дней перед отбором.
Для оценки клинического состояния всем пациентам было проведено анкетирование, осмотр, измерение антропометрических и гемодинамических показателей.
Всем больным проводили электрокардиографию (ЭКГ) в 12-ти стандартных отведениях с помощью аппарата Schiller АТ-10 plus (Швейцария). Холтеровское мониторирование ЭКГ (качественная и количественная оценка нарушений ритма и проводимости, динамики сегмента SТ) проводили с помощью носимых мониторов Schiller МТ — 101 (Швейцария) и "Союз-"ДМС" (Россия). Эхокардиографическое исследование проводили трансторакальным доступом при помощи ультразвукового аппарата Samsung HM70A (Южная Корея) в соответствии с рекомендациями Американской ассоциации эхокардиографии в Ми В-режимах.
С целью визуализации коронарных артерий (КА) для определения тяжести атеросклеротического поражения и выбора оптимальной тактики лечения всем пациентам выполнялась селективная коронарография на ангиографической установке "Allura Xper FD20" (Phillips, Нидерланды) под местной анестезией (0,5% раствора новокаина) по методу М. Judkins путем чрескожной пункции бедренной артерии по S. Seldinger, либо через A. radialis справа.
В зависимости от клинического состояния и результатов коронарной ангиографии пациентам проводились различные виды реваскуляризации: баллонная ангиопластика без стентирования, стентирование (стент с лекарственным покрытием — DES), КШ, стентирование + КШ. Пациентам с острой формой ИБС реваскуляризация проводилась в экстренном порядке, тогда как больным с хронической формой ИБС выполнили процедуру в плановом порядке по факту госпитализации.
Через год после госпитализации со всеми пациентами связывались для оценки осложнений и конечных точек, к числу которых относили:
- повторный ИМ;
- острое нарушение мозгового кровообращения (ОНМК);
- смерть;
- повторную госпитализацию по сердечно-сосудистым событиям;
- повторную реваскуляризацию.
Проведена оценка суммарного показателя конечных точек.
Все пациенты подписали информированное согласие для участия в наблюдательном исследовании. Протокол одобрен локальным этическим комитетом.
Статистический анализ. Ввод данных в региональном исследовательском центре проводился в системе ACCESS MS OFFICE. Статистический анализ проведен при помощи статистического пакета SAS (Statistical Analysis System), а также среды анализа данных R 4.1.2. Распределение считалось близким к нормальному, если отсутствовала асимметричность и мультимодальность гистограммы распределения. Для оценки достоверности различий между двумя группами в случае близости параметра к нормальному распределению использовался t-критерий Стьюдента, в противном случае — критерий Манна-Уитни. Значимость различий качественных показателей определялась с помощью критерия χ2 и точного критерия Фишера. Данные представлены в виде средних (М) значений и ошибок среднего (m). В случае попарных сравнений между группами применена поправка Холма на множественные сравнения. Различия считались достоверными при значениях p<0,05.
Результаты
Клиническая характеристика пациентов, включенных в исследование, представлена в таблице 1. В группе лиц с острым коронарным синдромом (ОКС) при поступлении был выявлен ИМ без подъема сегмента ST, в группе лиц с СД2 у 42% больных, а в группе лиц без СД2 у 19% пациентов (p=0,018). Большинство пациентов в этих группах поступали с нестабильной стенокардией. В группе лиц с СД2 нестабильная стенокардия была выявлена у 58% пациентов, а в группе лиц без СД2 — у 81% пациентов (p=0,046). До 20% пациентов обеих групп отмечали наличие ИМ в анамнезе.
Таблица 1
Формы ИБС у пациентов, госпитализированных в кардиологическое отделение n (%)

Примечание: ИМ — инфаркт миокарда, СД2 — сахарный диабет 2 типа.
В группе лиц с хронической формой ИБС и СД2 у 33% пациентов поводом для госпитализации была стабильная стенокардия, а в группе лиц без СД2 этот показатель составил 50%. В то же время у 45% пациентов с СД2 в анамнезе был ИМ, а в группе лиц без СД2 ИМ был зарегистрирован в 38% случаев. У каждого пятого пациента с СД2 и десятого пациента без СД2 имелся атеросклеротический кардиосклероз. В целом, в группе лиц с хроническими формами ИБС и СД2 частота ИМ в анамнезе была в 2 раза выше по сравнению с острой формой ИБС, что было статистически значимо (p=0,03).
На госпитальном этапе всем пациентам проводилась комплексная лекарственная терапия. В группе с острой формой ИБС и СД2 2/3 пациентов получали сахароснижающую терапию в таблетированной форме. Инсулинотерапия, в т.ч. комбинированная терапия, была назначена каждому четвертому пациенту. Среди лиц с хронической формой ИБС и СД2 сахароснижающую терапию получал каждый второй, тогда как инсулинотерапия, в т.ч. комбинированная терапия, проводилась в 37% случаев. Всем пациентам была назначена антиагрегантная терапия. В случае острой формы ИБС в двух подгруппах все пациенты принимали двойную антиагрегантную терапию. У больных с хронической формой ИБС до 61% пациентов получали двойную антиагрегантную терапию, остальные принимали монотерапию. Бета-блокаторы и ингибиторы ангиотензинпревращающего фермента/ сартаны были назначены во всех группах до 95% случаев, диуретики от 60% (острая форма ИБС без СД2) до 94% (острая форма ИБС и СД2), а антагонисты кальция до 30% случаев. Всем пациентам также были назначены статины.
В ходе проведения коронарной ангиографии было выявлено, что группы с острой формой ИБС с или без СД2 по частоте поражений магистральных КА были сопоставимы. Обнаружено, что стенозы дистальной трети КА у пациентов с СД2 имели место в 2 раза чаще по сравнению с группой без СД2 (78% случаев), а у пациентов без СД2 (42%), эти различия были статистически значимы (р<0,001).
В группах лиц с хронической формой ИБС по частоте гемодинамически значимых поражений основных магистральных КА статистически значимые различия не выявлены. В группе лиц с ИБС и СД2 диффузное многососудистое поражение КА выявлялось достоверно чаще по сравнению с группой без СД2 — 73 и 45%, соответственно (р<0,005).
Необходимо подчеркнуть, что среди пациентов с острой и хронической формами ИБС из методов реваскуляризации преобладало стентирование (в несколько раз больше, чем КШ), сочетание стентирования и шунтирования, а также ангиопластика без стентирования (таблица 2). В группе с острой формой ИБС без СД2 количество процедур стентирования оказалось на 50% больше, чем в группе с СД2, что было статистически значимо — 65 vs 42% (p=0,028). Аналогичная картина отслеживается в группах с хронической формой ИБС. В группе без СД2 в 61% случаев было проведено стентирование, тогда как в группе с СД2 — только в 35% случаев (p=0,01). КШ было выполнено в диапазоне от 6 до 18% пациентов с острыми и хроническими формами ИБС. По частоте этой процедуры достоверных различий между группами не выявлено. В группах лиц с СД2 комбинированное вмешательство (КШ и ЧКВ) проводилось чаще, чем среди пациентов без СД2, однако различие между группами не достигло статистической значимости. В группах с СД2 4-6% пациентам проводилась ангиопластика без стентирования; в контрольных группах эта процедура не применялась. Обращает на себя внимание тот факт, что в каждой группе до 25% случаев не проводилась реваскуляризация миокарда.
Таблица 2
Вид реваскуляризации у пациентов с острыми и хроническими формами ИБС и СД2 (и без СД2)
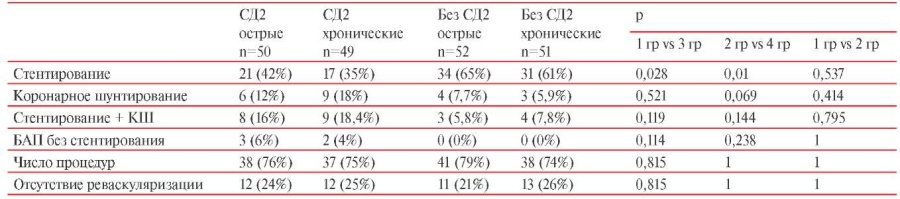
Примечание: БАП — баллонная ангиопластика, КШ — коронарное шунтирование, СД2 — сахарный диабет 2 типа.
Общее количество установленных стентов в группах было сопоставимо (таблица 3). В группах пациентов с острой и хронической формой ИБС без СД2 один стент устанавливался в 2-3 раза чаще по сравнению с группами с СД2; различие было статистически значимо. Группы лиц с острой и хронической формой ИБС и СД2 по частоте установления двух стентов не различалась. Число пациентов с тремя стентами во всех 4-х группах оказалось сопоставимым и, в среднем, составило до 15% случаев. Четыре и пять стентов установлено не более чем у 10% пациентов. В целом, среднее количество стентов во всех группах оказалось сопоставимым, и статистически значимые различия между группами не выявлены.
Таблица 3
Количество стентов у пациентов с острыми и хроническими формами ИБС и СД2 (и без СД2)

Примечание: СД2 — сахарный диабет 2 типа.
Наряду с этим, по причине многососудистого поражения, отказ от КШ и стентирования в группах лиц с острой и хроническими формами ИБС и СД2 наблюдается в 2 раза чаще, чем в группах без СД2 (таблица 4), однако различия не достигли статистической значимости. До 10% в группах с СД2 и до 20% группах без СД2 стенозы встречались у 5060% пациентов, что также служило причиной отказа от процедуры реваскуляризации.
Таблица 4
Пациенты с острыми и хроническими формами ИБС и СД2 (или без СД2) без реваскуляризации n (%)

Примечание: АКШ — аортокоронарное шунтирование, СД2 — сахарный диабет 2 типа, ЧКВ — чрескожное коронарное вмешательство.
Главной задачей настоящего исследования был анализ конечных точек у лиц с острыми и хроническими формами ИБС и СД2 (таблица 5). В обеих группах у лиц с СД2 повторный ИМ выявлен в 2 раза чаще по сравнению с группами без СД2. Частота ОНМК в группах наблюдалась до 5%. Смертельный исход за год в группах пациентов с острой и хронической формами ИБС составил 6%, а в группах без СД2 этот показатель колебался около 2%. У больных с СД2 повторная госпитализация наблюдалась в 2 раза чаще по сравнению с соответствующими контрольными группами. Обращает на себя внимание тот факт, что пациентам с острой и хроническими формами ИБС с СД2 повторная реваскуляризация потребовалась в 3 раза чаще по сравнению с пациентами без СД2. Это различие в группах с острой формой ИБС имеет тенденцию, а в группах с хроническими формами достигает статистической значимости.
Таблица 5
Конечные точки по результатам однолетнего наблюдения за пациентами с острыми и хроническими формами ИБС с различным гликемическим статусом n (%)
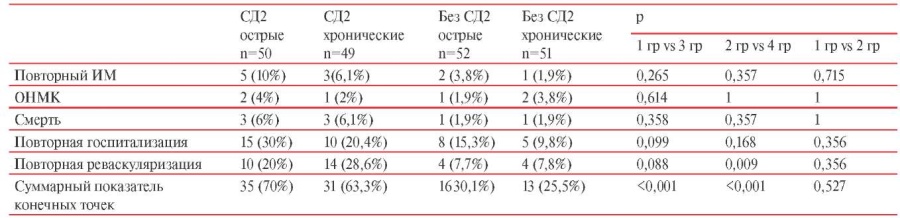
Примечание: ИМ — инфаркт миокарда, ОНМК — острое нарушение мозгового кровообращения, СД2 — сахарный диабет 2 типа.
Суммарный показатель конечных точек в группах с острой и хронической формой ИБС и СД2 оказался в 2,5 раза выше по сравнению с группами лиц без СД2, что в обоих случаях достигло статистической значимости (р<0,001).
Обсуждение
Проспективное сравнительное исследование посвящено изучению особенностей реваскуляризации миокарда и оценке осложнений у лиц с СД2 и различными формами ИБС. В контрольные группы включили пациентов с острыми и хроническими формами ИБС без нарушений углеводного обмена. Такой подход позволяет комплексно изучить проблемы реваскуляризации миокарда и отслеживать краткосрочный прогноз пациентов с сочетанием ИБС и СД2.
Высокая сердечно-сосудистая смертность у лиц с СД2 остается одной из серьезных медико-социальных проблем во многих странах мира. По данным регистра Gulf COAST (многоцентровое исследование в регионе стран Персидского залива) из 3576 пациентов с ОКС у 1906 (53,3%) больных был выявлен СД2. Отмечена достоверно более высокая госпитальная (4,8%), 30-дневная (6,7%) и 1-летняя (13,7%) смертность у больных СД2 по сравнению с пациентами без СД2 [16]. Следовательно, случаи смерти зарегистрированы у каждого десятого пациента с наличием СД2.
Влияние СД2 на отдаленный прогноз больных с ОКС изучалось также в другом проспективном исследовании с участием ~2 тыс. больных. При этом 1/5 часть больных имели установленный ранее СД2; 320 (17%) больных умерли в течение среднесрочного периода наблюдения (3,7 лет). Прогностическая значимость СД2 не зависела от курения, возраста, проведения тромболизиса, вида гипогликемической терапии. Однако риск смерти, ассоциированной с СД2, оказался достоверно выше у лиц женского пола [17].
Необходимо подчеркнуть, что СД2 присутствует у 25-30% пациентов, поступивших с ОКС. А среди пациентов, которым выполнялось КШ, 40% имеют СД2 [18].
Исследования показывают, что после реваскуляризации миокарда снижение абсолютного риска было более выражено у пациентов с СД2, чем у пациентов без СД2. Выбор стратегии реваскуляризации рекомендуется базировать на оценке клиники заболевания, сопутствующей патологии и анатомической тяжести поражения (например, SYNTAX — Synergy between Percutaneous Coronary Intervention with TAXUS and Cardiac Surgery) [19]. В международных рекомендациях предпочтение отдается КШ в качестве метода реваскуляризации для пациентов с СД2 и многососудистым поражением коронарного русла. Тем не менее, наличие тяжелой сопутствующей патологии, пожилой возраст и значение шкалы SYNTAX 0-22 являются показанием к проведению ЧКВ. В настоящее время принято считать, что критерии, применяемые к пациентам со стабильной ИБС при выборе метода реваскуляризации, должны соблюдаться и у стабилизированных пациентов с ОКС без подъема сегмента ST [20].
В настоящем исследовании до 80% больным с острыми и хроническими формами ИБС вне зависимости от наличия СД2 была проведена реваскуляризация миокарда. И в большинстве случаев — это процедура стентирования. Необходимо отметить, что стентирований среди лиц без СД2 с острой и хронической формами ИБС было достоверно выше по сравнению с лицами с СД2. В то же время абсолютное число пациентов с КШ и сочетанием КШ со стентированием было больше в группах лиц с СД2. В группах лиц без СД2 число пациентов с одним стентом оказалось в несколько раз больше по сравнению с группами, имеющими СД2. В то же время по частоте двух и более стентов группы не различались.
Согласно метаанализу 11 рандомизированных исследований с участием 11518 пациентов, ЧКВ (n=5753) или аортокоронарное шунтирование (АКШ) (n=5765) со средним периодом наблюдения 3,8 года, было продемонстрировано, что при АКШ смертность была выше по сравнению с ЧКВ у пациентов с многососудистым поражением (11,5% после ЧКВ vs 8,9% после АКШ, p=0,0019) и у пациентов с СД2 (15,5 vs 10,0%, p=0,0004). У пациентов с поражением ЛКА преимущества КШ перед ЧКВ не наблюдались. Авторы приходят к заключению, что необходимо более длительное наблюдение, чтобы лучше определить различия в смертности между стратегиями реваскуляризации [21].
В финском национальном регистре (20002015гг) проводилось сравнение различных исходов после КШ и ЧКВ у больных с СД2 (24%) по сравнению с лицами без СД2 (76%). На 28-й день риск летального исхода после ЧКВ был ниже, чем после КШ среди пациентов без СД2, тогда как среди пациентов с СД2 разницы не наблюдалось. В долгосрочном наблюдении ситуация была обратной: ЧКВ показало более высокий риск по сравнению с КШ для большинства исходов. В частности, при 3-летнем наблюдении риск смерти от всех причин был повышен среди больных СД2 (отношение рисков (ОР) — 1,30) при сравнении ЧКВ с КШ в большей степени, чем среди пациентов без СД2 (ОР — 1,09). То же самое относится и к сердечно-сосудистой смерти (ОР — 1,29) среди пациентов с СД2 и среди пациентов без СД2 (ОР — 1,03) [22].
В настоящем исследовании большинству пациентов с СД2 была проведена реваскуляризация миокарда, но при этом число отказов от процедур в этих группах имело место в 2 раза чаще по сравнению с пациентами без нарушений углеводного обмена — 15 vs 7%, соответственно.
Через год после госпитализации и проведенного лечения были оценены 5 показателей осложнений. Обращает внимание большее число госпитализаций и повторных процедур реваскуляризаций среди лиц с острой и хронической формами ИБС и СД2. По нефатальным и фатальным осложнениям группы больных СД2 и без него не различались, хотя абсолютные цифры этих показателей оказались выше в группах лиц с СД2. Тем не менее, частота суммарных показателей конечных точек у лиц с СД2 вне зависимости от формы ИБС оказалась в 2 раза больше по сравнению с соответствующими контрольными группами, что носило достоверный характер. Худший прогноз у больных СД2 может быть обусловлен более выраженным коронарным атеросклерозом в виде многососудистого и дистального типа поражения КА.
Эксперты утверждают, что после успешной реваскуляризации миокарда частота возникновения сердечно-сосудистых событий у пациентов с СД2 в целом остается высокой, независимо от способа реваскуляризации, что подчеркивает необходимость проведения вторичной профилактики [10].
Прогноз пациентов с СД2 и различными формами ИБС зависит от уровня проведенного комплексного лечения и профилактики. Согласно данным шведского национального регистра SWEDEHEART (The Swedish Web-system for Enhancement and Development of Evidence-based care in Heart disease Evaluated According to Recommended Therapies), длительное применение средств вторичной профилактики после реваскуляризации миокарда (статины, β-адреноблокаторы, блокаторы ренин-ангиотензин-альдостероновой системы и антитромбоцитарные средства) ассоциировано с более низким риском смерти: лечение статинами (ОР 0,56 при 95% доверительном интервале (ДИ): 0,52-0,60), блокаторами ренин-ангиотензин-альдостероновой системы (ОР 0,78 при 95% ДИ: 0,730,84) и антитромбоцитарными средствами (ОР 0,74 при 95% ДИ: 0,69-0,81) (р<0,001 для всех сравнений) [23].
Заключение
Большинство пациентов с острой и хронической формами ИБС вне зависимости от нарушений углеводного обмена подверглись реваскуляризации миокарда. У пациентов без СД2 преобладало стентирование чаще всего одной КА, в то же время у больных СД2 наряду со стентированием проводилось КШ и сочетание двух процедур. Через год наблюдения число сердечно-сосудистых осложнений у больных СД2 оказалось в 2 раза выше по сравнению с пациентами без СД2, что подчеркивает важность проведения вторичной профилактики, включая комплексную медикаментозную коррекцию.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Драпкина О.М., Концевая А.В., Калинина А.М. и др. Профилактика хронических неинфекционных заболеваний в Российской Федерации. Национальное руководство 2022. Кардиоваскулярная терапия и профилактика. 2022;21(4):3235. doi:10.15829/1728-8800-2022-3235.
2. Шальнова С.А., Драпкина О.М. Значение исследования ЭССЕ-РФ для развития профилактики в России. Кардиоваскулярная терапия и профилактика. 2020;19(3):2602. doi:10.15829/1728-8800-2020-2602.
3. Драпкина О. М., Мамедов М. Н., Руденко Б.А. Атлас ангиографических картин у больных сахарным диабетом. М. 2022. 210 с. ISBN 978-5-6047282-0-8.
4. Алгоритмы специализированной медицинской помощи больным сахарным диабетом; Под ред. И. И. Дедова, М.В. Шестаковой, А.Ю. Майорова. 9-й вып. (дополн.). М., 2019. 212 с. ISBN 978- 5-6043776-5-9. doi:10.14341/DM221S1.
5. Nanayakkara N, Curtis AJ, Heritier S, et al. Impact of age at type 2 diabetes mellitus diagnosis on mortality and vascular complications: systematic review and meta-analyses. Diabetologia. 2021;64(2):275-87. doi:10.1007/s00125-020-05319-w.
6. Ledru F, Ducimetiere P, Battaglia S, et al. New diagnostic criteria for diabetes and coronary artery disease: Insights from an angiographic study. J Am Coll Cardiol. 2001;37:1543-50.
7. Кокожева М. А., Марданов Б. У., Поддубская Е.А. и др. Оценка структурно-функциональных показателей миокарда у пациентов с хронической ишемической болезнью сердца и различным гликемическим статусом. Кардиоваскулярная терапия и профилактика. 2021;20(7):3077. doi:10.15829/1728-8800-2021-3077.
8. Moreno PR, Murcia AM, Palacios IF, et al. Coronary composition and macrophage infiltration in atherectomy specimens from patients with diabetes mellitus. Circulation. 2000;102:2180-4.
9. Marso SP, Mercado N, Maehara A, et al. Plaque composition and clinical outcomes in acute coronary syndrome patients with metabolic syndrome or diabetes. JACC Cardiovasc Imaging. 2012;5:S42-52. doi:10.1016/j.jcmg.2012.01.008.
10. Рекомендации ESC/EACTS по реваскуляризации миокарда 2018. Российский кардиологический журнал. 2019;24(8):151-226. doi:10.15829/1560-4071-2019-8-151-226.
11. Бузуртанова М.Б., Дидигова Р. Т., Угурчиева З. О. др. Клинико-анатомические особенности миокарда по данным инвазивных и неинвазивных методов исследования у больных ишемической болезнью сердца в сочетании с сахарным диабетом. Кардиоваскулярная терапия и профилактика. 2019;18(3):18-23. doi:10.15829/1728-8800-2019-3-18-23.
12. Fearon WF, Nishi T, De Bruyne B, et al.; FAME 2 Trial Investigators. Clinical outcomes and costeffectiveness of fractional flow reserve-guided percutaneous coronary intervention in patients with stable coronary artery disease: Three-year follow-up of the FAME 2 trial (Fractional Flow Reserve Versus Angiography for Multivessel Evaluation). Circulation. 2018;137:480-7. doi:10.1161/CIRCULATIONAHA.117.031907.
13. BARI Study Group 2D, Frye RL, August P, Brooks MM, et al. A randomized trial of therapies for type 2 diabetes and coronary artery disease. N Engl J Med. 2009;360:2503-15. doi:10.1056/NEJMoa0805796.
14. Shehab A, Bhagavathula AS, Al-Rasadi K, et al. Diabetes and Mortality in Acute Coronary Syndrome: Findings from the Gulf COAST Registry. Curr Vasc Pharmacol. 2020;18(1):68-76. doi:10.2174/1570161116666181024094337.
15. Мамедов М. Н., Канорский С. Г. Международные исследования в кардиологии. М.: Фонд Кардиопрогресс. 2021. 176 c. ISBN 978-5-9905730-6-2.
16. Zubaid M, Rashed W, Alsheikh-Ali AA, et al. Disparity in STsegment Elevation Myocardial Infarction Practices and Outcomes in Arabian Gulf Countries (Gulf COAST Registry). Heart Views. 2017;18(2):41-6. doi:10.4103/HEARTVIEWS.HEARTVIEWS_113_16.
17. Imamura F, Mukamal KJ, Meigs JB, et al. Risk factors for type 2 diabetes mellitus preceded by β-cell dysfunction, insulin resistance, or both in older adults: the Cardiovascular Health Study. Am J Epidemiol. 2013;177(12):1418-29. doi:10.1093/aje/kws440.
18. Luscher TF, Creager MA, Beckman JA, Cosentino F. Diabetes and vascular disease: Pathophysiology, clinical consequences, and medical therapy: Part II. Circulation. 2003;108:1655-61. doi:10.1161/01.CIR.0000089189.70578.E2.
19. Chang M, Lee CW, Ahn JM, et al. Comparison of outcome of coronary artery bypass grafting versus drug-eluting stent implantation for non-ST-elevation acute coronary syndrome. Am J Cardiol. 2017;120:380-6. doi:10.1016/j.amjcard.2017.04.038.
20. Mohr FW, Morice MC, Kappetein AP, et al. Coronary artery bypass graft surgery versus percutaneous coronary intervention in patients with three-vessel disease and left main coronary disease: 5-year follow-up of the randomised, clinical SYNTAX trial. Lancet. 2013;381:629-38. doi:10.1016/S0140-6736(13)60141-5.
21. Head SJ, Milojevic M, Daemen J, et al. Mortality after coronary artery bypass grafting versus percutaneous coronary intervention with stenting for coronary artery disease: a pooled analysis of individual patient data. Lancet. 2018;391(10124):939-48. doi:10.1016/S0140-6736(18)30423-9.
22. Lehto HR, Winell K, Pietilä A, et al. Outcomes after coronary artery bypass grafting and percutaneous coronary intervention in diabetic and non-diabetic patients. Eur Heart J Qual Care Clin Outcomes. 2021:qcab065. doi:10.1093/ehjqcco/qcab065.
23. Figtree GA, Vernon ST, Hadziosmanovic N, et al. Mortality in STEMI patients without standard modifiable risk factors: a sexdisaggregated analysis of SWEDEHEART registry data. Lancet. 2021;397(10279):1085-94. doi:10.1016/S0140-6736(21)00272-500.
Об авторах
М. Н. МамедовРоссия
Мехман Ниязи оглы Мамедов— доктор медицинских наук, профессор, руководитель отдела вторичной профилактики хронических неинфекционных заболеваний.
Москва
Б. У. Марданов
Россия
Баходир Умаркулович Марданов — кандидат медицинских наук, старший научный сотрудник отдела вторичной профилактики хронических неинфекционных заболеваний.
Москва
М. А. Кокожева
Россия
Мадина Алиевна Кокожева — аспирант отдела вторичной профилактики хронических неинфекционных заболеваний.
Москва
Ф. Б. Шукуров
Россия
Фирдавс Баходурович Шукуров — старший научный сотрудник отдела инновационных эндоваскулярных методов профилактики и лечения сердечно-сосудистых заболеваний, врач рентгенэндоваскулярных методов диагностики и лечения.
Москва
Х. Р. Ахундова
Россия
Хумра Рамизовна Ахундова — соискатель отдела вторичной профилактики хронических неинфекционных заболеваний.
Москва
В. А. Куценко
Россия
Владимир Александрович Куценко — младший научный сотрудник лаборатории биостатистики отдела эпидемиологии хронических неинфекционных заболеваний.
Москва
Рецензия
Для цитирования:
Мамедов М.Н., Марданов Б.У., Кокожева М.А., Шукуров Ф.Б., Ахундова Х.Р., Куценко В.А. Особенности реваскуляризации миокарда и анализ конечных точек через год наблюдения у больных с острыми и хроническими формами ишемической болезни сердца в зависимости от наличия или отсутствия сахарного диабета. Кардиоваскулярная терапия и профилактика. 2022;21(10):3394. https://doi.org/10.15829/1728-8800-2022-3394
For citation:
Mamedov M.N., Mardanov B.U., Kokozheva M.A., Shukurov F.B., Akhundova H.R., Kutsenko V.A. Analysis of myocardial revascularization and endpoints after a 1-year follow-up of patients with acute and chronic coronary artery disease, depending on diabetes presence. Cardiovascular Therapy and Prevention. 2022;21(10):3394. (In Russ.) https://doi.org/10.15829/1728-8800-2022-3394
JATS XML

























































