Перейти к:
Морфофункциональный подход к диагностике болезни коронарных артерий пересаженного сердца. Клинический случай
https://doi.org/10.15829/1728-8800-2024-4106
EDN: ZULNYD
Аннотация
Болезнь коронарных артерий пересаженного сердца (БКАПС) остается нерешенной проблемой современной трансплантологии. Данный патологический процесс приводит к смерти 10% реципиентов донорского сердца в течение 15 лет. Ранняя диагностика БКАПС способствует улучшению прогноза пациентов с трансплантированным сердцем. Коронароангиография имеет ограничения в оценке гиперплазии интимы у пациентов с БКАПС, в связи с чем методы внутрисосудистой визуализации и оценки коронарной физиологии являются незаменимыми помощниками в раннем выявлении этого состояния. Представлен клинический случай использования морфофункционального подхода к диагностике БКАПС. Для определения функциональной значимости стеноза было проведено инвазивное измерение фракционного резерва кровотока. Метод оптической когерентной томографии позволил оценить морфологический субстрат поражения и подтвердить аутоиммунный механизм его возникновения. Использование морфофункционального подхода к данной группе пациентов позволяет с большей точностью прогнозировать течение заболевания, а также при необходимости, проводить адекватное лечение.
Ключевые слова
Для цитирования:
Колесников А.Ю., Тетерин Г.А., Арнт А.А., Кочергин Н.А. Морфофункциональный подход к диагностике болезни коронарных артерий пересаженного сердца. Клинический случай. Кардиоваскулярная терапия и профилактика. 2024;23(12):4106. https://doi.org/10.15829/1728-8800-2024-4106. EDN: ZULNYD
For citation:
Kolesnikov A.Yu., Teterin G.A., Arnt A.A., Kochergin N.A. Morphofunctional approach in the diagnosis of cardiac allograft vasculopathy: a case report. Cardiovascular Therapy and Prevention. 2024;23(12):4106. (In Russ.) https://doi.org/10.15829/1728-8800-2024-4106. EDN: ZULNYD
Введение
Болезнь коронарных артерий пересаженного сердца (БКАПС) — уникальный фибропролиферативный процесс в коронарных артериях (КА) у пациентов после ортотопической трансплантации сердца (ОТС). Морфологически БКАПС представляет собой диффузную концентрическую доброкачественную гиперплазию интимы с последующей окклюзией сосуда [1][2]. Причем поражение не ограничивается эпикардиальными ветвями, процесс распространяется дальше вплоть до микроциркуляторного русла [1]. В развитии данной патологии принимают участие, как иммунные, так и неиммунные факторы. БКАПС развивается у ~50% пациентов в течение 10 лет, приводит к смерти у 10% реципиентов в течение 15 лет после ОТС и является главной причиной повторной пересадки сердца [1-3]. Типичные клинические проявления ишемии миокарда у пациентов с БКАПС отсутствуют, это связано с денервацией органа во время трансплантации. Клиника может манифестировать в виде острой сердечной недостаточности, декомпенсации хронической сердечной недостаточности или внезапной сердечной смерти [4]. Раннее выявление БКАПС может способствовать улучшению долгосрочного прогноза у пациентов с трансплантированным сердцем, но проблема ранней диагностики БКАПС сегодня как никогда актуальна [5].
Главным звеном патогенеза является иммуноопосредованное повреждение эндотелиоцитов КА аллотрансплантата, приводящее к гладкомышечной и эндотелиальной гиперплазии. После первичного повреждения интимы, эндотелиоциты инициируют провоспалительный каскад реакций, в результате чего и так поврежденная стенка КА инфильтрируется лимфоцитами и патологический процесс усугубляется [6]. Также установлена связь реакции острого отторжения аллотрансплантата с последующим развитием БКАПС [7]. Среди неиммунных компонентов патогенеза выделяют цитомегаловирусную инфекцию, классические факторы сердечно-сосудистого риска (артериальная гипертензия, сахарный диабет, дислипидемия, ожирение), причем как у реципиента, так и у донора. Важное значение имеет и характер смерти мозга донора, поскольку резкий выброс катехоламинов и провоспалительных цитокинов ассоциирован с последующим повреждением аллотрансплантата. Еще один неиммунный механизм — ишемическое реперфузионное повреждение, заключающееся в высвобождении свободных радикалов из ткани аллотрансплантата после восстановления коронарного кровотока, что коррелирует со временем холодовой и тепловой ишемии трансплантата сердца [1][6].
Согласно рекомендациям ISHLT (The International Society for Heart and Lung Transplantation) и данным зарубежных кардиологических центров, рутинным скрининговым методом в диагностике БКАПС на сегодняшний день остается коронароангиография (КАГ) [4][7]. КАГ позволяет оценить просвет сосуда, но не изучить детально его стенку, а её чувствительность в выявлении БКАПС составляет 44% [1][2][7][8]. Однако в ряде исследований, оценивающих гистологическое строение сосудистой стенки КА трансплантированного сердца, было показано, что у 75% пациентов, несмотря на нормальную КАГ, наблюдались изменения, характерные для БКАПС [9][10]. Методы внутрисосудистой визуализации позволяют с большей точностью оценить характер и тяжесть поражения КА [3]. Внутрисосудистое ультразвуковое исследование (ВСУЗИ) на сегодняшний день является золотым стандартом в ранней диагностике БКАПС, оно позволяет получить информацию о морфологической структуре стенки сосуда и оценить результат имплантации стентов [3][5][7].
Метод оптической когерентной томографии (ОКТ) рассматривается как альтернатива ВСУЗИ [5]. По данным ряда исследований ОКТ в диагностике БКАПС превосходит ВСУЗИ, поскольку имеет большее разрешение и позволяет выявить гиперплазию интимы на ранних этапах развития. Помимо этого, данная методика даёт возможность дифференцировать слои стенок венечных артерий и изучить их ультраструктуры, которые, в свою очередь, могут быть предикторами начала развития БКАПС [3-5][7].
На сегодняшний день основными принципами профилактики развития БКАПС являются коррекция факторов сердечно-сосудистого риска (артериальная гипертензия, сахарный диабет, гиперлипидемия, курение, ожирение), поддержание физической активности пациента, адекватная иммуносупрессивная терапия [7]. Фармакологические методы лечения крайне ограничены, а их эффективность дискутабельна и требует дальнейших исследований [7]. Реваскуляризация миокарда является симптоматической коррекцией БКАПС, но сегодня это главный хирургический подход в лечении таких пациентов, поскольку стентирование позволяет сохранить аллотрансплантат и избежать повторной трансплантации сердца [7].
Таким образом, БКАПС по сей день остается нерешенной проблемой для современной трансплантологии, методы внутрисосудистой визуализации помогают в ранней диагностике заболевания, но эффективной превентивной терапии пока не предложено.
Клинический случай
В приемное отделение 26.11.2020 поступил пациент С. 55 лет с клиникой острого коронарного синдрома (хронология течения болезни представлена на рисунке 1). По результатам электрокардиографического исследования выявлен Q-образующий нижнебоковой перегородочный инфаркт миокарда, трепетание предсердий. Эхокардиографическое исследование показало наличие митрально-папиллярной дисфункции с регургитацией на митральном клапане 2 ст., фракция выброса (ФВ) составляла 52%. Пациенту проведена КАГ — значимые стенозы в передней межжелудочковой артерии (ПМЖА) и огибающей артерии, разрешенные проведением чрескожного коронарного вмешательства.
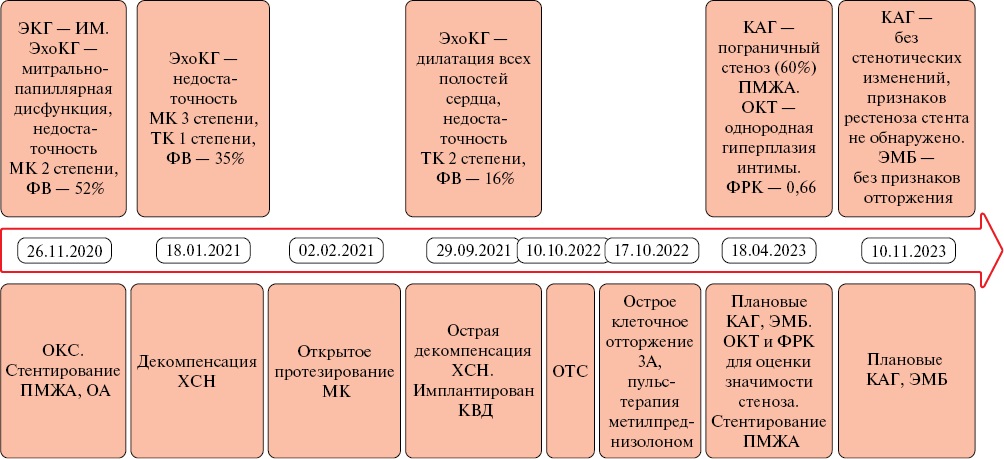
Рис. 1 Хронология течения болезни.
Примечание: ИМ — инфаркт миокарда, КАГ — коронароангиография, КВД — кардиовертер-дефибриллятор, МК — митральный клапан, ОА — огибающая артерия, ОКС — острый коронарный синдром, ОКТ — оптическая когерентная томография, ОТС — ортотопическая трансплантация сердца, ПМЖА — передняя межжелудочковая артерия, ТК — трикуспидальный клапан, ФВ — фракция выброса, ФРК — фракционный резерв кровотока, ХСН — хроническая сердечная недостаточность, ЭКГ — электрокардиография, ЭМБ — эндомиокардиальная биопсия, ЭхоКГ — эхокардиография.
С начала января 2021г в домашних условиях ухудшение состояния в виде нарастания одышки и отеков нижних конечностей. Обратился в поликлинику 18.01.2021г, в тот же день госпитализирован в стационар с декомпенсацией хронической сердечной недостаточности. На эхокардиографии выявлена прогрессирующая недостаточность митрального клапана с регургитацией 3 ст., относительная недостаточность трикуспидального клапана с регургитацией 1 ст., а ФВ левого желудочка снизилась до 35%. Больной был консультирован кардиохирургом, после чего кардиокоманда приняла решение выполнить открытое протезирование митрального клапана. Консультирован хирургом-аритмологом, рекомендована имплантация кардиовертера-дефибриллятора.
Через полгода этот же пациент повторно госпитализируется в клинику с острой декомпенсацией хронической сердечной недостаточности. ФВ левого желудочка составляет 16%, отмечается дилатация всех полостей сердца, недостаточность трикуспидального клапана 2 ст. Пациенту была выполнена имплантация кардиовертера-дефибриллятора. Был установлен диагноз ишемической кардиомиопатии, в связи с чем пациент включен в лист ожидания трансплантации сердца.
Пациенту 10.10.2022 была выполнена ОТС по биатриальной методике. Длительность холодовой ишемии составила 125 мин, тепловой — 80 мин. После имплантации донорского органа сердечная деятельность восстановилась спонтанно, отмечалась гипотония, повышенная потребность в инотропной поддержке. Принято решение выполнить КАГ с эндомиокардиальной биопсией, выявлено острое клеточное отторжение 3А, купированное пульс-терапией метилпреднизолоном. Окклюзионно-стенотических поражений выявлено не было. Во время пребывания в стационаре пациент получал комбинированную медикаментозную терапию (статины, блокаторы медленных Ca-каналов, ингибиторы ангиотензинпревращающего фермента, антикоагулянты, двойную антиагрегантную терапию, микофенолата мофетил, такролимус, ко-тримоксазол, валганцикловир). В последующем пациент был выписан из стационара в удовлетворительном состоянии.
Спустя полгода 18.04.2023 пациент поступил на плановое обследование, коррекцию лечения. Были проведены эндомиокардиальная биопсия, КАГ, по данным которой у пациента отмечается пограничное (60%) поражение ПМЖА (рисунок 2). Принято решение об измерении фракционного резерва кровотока (ФРК). Выполнена селективная катетеризация левой КА проводниковым катетером EBU 4,0, по которому интракоронарно введено 150 мкг нитроглицерина. После предварительной калибровки, в ПМЖА заведен датчик ФРК на 20 мм дистальнее целевой зоны, с последующим интракоронарным введением аденозинтрифосфата со скоростью 140 мг/кг/мин, на пике гиперемии значение ФРК составило 0,66 (рисунок 3), что свидетельствует о значимости стеноза. С целью оценки морфологического субстрата стеноза КА следующим этапом было решено провести ОКТ. Заведен коронарный проводник в апикальный сегмент ПМЖА, по которому заведен датчик ОКТ. Выполнена автоматическая протяжка на фоне введения контрастного вещества. По результатам ОКТ выявлена однородная гиперплазия интимы (рисунок 4) на всём протяжении стеноза, его протяженность — 14 мм, диаметр сосуда за сужением составил 3,12 мм. С учетом полученных результатов проведен подбор стента и выполнено стентирование средней трети ПМЖА (рисунок 5), с контролем результата методом ОКТ — полная аппозиция стента без признаков диссекции, после чего процедура была завершена.
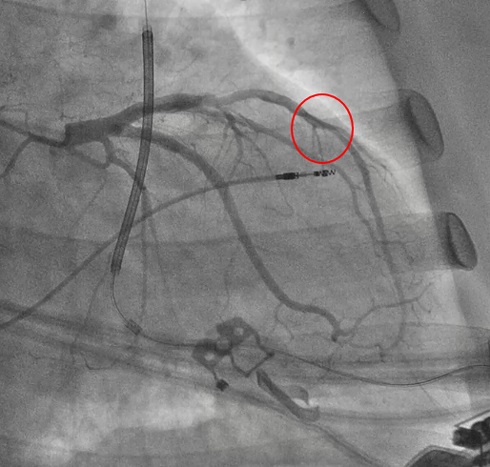
Рис. 2 КАГ, пограничное поражение ПМЖА.
Примечание: КАГ — коронароангиография, ПМЖА — передняя межжелудочковая артерия.
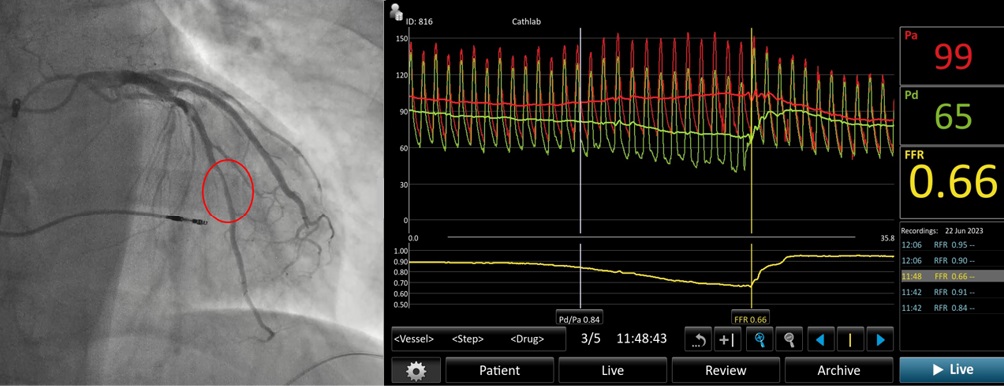
Рис. 3 Измерение ФРК.
Примечание: ФРК — фракционный резерв кровотока.
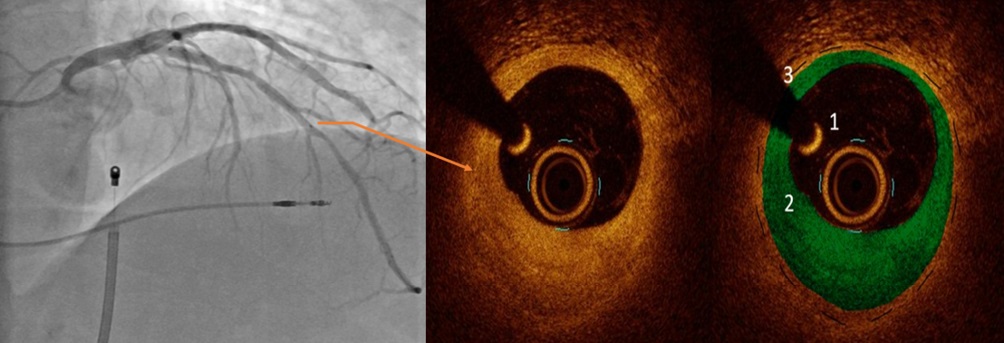
Рис. 4 ОКТ. 1 — просвет коронарной артерии, 2 — гиперплазия неоинтимы, 3 — медия.
Примечание: ОКТ — оптическая когерентная томография. Цветное изображение доступно в электронной версии журнала.
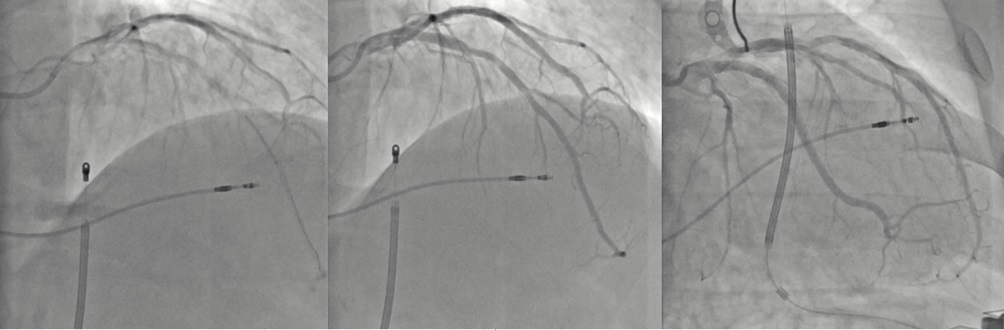
Рис. 5 Стентирование ПМЖА и его ангиографический результат.
Примечание: ПМЖА — передняя межжелудочковая артерия.
По данным эндомиокардиальной биопсии из правого желудочка у пациента отмечается клеточное отторжение 1А. Проведена коррекция медикаментозной терапии, и пациент был в удовлетворительном состоянии выписан домой.
При последующем наблюдении через 6 мес. была выполнена КАГ и эндомиокардиальная биопсия, стенотических изменений в коронарном русле и признаков гуморального или клеточного отторжения трансплантата обнаружено не было. В месте имплантации стента в ПМЖА также не было обнаружено рестенозирования. Самочувствие пациента удовлетворительное, без отрицательной динамики.
Таким образом, использовался морфофункциональный подход для оценки стеноза у данного пациента с последующим принятием решения о тактике лечения с положительным полугодовым результатом.
Обсуждение
Использование метода измерения ФРК позволяет провести оценку физиологической значимости стеноза КА. Для пациентов после ОТС значение ФРК <0,90 предрасполагает к неблагоприятным клиническим исходам [11]. Одной лишь визуальной оценки поражения КА может быть недостаточно, например, в рандомизированном клиническом исследовании FULL REVASK (Ffr-gUidance for compLete non-cuLprit REVASCularization) разница в определении анатомической и функциональной значимости стеноза достигает 34% при пограничных стенозах (50-69%), 47% при ангиографически значимых стенозах (70-89%) и 18% при тяжелых стенозах (90-99%) [12].
Снижение ФРК у пациентов после ОТС является независимым предиктором отдаленной смерти или необходимости в ретрансплантации сердца [13]. В исследовании Nagumo S, et al. [11] у метода ФРК был обнаружен диагностический потенциал: 34,8% пациентов были реклассифицированы из группы низкого риска по критериям ISHLT в группу функционально высокого риска со значением ФРК <0,80. В другом исследовании Mileva N, et al. [14] был проведен сравнительный анализ показателей виртуального ФРК и инвазивного измерения ФРК, который доказал альтернативность этих двух методов у пациентов с БКАПС. Это дает основанием полагать, что у данного метода есть определенная клиническая значимость в функциональной оценке стенозов при БКАПС.
Вместе с тем, у метода ФРК существуют ограничения при БКАПС. ФРК отражает лишь физиологию эпикардиального кровотока и не учитывает микроциркуляторное русло. При БКАПС характер поражения может быть диффузным, в связи с чем замеряемые датчиком цифры давления за исследуемым стенозом на пике гиперемии могут быть недостоверными, что искажает конечный результат измерения ФРК [15]. На сегодняшний день из физиологических измерений коронарной гемодинамики последние рекомендации ISHLT ставят на первое место измерение коронарного резерва кровотока и индекса микроциркуляторной резистентности [7]. В данном клиническом случае метод ОКТ позволил оценить морфологию поражения КА и доказать отсутствие его диффузности, в связи с чем результаты ФРК можно считать корректными.
Ранняя диагностика БКАПС является важной и неотъемлемой частью ведения пациентов, перенесших ОТС. Классическая КАГ недооценивает степень поражения коронарного русла в связи с диффузностью поражения, тогда как методы внутрисосудистой визуализации способны справится с этой задачей.
Международные рекомендации сегодня предлагают КАГ в комбинации с ВСУЗИ в качестве стандартного метода диагностики БКАПС [1][7]. Применение ВСУЗИ, в связи с высокой проникающей способностью, действительно приводит к успехам в ранней диагностике БКАПС, а чувствительность метода по результатам некоторых исследований составляет 76,3 vs 24% у КАГ. Так, в одном из сравнительных исследований Torres, et al. КАГ выявила признаки БКАПС лишь у 32,3% пациентов, а ВСУЗИ — 54,8% [16]. Несмотря на это ВСУЗИ обладает своими недостатками. В частности, низкая разрешающая способность не позволяет выявить начальные изменения в интиме коронарных сосудов, кроме того, ВСУЗИ не позволяет оценить функциональную значимость имеющихся стенозов [11][17].
Так же, как и ВСУЗИ, метод ОКТ дает возможность выявить и оценить гиперплазию интимы. Преимуществом ОКТ является большая разрешающая способность, превышающая таковую у ВСУЗИ в 10 раз, что позволяет выявить самые ранние изменения в интиме КА, получить изображение, близкое к гистологическому уровню, и идентифицировать ультраструктуры, являющиеся предикторами развития БКАПС [3-5]. В своей работе Hou J, et al. (2012) сравнивали эффективность ВСУЗИ и ОКТ на 7 пациентах, перенесших ОТС, гиперплазия интимы была выявлена по ОКТ в 66,7% случаев и лишь в 14,3% на ВСУЗИ [4]. Из ограничений ОКТ имеет низкую проникающую способность, что не позволяет оценить глубокие поражения при выраженной гиперплазии неоинтимы [7][17].
Заключение
В представленном клиническом случае продемонстрирован морфофункциональный подход к диагностике БКАПС. Для определения функциональной значимости стеноза было проведено инвазивное измерение ФРК. Метод ОКТ позволил оценить морфологический субстрат поражения, подтвердить БКАПС. Использование морфофункционального подхода к данной группе пациентов позволяет с большей точностью прогнозировать течение заболевания, а также при необходимости, проводить адекватное лечение.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Pighi M, Gratta A, Marin F, et al. Cardiac allograft vasculopathy: Pathogenesis, diagnosis and therapy. Transplant Rev (Orlando). 2020;34(4):100569. doi:10.1016/j.trre.2020.100569.
2. Mendiz OA, Gamboa P, Renedo MF, et al. Intravascular ultrasound for cardiac allograft vasculopathy detection. Clin Transplant. 2021;35(2):e14167. doi:10.1111/ctr.14167.
3. Khandhar SJ, Yamamoto H, Teuteberg JJ, et al. Optical coherence tomography for characterization of cardiac allograft vasculopathy after heart transplantation (OCTCAV study). J Heart Lung Transplant. 2013;32(6):596-602. doi:10.1016/j.healun.2013.02.005.
4. Hou J, Lv H, Jia H, et al. OCT assessment of allograft vasculopathy in heart transplant recipients. JACC Cardiovasc Imaging. 2012;5(6):662-3. doi:10.1016/j.jcmg.2012.01.018.
5. Саховский С. А., Колоскова Н. Н., Гончарова А. Ю. и др. Внутрисосудистые методы визуализации в оценке васкулопатии трансплантированного сердца. Вестник трансплантологии и искусственных органов. 2019;21(1):165-8. doi:10.15825/1995-1191-2019-1-165-168.
6. Lee F, Nair V, Chih S. Cardiac allograft vasculopathy: Insights on pathogenesis and therapy. Clin Transplant. 2020;34(3):e13794. doi:10.1111/ctr.13794.
7. Velleca A, Shullo MA, Dhital K, et al. The International Society for Heart and Lung Transplantation (ISHLT) guidelines for the care of heart transplant recipients. J Heart Lung Transplant. 2023;42(5):e1-e141. doi:10.1016/j.healun.2022.10.015.
8. Pollack A, Nazif T, Mancini D, et al. Detection and imaging of cardiac allograft vasculopathy. JACC Cardiovasc Imaging. 2013;6(5):613-23. doi:10.1016/j.jcmg.2013.03.001.
9. Olymbios M, Kwiecinski J, Berman DS, et al. Imaging in Heart Transplant Patients. JACC Cardiovasc Imaging. 2018;11(10): 1514-30. doi:10.1016/j.jcmg.2018.06.019.
10. Clemmensen TS, Jensen NM, Eiskjær H. Imaging of Cardiac Transplantation: An Overview. Semin Nucl Med. 2021;51(4): 335-48. doi:10.1053/j.semnuclmed.2020.12.012.
11. Nagumo S, Gallinoro E, Candreva A, et al. Vessel Fractional Flow Reserve and Graft Vasculopathy in Heart Transplant Recipients. J Interv Cardiol. 2020;12;2020:9835151. doi:10.1155/2020/9835151.
12. Böhm F, Mogensen B, Östlund O, et al. The Full Revasc (FfrgUidance for compLete non-cuLprit REVASCularization) Registrybased randomized clinical trial. Am Heart J. 2021;241:92-100. doi:10.1016/j.ahj.2021.07.007.
13. Lee MS, Tadwalkar RV, Fearon WF, et al. Cardiac allograft vasculopathy: A review. Catheter Cardiovasc Interv. 2018;92(7): E527-36. doi:10.1002/ccd.27893.
14. Mileva N, Nagumo S, Gallinoro E, et al. Validation of Coronary Angiography-Derived Vessel Fractional Flow Reserve in Heart Transplant Patients with Suspected Graft Vasculopathy. Diagnostics (Basel). 2021;11(10):1750. doi:10.3390/diagnostics11101750.
15. Кальченко Е. А., Гончарова А. Ю., Саховский С. А. Проблема диагностики и лечения болезни коронарных артерий пересаженного сердца (обзор литературы). Диагностическая и интервенционная радиология. 2019;13(3):58-67. doi:10.25212/DIR.2019.13.3.07.
16. Torres HJ, Merello L, Ramos SA, et al. Prevalence of cardiac allograft vasculopathy assessed with coronary angiography versus coronary vascular ultrasound and virtual histology. Transplant Proc. 2011;43(6):2318-21. doi:10.1016/j.transproceed.2011.06.002.
17. Колесников А. Ю., Арнт А. А., Кочергин Н. А. Возможности внутрисосудистых методов визуализации в диагностике васкулопатии трансплантированного сердца. Обзор литературы. Вестник трансплантологии и искусственных органов. 2024;26(1):97-102. doi:10.15825/1995-1191-2024-1-97-102.
Об авторах
А. Ю. КолесниковРоссия
м.н.с. лаборатории тканевой инженерии и внутрисосудистой визуализации.
Кемерово
Г. А. Тетерин
Россия
студент 4 курса лечебного факультета.
Кемерово
А. А. Арнт
Россия
м.н.с. лаборатории тканевой инженерии и внутрисосудистой визуализации.
Кемерово
Н. А. Кочергин
Россия
к.м.н., зав. лабораторией тканевой инженерии и внутрисосудистой визуализации.
Кемерово
Дополнительные файлы
- Представлен клинический случай использования морфофункционального подхода в ранней диагностике болезни коронарных артерий пересаженного сердца (БКАПС).
- Оценка одновременно морфологического субстрата методом оптической когерентной томографии и функциональной значимости стеноза методом измерения фракционного резерва кровотока позволяет с высокой достоверностью диагностировать БКАПС на ранних сроках её развития.
- Морфофункциональный подход в оценке БКАПС позволяет прогнозировать дальнейшее течение заболевания и определить подходящую тактику лечения таких пациентов.
Рецензия
Для цитирования:
Колесников А.Ю., Тетерин Г.А., Арнт А.А., Кочергин Н.А. Морфофункциональный подход к диагностике болезни коронарных артерий пересаженного сердца. Клинический случай. Кардиоваскулярная терапия и профилактика. 2024;23(12):4106. https://doi.org/10.15829/1728-8800-2024-4106. EDN: ZULNYD
For citation:
Kolesnikov A.Yu., Teterin G.A., Arnt A.A., Kochergin N.A. Morphofunctional approach in the diagnosis of cardiac allograft vasculopathy: a case report. Cardiovascular Therapy and Prevention. 2024;23(12):4106. (In Russ.) https://doi.org/10.15829/1728-8800-2024-4106. EDN: ZULNYD
JATS XML

























































