Перейти к:
Безболевой перипроцедурный инфаркт миокарда при несердечной операции. Клинический случай
https://doi.org/10.15829/1728-8800-2025-4143
EDN: IUXTYG
Аннотация
Введение. Диагностика безболевых форм ишемической болезни сердца (ИБС) в раннем послеоперационном периоде затруднительна. Важно своевременно выявлять факторы риска сердечно-сосудистых осложнений перед несердечными хирургическими вмешательствами, что определяет выбор оптимальной диагностической и лечебной стратегии в раннем послеоперационном периоде.
Краткое описание. В представленном клиническом случае оценены результаты обследования, тактика диагностики и лечения пациентки 59 лет с сахарным диабетом 2 типа, артериальной гипертензией и факторами риска ИБС после эндопротезирования тазобедренного сустава при отсутствии клинически вероятной ИБС. Объективный статус пациентки оценивали с помощью клинических, функциональных, лабораторных методов исследований и оценочных шкал предтестовой вероятности ИБС, RCRI (Revised Cardiac Risk Index), Gupta MICA (Myocardial Infarction or Cardiac Arest), Caprini (Сaprini risk score/Caprini Risk Assessment Model), Wells (The Wells criteria for pulmonary embolism), Н2FPEF (Heavy; Hypertensive; Atrial Fibrillation; Pulmonary Hypertension; Elder; Filling Pressure). Риск сердечно-сосудистых осложнений по шкалам RCRI, Gupta MICA был расценен как низкий. При внесердечной операции среднего риска на фоне кровопотери у пациентки возникла острая сердечно-сосудистая недостаточность, диагностирован тропонин-положительный инфаркт миокарда при отсутствии электрокардиографических и эхокардиографических признаков нарушения локальной сократимости, на фоне стенозирующего атеросклероза коронарных артерий, подтвержденного результатами коронароангиографии.
Заключение. Клинический случай демонстрирует актуальность оценки вероятности ИБС (предтестовой, клинической) у пациентов с факторами риска ИБС при несердечных операциях. Частота инфарктов миокарда после несердечных операций, по данным Kashlan B, et al. (2024), составляет 1%. Необходимо учитывать, что существующие шкалы оценки риска перипроцедурных осложнений не обладают высокой точностью и требуют осмысленного применения. Случай представляет интерес для терапевтов, кардиологов, эндокринологов в отношении подготовки коморбидного пациента к плановой операции с достижением рекомендованных целевых показателей у пациента с факторами риска ИБС и необходимостью оценки периоперационных рисков.
Ключевые слова
Для цитирования:
Иванова Э.В., Арсентьев А.В., Илларионова М.К. Безболевой перипроцедурный инфаркт миокарда при несердечной операции. Клинический случай. Кардиоваскулярная терапия и профилактика. 2025;24(2):4143. https://doi.org/10.15829/1728-8800-2025-4143. EDN: IUXTYG
For citation:
Ivanova E.V., Arsentyev A.V., Illarionova M.K. Silent periprocedural myocardial infarction during non-cardiac surgery: a case report. Cardiovascular Therapy and Prevention. 2025;24(2):4143. (In Russ.) https://doi.org/10.15829/1728-8800-2025-4143. EDN: IUXTYG
Введение
В мире ежегодно проводится >300 млн несердечных операций, зачастую сопровождающихся миокардиальным повреждением (МП). По данным исследования VISION (международное многоцентровое исследование с участием 21842 пациентов в возрасте ≥45 лет, перенесших стационарную не кардиальную операцию), МП — вторая по частоте причина смерти в течение 30 сут. после состоявшегося кровотечения [1]. Среди сердечно-сосудистых осложнений (ССО) при летальных исходах отмечаются остановка сердца (64%), аритмии (52%), отек легких (24%), инфаркт миокарда (ИМ) (18%), инсульт (13%), тромбоэмболия легочной артерии (3,5%) [2]. По данным национального регистра США, периоперационный ИМ возникает у 0,9% пациентов при больших несердечных операциях, четко связан с риском смерти после операции [3].
Информации о частоте безболевого перипроцедурного ИМ и методах его своевременной диагностики в литературе недостаточно. Следует учитывать, что существующие шкалы оценки риска перипроцедурных осложнений не обладают высокой точностью и требуют осмысленного применения.
Выявление пациентов с повышенным риском ССО перед несердечными операциями остается актуальной задачей1 [4]. Безболевая форма ишемической болезни сердца (ИБС) может быть случайной находкой при рутинных исследованиях перед планируемым несердечным хирургическим вмешательством, что в результате потребует такой же лечебной тактики, как и при типичной/атипичной стенокардии2 [5-11].
Цель исследования — демонстрация клинического случая безболевого перипроцедурного ИМ в раннем послеоперационном периоде после плановой травматолого-ортопедической операции.
Клинический случай
Информация о пациенте
Пациентка 59 лет, русская, городская жительница, госпитализирована в федеральный травматолого-ортопедический центр (Центр) 23.06.2023 для планового эндопротезирования тазобедренного сустава. Выявленные факторы риска ИБС: менопауза, артериальная гипертензия (АГ) с 2008г, сахарный диабет 2 типа с 2014г, гиперхолестеринемия (уровень общего холестерина — 5,79 ммоль/л). Наследственность по сердечно-сосудистым заболеваниям не отягощена.
Результаты физикального осмотра
Клинические данные о наличии у пациентки симптомов типичной и атипичной стенокардии отсутствовали.
Предоперационный диагноз
Посттравматический деформирующий правосторонний коксартроз 3 стадии. Сопутствующие заболевания — гипертоническая болезнь II стадии, контролируемая АГ, атеросклероз аорты с переходом на аортальный клапан, риск 4 (очень высокий), целевое артериальное давление (АД) 120-130 мм рт.ст.; сахарный диабет, тип 2, целевой уровень гликированного гемоглобина (НbА1с) <7,0% достигнут; посттравматическая нейропатия правых малоберцового и большеберцового нервов с парезом правой стопы и сенсорными нарушениями, болевой вариант, и левого малоберцового нерва с сенсомоторными нарушениями; состояние после компрессионного перелома L2 позвонка; протрузии межпозвонковых дисков L4-L5-S1; вертеброгенный болевой синдром.
Временнáя шкала представлена в таблице 1.
Таблица 1
Временнáя шкала

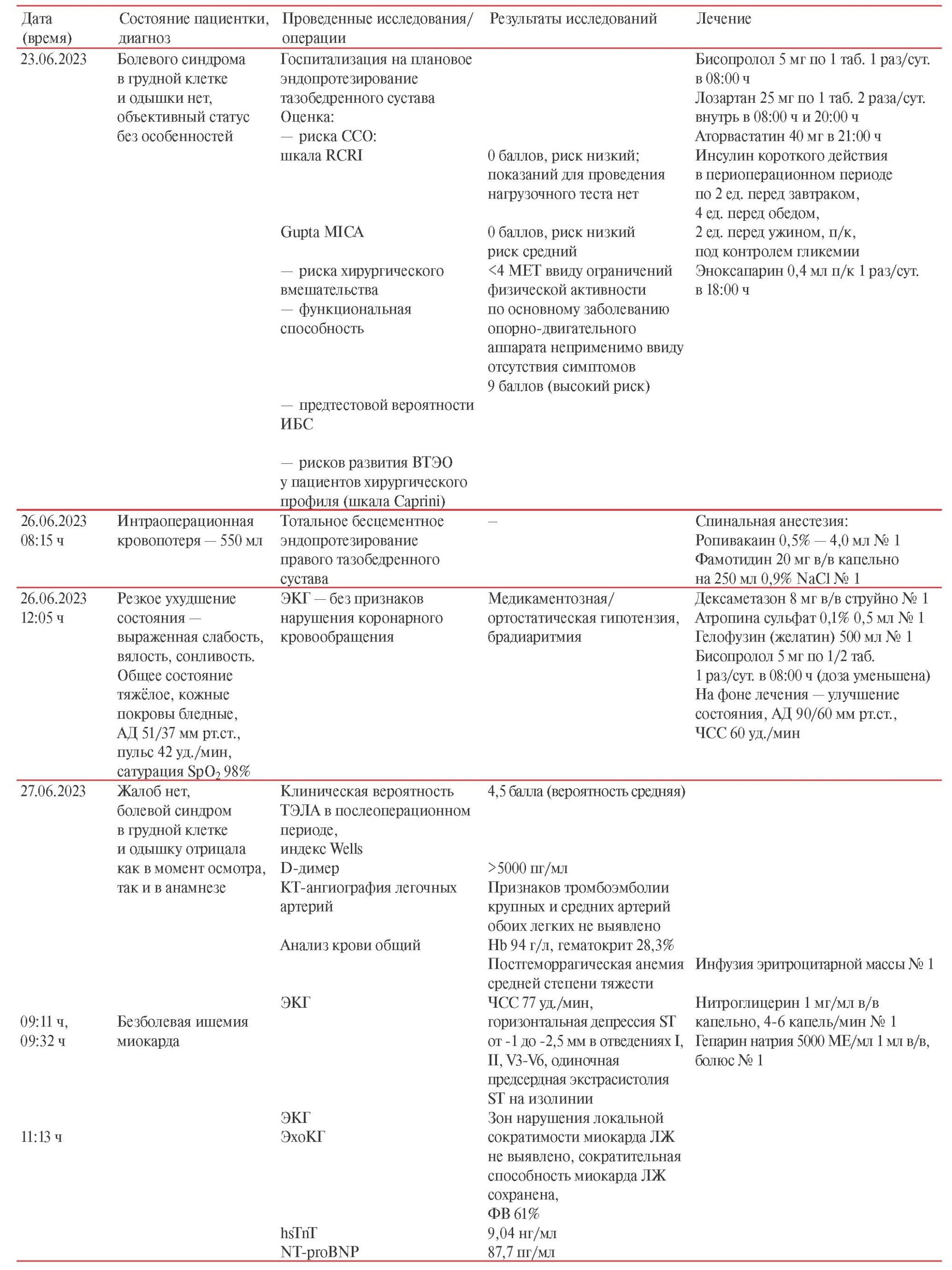
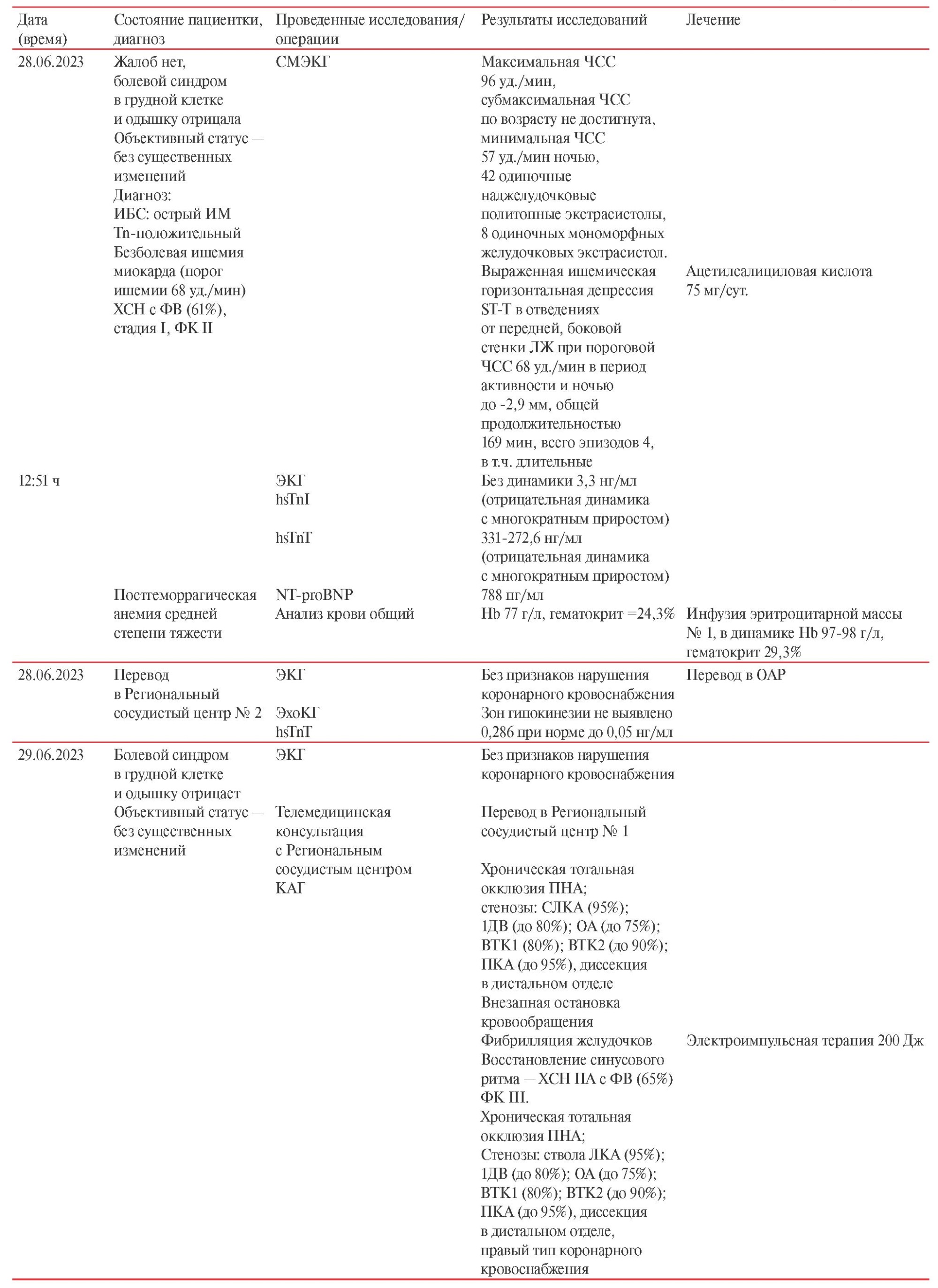
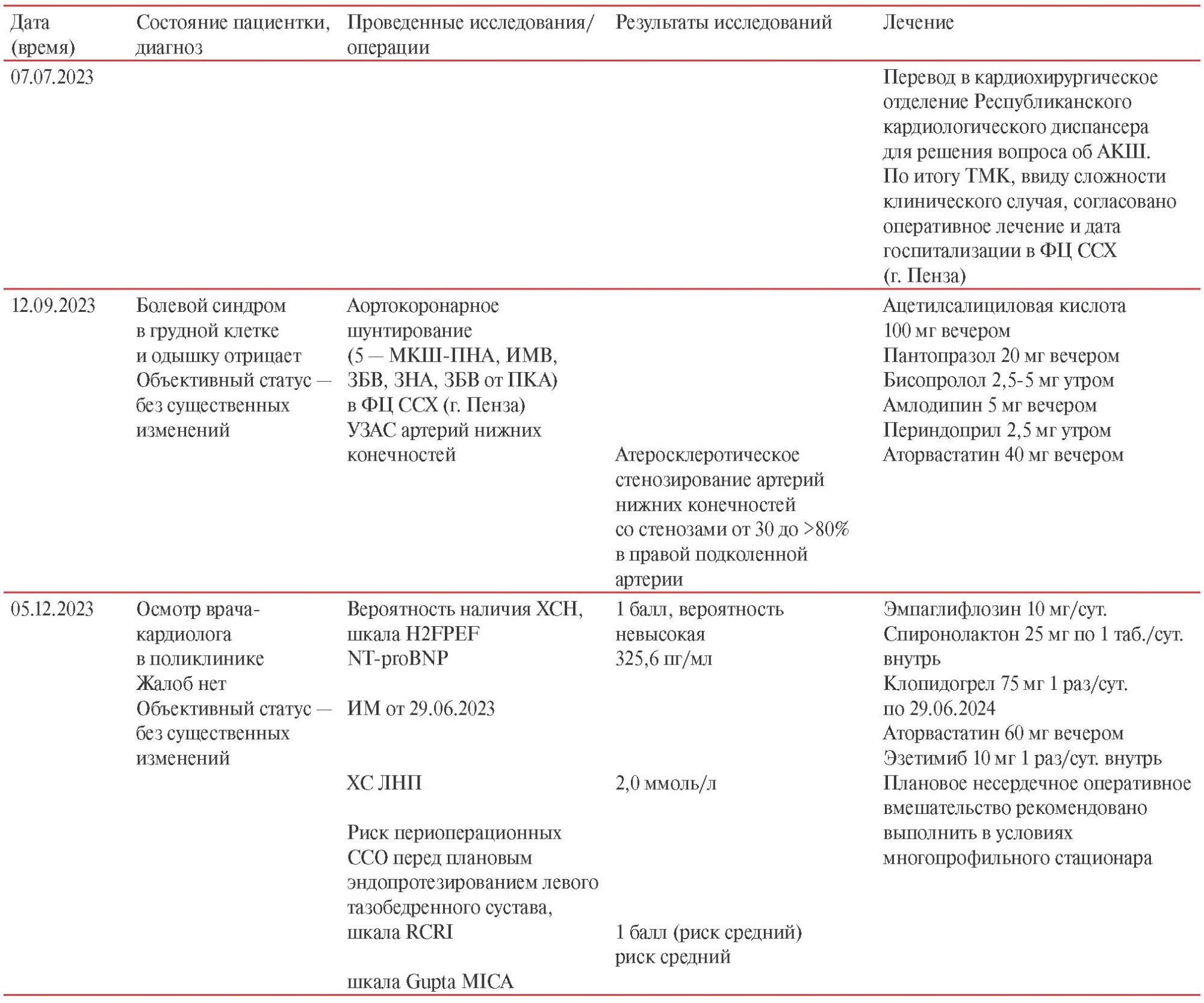
Примечание: ДВ — диагональная ветвь, АД — артериальное давление, АКШ — аортокоронарное шунтирование, в/в — внутривенно, ВТК — ветвь тупого края, ВТЭО — венозные тромбоэмболические осложнения, ЗБВ — заднебоковая ветвь, ЗНА — задняя нисходящая артерия, ИБС — ишемическая болезнь сердца, ИМ — инфаркт миокарда, ИМВ — интермедиальная ветвь, КАГ — коронароангиография, КТ — компьютерная томография, ЛЖ — левый желудочек, ЛКА — левая коронарная артерия, ЛНП — липопротеины низкой плотности, МКШ — маммарокоронарное шунтирование, ОА — огибающая артерия, ОАР — отделение анестезиологии-реанимации с палатами реанимации и интенсивной терапии Центра, п/к — подкожно, ПКА — правая коронарная артерия, ПНА — передняя нисходящая артерия, СЛКА — ствол ЛКА, СМЭКГ — суточное мониторирование ЭКГ, ССО — сердечно-сосудистое осложнение, ТМК — телемедицинская консультация, ТЭЛА — тромбоэмболия легочной артерии, УЗАС — ультразвуковое ангиосканирование, ФВ — фракция выброса, ФК — функциональный класс, ФЦ ССХ — Федеральный центр сердечно-сосудистой хирургии, ХС — холестерин, ХСН — хроническая сердечная недостаточность, ЧСС — частота сердечных сокращений, ЭКГ — электрокардиография, ЭхоКГ — эхокардиография, Gupta MICA — Myocardial Infarction or Cardiac Arest, Hb — гемоглобин, hsTnI — тропонин I, определенный высокочувствительным методом, hsTnT — тропонин T, определенный высокочувствительным методом, MET — метаболический эквивалент, NT-proBNP — N-концевой промозговой натрийуретический пептид, RCRI — Revised Cardiac Risk Index, SpO2 — сатурация кислорода, Н2FPEF — Heavy; Hypertensive; Atrial Fibrillation; Pulmonary Hypertension; Elder; Filling Pressure.
Диагностическая оценка
Для оценки объективного статуса пациентки проведены клинико-лабораторные исследования, в т.ч. определены: уровень гемоглобина, биомаркеры некроза миокарда; шкалы RCRI (Revised Cardiac Risk Index), Gupta MICA (Myocardial Infarction or Cardiac Arest), предтестовой вероятности ИБС, Caprini (Сaprini risk score/Caprini Risk Assessment Model), Wells (The Wells criteria for pulmonary embolism), Н2FPEF (Heavy; Hypertensive; Atrial Fibrillation; Pulmonary Hypertension; Elder; Filling Pressure). В отношении пациентов с патологией опорно-двигательной системы, как и в данном случае, применение нагрузочных тестов и оценка индекса DASI (Duke Activity Status Index) затруднительны ввиду ограничений физической активности на фоне локального болевого синдрома. При наличии показаний такие пациенты направляются на коронароангиографию (КАГ) и мультиспиральную компьютерную томографию коронарных артерий (КА).
Дифференциальная диагностика
Проводилась между повреждением миокарда ишемической и неишемической этиологии на основании динамики биомаркеров некроза миокарда при отсутствии электрокардиографических (ЭКГ)-, эхокардиографических (ЭхоКГ)-признаков ишемии и нарушений локальной сократимости миокарда.
Прогностические характеристики
Для оценки сердечно-сосудистых рисков применялись рекомендованная при несердечных операциях шкала RCRI (0 баллов, риск низкий; показаний для проведения нагрузочного теста нет); рекомендованная при любых операциях шкала Gupta MICA (0 баллов, риск низкий). Проведена оценка риска хирургического вмешательства, риск средний. Оценена функциональная способность: <4 МЕТ (метаболический эквивалент) ввиду ограничений физической активности по основному заболеванию опорно-двигательного аппарата. Риск венозных тромбоэмболических осложнений по шкале Caprini — 9 баллов (высокий); назначены низкомолекулярные гепарины [12].
Медицинские вмешательства
26.06.2023 через 2,5 ч после проведения несердечной операции (тотальное эндопротезирование тазобедренного сустава), на фоне интраоперационной кровопотери (550 мл), наступило резкое ухудшение состояния, выраженная слабость, вялость, сонливость. Общее состояние тяжёлое, кожные покровы бледные, АД 51/37 мм рт.ст., частота сердечных сокращений (ЧСС) 42 уд./мин, сатурация кислорода (SpO2) 98%. ЭКГ — без признаков нарушения коронарного кровообращения. Состояние оценено как ортостатическая гипотензия на фоне вертикализации; назначены глюкокортикостероиды, препараты желатина; состояние улучшилось — АД 90/60 мм рт.ст., ЧСС 60 уд./мин.
По опыту обычный объем кровопотери при данной операции составляет ~200 мл. В данном случае объем превышен ввиду технических особенностей хода операции: смена инструментов, подбор имплантата под индивидуальные размеры и анатомические особенности — иногда это возможно только интраоперационно, — что привело к увеличению продолжительности операции и, соответственно, к большей кровопотере.
27.06.2023 назначен осмотр врача-кардиолога; определена клиническая вероятность тромбоэмболии легочной артерии (индекс Wells — 4,5 балла, вероятность средняя); проведена компьютерная томография (КТ)-ангиография легочных артерий — признаков тромбоэмболии крупных и средних артерий обоих легких не выявлено.
На ЭКГ в отсутствие клинических проявлений: признаки диффузной субэндокардиальной ишемии миокарда (ЧСС 77 уд./мин, ишемическая, горизонтальная депрессия ST от -1 до -2,5 мм в I, II, V3-V6 отведениях, одиночная предсердная экстрасистолия) (рисунок 1 А, Б). Повторная ЭКГ через 1,5 ч — ST на изолинии (рисунок 1 В); при ЭхоКГ зон нарушения локальной сократимости миокарда ЛЖ не выявлено; биомаркеры некроза миокарда в пределах референсных значений (таблица 1); показаний к экстренной КАГ не определено (рисунок 1 А, Б, В).
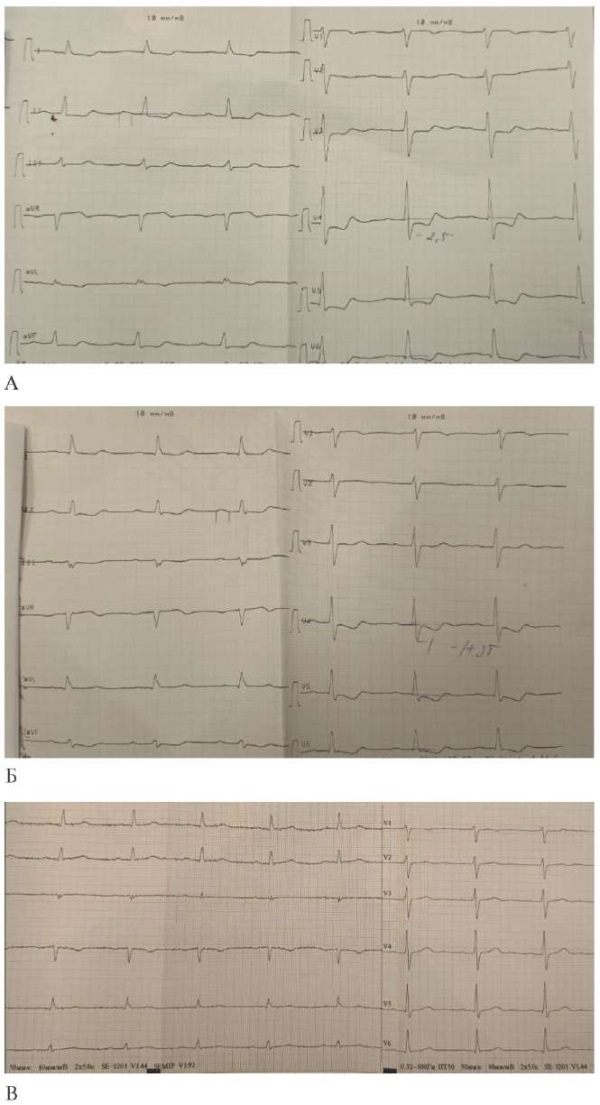
Рис. 1 ЭКГ пациентки от 27.06.2023: А) в 09:11 ч; Б) в 09:32 ч; В) в 11:13 ч.
Примечание: ЭКГ — электрокардиограмма.
Назначены суточное мониторирование ЭКГ, ЭКГ, тропонин I (TnI), уровень которого определяли высокочувствительным методом (hsTnI) в динамике. Уменьшена суточная доза β-блокаторов, проведена инфузия нитроглицерина, назначена ацетилсалициловая кислота 100 мг/сут., нефракционированный гепарин (5000 МЕ/мл внутривенно (в/в) болюс). С учётом признаков постгеморрагической анемии средней степени тяжести (уровень гемоглобина до операции — 125 г/л) проведена внутривенная инфузия эритроцитарной массы.
Суточное мониторирование ЭКГ от 27-28.06.2023: субмаксимальная ЧСС по возрасту не достигнута, минимальная ЧСС 57 уд./мин ночью. Зарегистрированы 42 одиночных наджелудочковых политопных, 8 одиночных мономорфных желудочковых экстрасистол; выраженная ишемическая горизонтальная депрессия ST-T в отведениях от передней, боковой стенки ЛЖ при пороговой ЧСС 68 уд./мин в период активности и ночью до -2,9 мм, общей продолжительностью 169 мин, всего эпизодов — 4, в т.ч. длительные (рисунок 2).
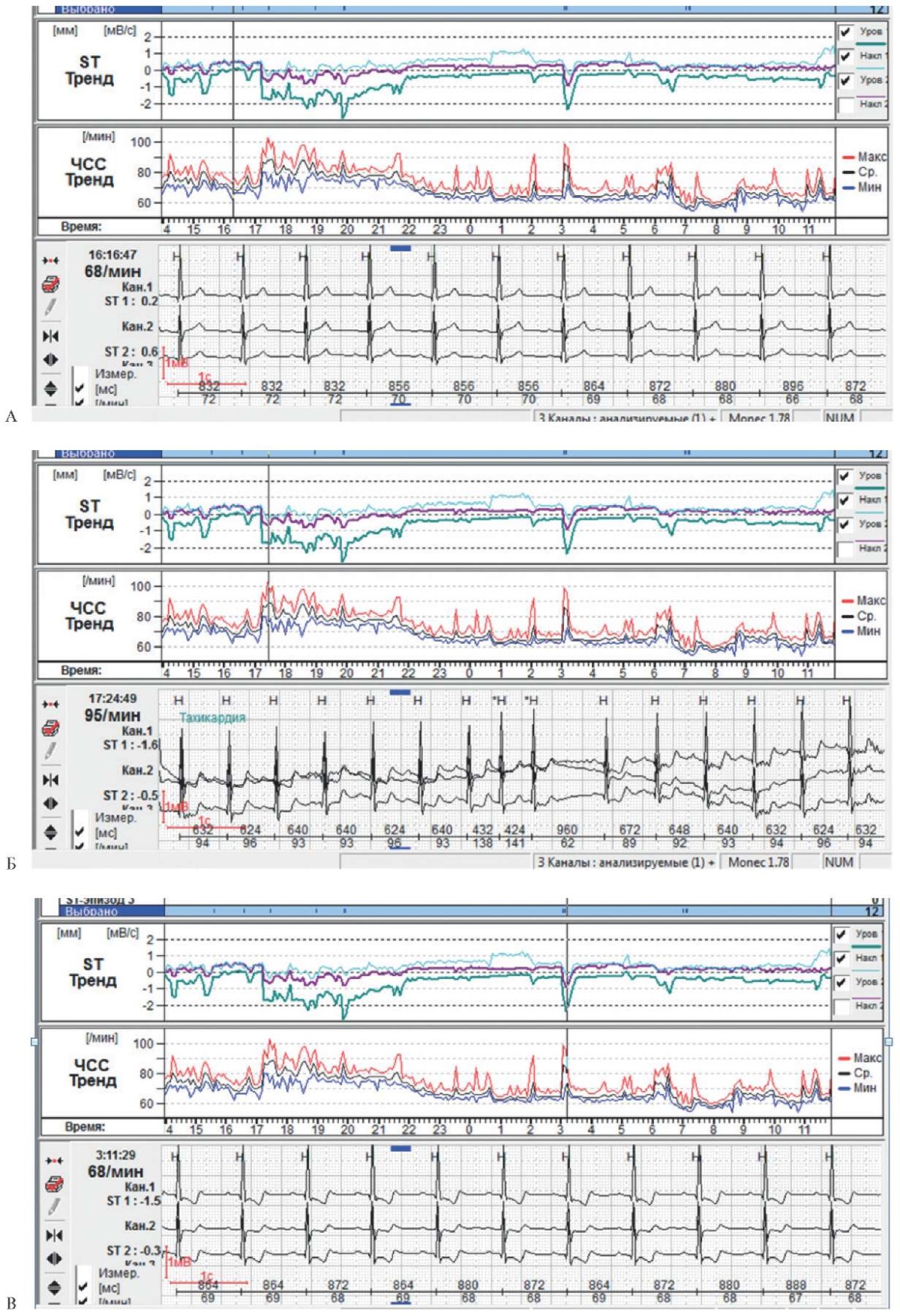
Рис. 2 Фрагменты СМЭКГ пациентки, 27-28.06.2023: А) и Б) — вечернее время, В) ночное время.
Примечание: СМЭКГ — суточное мониторирование электрокардиограммы, ЧСС — частота сердечных сокращений. Цветное изображение доступно в электронной версии журнала.
28.06.2023 впервые зарегистрирован уровень hsTn I 3,3 нг/мл.
Диагностирована ИБС: острый ИМ (hsTnI-положительный), безболевая ишемия миокарда (порог ишемии 68 уд./мин). Осложнения: хроническая сердечная недостаточность (ХСН) с фракцией выброса (ФВ) 61%, стадия I, функциональный класс (ФК) II. В течение 28.06.2023 — увеличение уровня hsTnI в динамике; повторные ЭхоКГ и ЭКГ — без изменений. Сохранялись признаки постгеморрагической анемии средней степени тяжести (таблица 2), повторно проведена в/в инфузия эритроцитарной массы.
Таблица 2
Динамика отдельных лабораторных показателей
|
Показатель/ед.изм. |
Норма |
27.06.2023 |
27.06.2023 |
28.06.2023 |
28.06.2023 |
29.06.2023 |
|
hsTnI, нг/мл |
<0,029 |
0,004-0,01 |
3,3-1,69 |
|||
|
hsTnT, нг/мл |
0-14 |
9,04 |
333,1-272,6 |
|||
|
NT-proBNP, пг/мл |
<125 |
87,7 |
788 |
|||
|
D-димер, пг/мл |
<500 |
>5000 |
2012 |
|||
|
Hb, г/л |
125 |
94 |
77 |
97-98 |
||
|
Гематокрит, % |
43,3 |
28,3 |
24,3 |
29,3 |
32,6 |
Примечание: Hb — гемоглобин, hsTnI — тропонин I, определенный высокочувствительным методом, hsTnT — тропонин T, определенный высокочувствительным методом, NT-proBNP — N-концевой промозговой натрийуретический пептид.
С учётом острой сердечно-сосудистой недостаточности от 26.06.2023 и прироста уровня hsTnI от 28.06.2023 при отсутствии ЭКГ-признаков ишемии и ЭхоКГ-данных за локальные нарушения сократимости с целью исключения МП ишемического генеза и для проведения КАГ пациентка направлена в Региональный сосудистый центр № 2. ЭКГ в приемном отделении — без признаков нарушения коронарного кровоснабжения; ЭхоКГ зон гипокинезии не выявила; уровень TnТ, определенного высокочувствительным методом (hsTnТ), 0,286 при норме до 0,05 нг/мл оценен как обусловленный проведенной операцией, в связи с чем получен отказ в госпитализации; пациентка переведена обратно в Центр.
29.06.2023 объективный статус — без изменений. Данная клиническая ситуация рассматривалась как МП миокарда при несердечных операциях в раннем послеоперационном периоде на фоне отсутствия клинической симптоматики (таблица 2). По итогам телемедицинской консультации пациентка переведена в Региональный сосудистый центр № 1 для проведения КАГ; диагностировано многососудистое атеросклеротическое поражение коронарного русла с диссекцией в дистальном отделе правой КА (ПКА), правый тип коронарного кровоснабжения. Подтвержден основной диагноз — ИБС: острый циркулярный ИМ без подъема сегмента ST от 26.06.2023; атеросклероз КА. КАГ от 29.06.2023: хроническая тотальная окклюзия передней нисходящей артерии (ПНА); стенозы: ствол левой КА (95%); 1 диагональная ветвь (1ДВ) (до 80%); огибающая артерия (до 75%); ветвь тупого края 1 (ВТК1) (80%); ВТК2 (до 90%); ПКА (до 95%), диссекция в дистальном отделе. Осложнение: внезапная остановка кровообращения; фибрилляция желудочков от 29.06.2023; восстановление синусового ритма — электроимпульсная терапия 200 Дж. ХСН IIА с ФВ (65%) ФК III.
07.07.2023 — перевод в кардиохиругическое отделение Республиканского кардиологического диспансера; телемедицинская консультация с Федеральным центром сердечно-сосудистой хирургии (г. Пенза) с последующим проведением 12.09.2023 аортокоронарного шунтирования (5 — маммарокоронарное шунтирование (МКШ)-ПНА, ИМВ (интермедиальная ветвь), ЗБВ (заднебоковая ветвь), ЗНА (задняя нисходящая артерия) ЗБВ от ПКА); подтвержден мультифокальный атеросклероз (атеросклеротическое стенозирование артерий нижних конечностей со стенозами ≥30-80% в правой подколенной артерии).
05.12.2023 в Центре при амбулаторном осмотре врачом-кардиологом при невысокой вероятности наличия ХСН с ФВ по шкале Н2FPEF (1 балл) оценен уровень N-концевого промозгового натрийуретического пептида (NT-proBNP) (325,6 пг/мл); назначен эмпаглифлозин 10 мг/сут.; продолжена двойная дезагрегантная терапия; оценен риск периоперационных ССО (по RCRI и Gupta MICA — средний) перед плановым эндопротезированием левого тазобедренного сустава, которое рекомендовано выполнить в условиях многопрофильного стационара.
Клинический диагноз
Предварительный клинический диагноз: МП при несердечных операциях. Конкурирующий диагноз: ИБС: острый ИМ (перипроцедурный), циркулярный, hsTnI-положительный. Осложнения: ХСН с сохраненной ФВ (61%), стадия I, ФК II. Сопутствующий диагноз: гипертоническая болезнь, III стадии, контролируемая АГ; атеросклероз аорты с переходом на аортальный клапан, риск 4 (очень высокий), целевое АД — 120-130 мм рт.ст.; сахарный диабет тип 2, целевой НbА1с <7,0% достигнут. Конкурирующий диагноз: состояние после тотального эндопротезирования правого тазобедренного сустава от 26.06.2023; постгеморрагическая анемия средней степени тяжести; медикаментозная/ортостатическая гипотензия и брадиаритмия с ЧСС до 42 уд./мин от 26.06.2023.
Динамика и исходы
После проведенной хирургической реваскуляризации миокарда состояние пациентки удовлетворительное, жалоб нет, наблюдается у врача-кардиолога, получает рекомендованную терапию, готовится к плановому эндопротезированию левого тазобедренного сустава.
Обсуждение
Уникальность клинического случая безболевого 95%-го поражения ствола левой КА (ЛКА) (и в целом тяжелого 3-сосудистого, прогностически крайне неблагоприятного, поражения КА) состоит в отсутствии клинических симптомов ИМ при наличии лабораторных признаков повреждения миокарда.
Ключевыми особенностями оказания медицинской помощи пациентке явились невозможность оценки функциональной способности в силу ограничений физической активности по основному заболеванию опорно-двигательного аппарата и, соответственно, невозможность выполнения нагрузочного теста; "пропущенное" поражение ствола ЛКА — вследствие вышеуказанных причин. Недостатки медицинской помощи — поздняя реваскуляризация миокарда.
В научной литературе недостаточно работ о диагностированных случаях безболевого перипроцедурного ИМ после несердечных хирургических вмешательств. По данным Kashlan B, et al. (2024), их частота составляет 1% [13]. Повреждение миокарда после несердечной операции, по результатам исследования de Oliveira Gomes BF, et al. (2023), увеличивает риск смерти в течение 30 сут. [14].
При подготовке к плановому несердечному оперативному вмешательству на амбулаторном этапе необходимо оценивать риски ССО; при подозрении на ИБС — определять предтестовую и клиническую вероятность и принимать решение о проведении дополнительных неинвазивных и инвазивных тестов; проводить терапию сердечно-сосудистых заболеваний с достижением целевых показателей холестерина липопротеинов низкой плотности, АД, HbA1c. На наш взгляд, данные требования учитываются не всегда, и возможности существующих шкал оценки риска выявлять прогностически крайне неблагоприятное поражение коронарных артерий ограничены. Так, согласно результатам исследования Bularga A, et al. (2021), только 32% клиник в 37 странах широко применяют оценку предтестовой вероятности ИБС [15].
На основании уровня повышения hsTnТ, наличия симптомов ишемии и риска развития кровотечений у пациента после несердечного вмешательства должно приниматься решение о показаниях к проведению КАГ с целью дифференциальной диагностики между ишемическим и неишемическим повреждением миокарда, что особенно важно в послеоперационном периоде после несердечного хирургического вмешательства [16].
Заключение
Представленный клинический случай показал целесообразность предоперационной оценки сердечно-сосудистых рисков и необходимость рутинного контроля ЭКГ, что способствовало выявлению безболевого перипроцедурного ИМ, проведению своевременной оптимальной диагностической и лечебной стратегии и, в итоге, сохранению жизни пациентки.
Прогноз для пациента: благоприятный с учётом хирургической реваскуляризации миокарда и рекомендованной терапии ИБС, АГ, ХСН.
Информированное согласие. От пациента получено письменное добровольное информированное согласие на публикацию результатов его обследования и лечения (дата подписания 23.06.2023).
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Бойцов С. А., Барбараш О. Л., Вайсман Д. Ш. и др. Клиническая, морфологическая и статистическая классификация ишемической болезни сердца. Консенсус Российского кардиологического общества, Российского общества патологоанатомов и специалистов по медицинской статистике. https://scardio.ru/content/Guidelines/Klass_IBS_2020.pdf (08.10.2024).
2. Клинические рекомендации Министерства здравоохранения Российской Федерации "Стабильная ишемическая болезнь сердца". 2020. Доступно по ссылке: https://cr.minzdrav.gov.ru/schema/155_1 (дата обращения 25.09.2024).
Список литературы
1. Сумин А. Н., Дупляков Д. В., Белялов Ф. И. и др. Рекомендации по оценке и коррекции сердечно-сосудистых рисков при несердечных операциях 2023. Российский кардиологический журнал. 2023;28(8):5555. doi:10.15829/1560-4071-2023-5555. EDN MQQWMW.
2. International Surgical Outcomes Study group. Global patient outcomes after elective surgery: prospective cohort study in 27 low-, middle- and high-income countries. Br J Anaesth. 2016;117(5):601-9. doi:10.1093/bja/aew316.
3. Smilowitz NR, Gupta N, Guo Y, et al. Perioperative acute myocardial infarction associated with non-cardiac surgery. Eur Heart J. 2017;38(31):2409-17. doi:10.1093/eurheartj/ehx313.
4. Sazgary L, Puelacher C, Lurati Buse G, et al. BASEL-PMI Investigators. Incidence of major adverse cardiac events following non-cardiac surgery. Eur Heart J Acute Cardiovasc Care. 2021; 10(5):550-8. doi:10.1093/ehjacc/zuaa008.
5. Абдрахманова А. И., Амиров Н. Б., Сайфуллина Г. Б. Безболевая ишемия миокарда (обзор литературы). Вестник современной клинической медицины. 2015;8(6):103-15.
6. Карпов Ю. А., Барбараш О. Л., Бощенко А. А. и др. Рекомендации ЕSC по диагностике и лечению хронического коронарного синдрома, 2020 год; Евразийские клинические рекомендации по диагностике и лечению стабильной ишемической болезни сердца (2020-2021). Евразийский кардиологический журнал. 2021;3(36):54-93. doi:10.38109/2225-1685-2021-3-54-93. EDN GRYBPE.
7. Щеглова А. В., Сумин А. Н., Олейник П. А. и др. Результативность оценки предтестовой и клинической вероятности у больных с подозрением на ИБС в реальной клинической практике. Уголь. 2023;S12:135-42. doi:10.18796/0041-5790-2023-S12-135-142.
8. Аншелес А. А., Сергиенко И. В., Денисенко-Канкия Е. И. и др. Предтестовая оценка вероятности ишемической болезни сердца. Вестник Национального медико-хирургического центра им. Н. И. Пирогова. 2020;15(3-2):124-32. doi:10.25881/BPNMSC.2020.30.69.023.
9. Ройтберг Г. Е., Сластникова И. Д., Давыдова А. Ш. и др. Различные прогностические шкалы предтестовой вероятности в выявлении больных низкого риска ишемической болезни сердца. Лечебное дело. 2022;3-4:95-102.
10. Ройтберг Г. Е., Сластникова И. Д., Шархун О. О. и др. Значение факторов риска сердечно-сосудистых заболеваний в предтестовой оценке ишемической болезни сердца. Терапия. 2023;9(1-63):70-7. doi:10.18565/therapy.2023.1.70-77.
11. Сумин А. Н., Щеглова А. В. Оценка предтестовой и клинической вероятности в диагностике хронического коронарного синдрома — что нового? Рациональная фармакотерапия в кардиологии. 2022;18(1):92-6. doi:10.20996/1819-6446-2022-02-04.
12. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений (ВТЭО). Утв. совещанием экспертов 20.05.2015г. Москва. Флебология. 2015; 9(4-2):2-52.
13. Kashlan B, Kinno M, Syed M. Perioperative myocardial injury and infarction after noncardiac surgery: a review of pathophysiology, diagnosis, and management. Front Cardiovasc Med. 2024;11: 1323425. doi:10.3389/fcvm.2024.1323425.
14. de Oliveira Gomes BF, da Silva TMB, Dutra GP, et al. Late Mortality After Myocardial Injury in Critical Care Non-Cardiac Surgery Patients Using Machine Learning Analysis. Am J Cardiol. 2023;204:70-6. doi:10.1016/j.amjcard.2023.07.044.
15. Bularga A, Saraste A, Fontes-Carvalho R, et al. EACVI survey on investigations and imaging modalities in chronic coronary syndromes. Eur Heart J Cardiovasc Imaging. 2021;22(1): 1-7. doi:10.1093/ehjci/jeaa300. PMID: 33165600; PMCID: PMC7758034.
16. Толпыгина С. Н., Марцевич С. Ю. Стратификация риска сердечно-сосудистых осложнений при стабильной ишемической болезни сердца. Клиницист. 2020;14(1-2):24-33. doi:10.17650/1818-8338-2020-14-1-2-24-33.
Об авторах
Э. В. ИвановаРоссия
Эльза Владимировна Иванова — зав. поликлиникой — врач-кардиолог
Чебоксары
А. В. Арсентьев
Россия
Андрей Владимирович Арсентьев — зав. отделением анестезиологии-реанимации с палатами реанимации и интенсивной терапии, врач-анестезиолог-реаниматолог
Чебоксары
М. К. Илларионова
Россия
Марина Константиновна Илларионова — врач функциональной диагностики
Чебоксары
Дополнительные файлы
- Безболевая форма ишемической болезни сердца — случайная находка при рутинном обследовании пациента.
- Требуется выявление факторов риска ишемической болезни сердца и риска сердечно-сосудистых осложнений у пациентов перед несердечными хирургическими вмешательствами.
- При росте уровня тропонина и отсутствии электрокардиографических, эхокардиографических данных за ишемию для дифференциальной диагностики ишемического и неишемического повреждения миокарда необходимо оценить показания к проведению коронароангиографии.
- Клинический случай иллюстрирует пример своевременной диагностики и лечения пациентки с безболевой формой перипроцедурного инфаркта миокарда, диагностированного после травматолого-ортопедической операции.
Рецензия
Для цитирования:
Иванова Э.В., Арсентьев А.В., Илларионова М.К. Безболевой перипроцедурный инфаркт миокарда при несердечной операции. Клинический случай. Кардиоваскулярная терапия и профилактика. 2025;24(2):4143. https://doi.org/10.15829/1728-8800-2025-4143. EDN: IUXTYG
For citation:
Ivanova E.V., Arsentyev A.V., Illarionova M.K. Silent periprocedural myocardial infarction during non-cardiac surgery: a case report. Cardiovascular Therapy and Prevention. 2025;24(2):4143. (In Russ.) https://doi.org/10.15829/1728-8800-2025-4143. EDN: IUXTYG
JATS XML

























































