Перейти к:
Кардиопульмональное нагрузочное тестирование у пациентов с прекапиллярной легочной гипертензией, имеющих неблагоприятный прогноз
https://doi.org/10.15829/1728-8800-2024-4088
EDN: QLXMDS
Аннотация
Цель. Провести сопоставление клинических и гемодинамических параметров с выживаемостью инцидентных больных идиопатической легочной артериальной гипертензией (ИЛАГ) и хронической тромбоэмболической легочной гипертензией (ХТЭЛГ), имеющих прогностически неблагоприятный паттерн показателей кардиопульмонального нагрузочного тестирования (КПНТ).
Материал и методы. В исследование включены 48 инцидентных случаев с верифицированным диагнозом ИЛАГ (n=18) и ХТЭЛГ (n=30). Все пациенты обследованы в соответствии с рекомендациями Европейского общества кардиологов и Европейского респираторного общества 2015г. В качестве критерия включения выбран вентиляторный эквивалент по диоксиду углерода (СО2) по данным КПНТ (VE/VCO2) >44, свидетельствующий о неблагоприятном прогнозе пациентов.
Результаты. VE/VCO2 у обследованных пациентов ИЛАГ и ХТЭЛГ в среднем составил 70,6±0,8 и не различался в исследуемых группах. Гемодинамические параметры пациентов с ИЛАГ и ХТЭЛГ также указывали на высокий риск развития неблагоприятных событий: сердечный индекс 1,9±0,1 и 1,8±0,1 л/мин/м2, соответственно (р=0,3). Пиковое потребление кислорода, уровень анаэробного порога, доставка кислорода на объем выполненной работы были снижены в обеих группах. Но у пациентов с ИЛАГ отсутствовало снижение вентиляции мертвого пространства и степень десатурации при физической нагрузке была больше, чем у пациентов с ХТЭЛГ. Пациенты с ХТЭЛГ имели лучшую выживаемость по сравнению с больными ИЛАГ: 1 год — 89 vs 83%, 3 год — 84 vs 65%, 5 год — 73 vs 35%, 7 год — 55 vs 36%.
Заключение. Среди пациентов с ИЛАГ и ХТЭЛГ, имеющих неблагоприятный прогноз, пациенты с ИЛАГ при физической нагрузке демонстрируют более выраженное снижение резервных возможностей сердечно-сосудистой и дыхательной систем, что негативно отражается на выживаемости пациентов. КПНТ может быть ценным неинвазивным методом стратификации риска летальных исходов у пациентов с ИЛАГ и ХТЭЛГ.
Ключевые слова
Для цитирования:
Березина А.В., Злобина И.С., Гончарова Н.С., Симакова М.А., Лапшин К.Б., Моисеева О.М. Кардиопульмональное нагрузочное тестирование у пациентов с прекапиллярной легочной гипертензией, имеющих неблагоприятный прогноз. Кардиоваскулярная терапия и профилактика. 2024;23(9):4088. https://doi.org/10.15829/1728-8800-2024-4088. EDN: QLXMDS
For citation:
Berezina A.V., Zlobina I.S., Goncharova N.S., Simakova M.A., Lapshin K.B., Moiseeva O.M. Cardiopulmonary exercise testing in patients with precapillary pulmonary hypertension with an unfavorable prognosis. Cardiovascular Therapy and Prevention. 2024;23(9):4088. (In Russ.) https://doi.org/10.15829/1728-8800-2024-4088. EDN: QLXMDS
Введение
Среди основных вариантов легочной гипертензии (ЛГ) наибольший интерес представляют идиопатическая легочная артериальная гипертензия (ИЛАГ) и хроническая тромбоэмболическая ЛГ (ХТЭЛГ), связанная с обструкцией ветвей легочной артерии (ЛА) [1]. Несмотря на различия в патогенезе и морфологии поражения сосудов легких, ИЛАГ и ХТЭЛГ относятся к прекапиллярному гемодинамическому варианту ЛГ [1]. В качестве ключевого механизма патогенеза ИЛАГ рассматриваются повреждение и дисфункция эндотелия, ассоциированные с развитием вазоконстрикторных реакций, ремоделированием артерий и артериол малого круга кровообращения (МКК) и редукцией микроциркуляторного русла за счет облитерации мелких артерий [2][3]. В отличие от ИЛАГ при ХТЭЛГ к увеличению легочного сосудистого сопротивления (ЛСС) приводит окклюзия проксимальных ЛА фиброзно-измененными тромботическими массами в сочетании с вторичной микроваскулопатией [4]. Течение любого варианта ЛГ определяется выраженностью структурных изменений в сосудах МКК и адаптационными возможностями правого желудочка. При стратификации риска пациентов с ЛГ традиционно проводят оценку клинических проявлений заболевания, физической работоспособности, уровня N-концевого промозгового натрийуретического пептида (NT-proBNP) как маркера сердечной недостаточности, гемодинамических показателей, а также структурно-функциональных изменений сердца, в первую очередь, правых камер сердца по данным эхокардиографии (ЭхоКГ) или магнитно-резонансной томографии сердца [1]. Несмотря на высокую предсказательную ценность показателей гемодинамики и шкал стратификации риска летальных исходов [5], течение ИЛАГ и ответ на специфическую терапию у отдельных пациентов могут существенно различаться. Дополнительные возможности для ведения пациентов открывает кардиопульмональное нагрузочное тестирование (КПНТ), значение которого в диагностике и последующем наблюдении пациентов с ЛГ в настоящих рекомендациях недооценено. Недостаточно изучены и особенности патофизиологических механизмов сопряжения сердечно-сосудистой и респираторной систем, определяющие неблагоприятный прогноз больных с прекапиллярной ЛГ. Вместе с тем, оценка функциональной сопряженности кардиореспираторной системы и индивидуальных особенностей на метаболическом уровне с помощью КПНТ могут внести существенный вклад в понимание патофизиологических механизмов прогрессирования ИЛАГ и ХТЭЛГ, а также улучшить стратификацию риска летальных исходов и персонифицировать подбор лекарственной терапии [6-8]. Основным преимуществом КПНТ является неинвазивная объективизация функционального статуса и резервных возможностей сердечно-сосудистой, дыхательной и мышечной систем как с точки зрения доставки кислорода, так и его утилизации. Степень снижения резервных возможностей и, соответственно, ухудшение доставки кислорода в мышцы, приводящее к снижению переносимости физической нагрузки, служит объективным критерием тяжести и прогноза заболеваний.
Цель настоящего исследования — провести сопоставление клинических и гемодинамических параметров с выживаемостью инцидентных больных ИЛАГ и ХТЭЛГ, имеющих прогностически неблагоприятный паттерн показателей КПНТ.
Материал и методы
За период 2010-2023гг в проспективное одноцентровое исследование отобраны 48 инцидентных случаев (возраст пациентов от 20 до 73 лет) с верифицированным диагнозом ИЛАГ — 18 больных и ХТЭЛГ — 30 больных (таблица 1). В исследование включены пациенты, которые имели по результатам катетеризации правых камер сердца (КПКС) в соответствии с рекомендациями Европейского общества кардиологов и Европейского респираторного общества 2015г прекапиллярную ЛГ: среднее давление в легочной артерии (ДЛА) ≥25 мм рт.ст., ЛСС >3 ед. Вуда, а также вентиляторный эквивалент по диоксиду углерода(VE/VCO2) по данным КПНТ >44, свидетельствующий о неблагоприятном прогнозе [9].
Критериями невключения в исследование были легочная артериальная гипертензия иной этиологии, чем ИЛАГ; умеренные или тяжелые заболевания легких; ЛГ, ассоциированная с патологией левых отделов сердца; клинически значимые нарушения ритма и проводимости; установленные злокачественные новообразования; сахарный диабет; заболевания щитовидной железы; тяжелая дисфункция почек или печени, анемия или латентный железодефицит; воспалительные заболевания и психические расстройства.
Группы не различались по частоте артериальной гипертензии. Все исследования выполнены у пациентов с ИЛАГ до старта специфической медикаментозной терапии и у пациентов с ХТЭЛГ до хирургического лечения. В качестве фоновой терапии пациенты ИЛАГ и ХТЭЛГ получали петлевые диуретики и антагонисты альдостерона, пациенты с ХТЭЛГ дополнительно получали терапию варфарином. Достоверных различий в уровне гемоглобина среди пациентов ИЛАГ и ХТЭЛГ не выявлено: 153±18 и 148±15 г/л, соответственно (р=0,279).
Всем пациентам выполнено ЭхоКГ на аппарате VIVID 7 Dimension. Оценку правых камер сердца проводили по стандартному протоколу в соответствии с рекомендациями 2015г [10].
Гемодинамику оценивали в ходе КПКС с сосудистым доступом через яремную вену и использованием термодилюционного баллонного катетера Свана-Ганца (BBraun Сorodyn TD 7Fr). ЛСС рассчитывали по формуле: (среднее ДЛА — ДЗЛА (давление заклинивания в ЛА)/сердечный выброс. Комплексное исследование функции внешнего дыхания с определением стандартных и динамических показателей вентиляции и статических объемов легких выполняли на аппарате VIASYS Healthcare Hoechberg (Германия). Дополнительно оценивали диффузионную способность легких по монооксиду углерода с коррекцией на уровень гемоглобина. КПНТ проводили на велоэргометре с одновременной оценкой газообмена. Для газоанализа использовали метод breath-by-breath (анализ каждого дыхательного цикла в режиме реального времени) с помощью системы Oxycon Pro. Пациенты выполняли симптом-лимитированную, непрерывно-возрастающую физическую нагрузку (ФН) на велоэргометре с увеличением нагрузки на 10 Вт/мин. Регистрацию электрокардиограммы, определение насыщения крови кислородом (SpO2) с помощью пульсоксиметра проводили непрерывно в течение всего теста, мониторинг артериального давления (АД) проводили каждые 2 мин. Субъективные ощущения пациента оценивали по 10-балльной шкале Борга. Критериями прекращения ФН было достижение максимально возможной ФН или появление симптомов, лимитирующих ее выполнение: выраженная усталость, одышка, пресинкопальные состояния, нарушения ритма сердца, ишемические изменения на электрокардиограмме, боли за грудиной, снижение АД. Ответ сердечно-сосудистой и легочной систем на ФН оценивали по пиковому потреблению кислорода (VO2peak), приросту потребления кислорода в расчете на выполненную работу (ΔVO2/ΔW), потребление кислорода на уровне анаэробного порога (VO2 на АП), приросту частоты сердечных сокращений (ЧСС/VO2) во время ФН, кислородному пульсу (VO2/ЧСС), который является индексом ударного объема, парциальному давлению углекислого газа в конце выдоха (PETCO2peak), VE/VCO2 и уровню АД на пике ФН. Снижение объема вентиляции мертвого пространства при ФН определяли по изменению соотношения объема мертвого пространства к дыхательному объему (∆VD/VT) в покое и на пике нагрузки.
В соответствии с законодательством РФ и локальными актами НМИЦ им. В. А. Алмазова проведение ретроспективного когортного исследования не требует разрешения Этического комитета. Исследование отражает повседневную клиническую практику в рамках клинических рекомендаций по ведению пациентов с ЛГ [1][9]. Идентифицируемая информация о пациенте не была представлена в исследовании.
Статистический анализ. Демографические, клинические данные, показатели КПНТ, КПКС, ЭхоКГ и лабораторные данные сравнивали между больными ИЛАГ и ХТЭЛГ, а также между живыми и умершими пациентами в группе пациентов с ИЛАГ. Числовые показатели с нормальным распределением представлены в виде среднего арифметического значения (M) и стандартной ошибки (m); числовые показатели с распределением, отличным от нормального, — как медиана (Me) и интерквартильный размах (Q25; Q75). Для сравнения количественных данных двух независимых выборок использовали непараметрический U-критерий Манна-Уитни. Для сравнения категориальных показателей применяли критерий χ2 и точный двусторонний тест Фишера. Для оценки связей между анализируемыми параметрами был применен линейный корреляционный анализ. Критерием статистической достоверности получаемых результатов считали общепринятую в медицине величину р<0,05. Анализ выживаемости проводился с использованием кривых Каплана-Мейера и логарифмического рангового критерия для сравнения распределения выживаемости между пациентами. С помощью унивариантного регрессионного анализа Кокса оценивалась взаимосвязь исследуемых показателей с выживаемостью. Учитывая небольшую популяцию пациентов, множественный регрессионный анализ не проводили.
Статистическую обработку данных проводили с помощью программы SPSS Statistics 23.0 (USA).
Результаты
Пациенты с ИЛАГ были достоверно моложе по сравнению с больными ХТЭЛГ, с преобладанием пациентов женского пола. Все пациенты на момент выполнения КПНТ находились в III функциональном классе (ВОЗ) (таблица 1). У 93,3% больных ХТЭЛГ был выявлен долевой и/или сегментарный уровень поражений ЛА. VE/VCO2 составил — 70,6±0,8 в общей группе. При этом у 43,8% пациентов его значение было >44, а у 56,3% не определялся в связи с очень высокими значениями. По средним значениям VE/VCO2 больные ИЛАГ и ХТЭЛГ не различались.
Уровень NT-proBNP был достоверно выше у пациентов с ИЛАГ. У пациентов с ХТЭЛГ отмечено увеличение индекса объема левого предсердия и большие значения конечного диастолического размера левого желудочка (ЛЖ) по сравнению с пациентами с ИЛАГ. Достоверных различий в показателях, характеризующих состояние правого желудочка (ПЖ), не выявлено. Однако у всех пациентов с ИЛАГ нумеристически соотношение ПЖ и ЛЖ было бóльшим по сравнению с больными ХТЭЛГ (χ2=4,1, р=0,04).
Величины сердечного индекса и насыщения кислородом (сатурации) смешанной венозной крови (SvO2), которые традиционно рассматриваются в качестве предикторов неблагоприятного прогноза, были сопоставимы в исследуемых группах. Вместе с тем, ЛСС и SpO2 были более высокими у больных ИЛАГ, тогда как ДЗЛА и центральное венозное давление были значительно выше у пациентов с ХТЭЛГ. Выявлена тенденция к повышению среднего ДЛА у больных ИЛАГ (р=0,06). В обеих группах пациентов сердечный индекс и SvO2 были значительно снижены: ≤2,0 л/мин/м2 и SvO2 <60%, соответственно. По сравнению с ИЛАГ у больных ХТЭЛГ чаще регистрировались более высокие значения центрального венозного давления и более низкий уровень SvO2.
Показатели спирометрии и бодиплетизмографии находились в пределах референтных значений и достоверно не различались между анализируемыми группами. Диффузионная способность легких по монооксиду углерода была умеренно снижена как у больных ИЛАГ, так и ХТЭЛГ — 52,3±5,34 и 64,1±3,3%, соответственно (р>0,1).
Пиковое потребление кислорода, уровень АП, ΔVO2/ΔW в обеих группах были снижены относительно должных значений. У пациентов с ИЛАГ и ХТЭЛГ регистрировался нефизиологичный прирост сердечного выброса, что характеризовалось низким значением VO2/ЧСС и ускоренным приростом ЧСС. Легочный резерв был сохранен у подавляющего большинства пациентов, при том, что у всех пациентов наблюдалась гипервентиляция при нормальном паттерне дыхания. Вместе с тем, SpO2 на пике ФН достоверно снижалась у всех исследуемых пациентов. Однако степень десатурации при ФН была выше у больных ИЛАГ по сравнению с пациентами с ХТЭЛГ. Кроме того, у больных ИЛАГ соотношение VD/VT на пике ФН было больше, чем у больных ХТЭЛГ. Наряду с этим для больных ИЛАГ было характерно меньшее снижение ∆VD/VT при ФН, чем при ХТЭЛГ (таблица 2).
При проведении корреляционного анализа наиболее важные взаимосвязи установлены между величиной сердечного индекса и такими параметрами КПНТ, как VO2/ЧСС и VE/VCO2 (таблица 3). Разнонаправленность корреляционных связей у пациентов с ИЛАГ и ХТЭЛГ между другими гемодинамическими показателями и параметрами КПНТ можно объяснить различиями в патогенезе заболеваний и ограниченностью исследуемых выборок.
При анализе общей выборки пациентов с ЛГ методом линейного регрессионного анализа установлено, что показатель VE/VCO2 тесно связан с величиной сердечного индекса (r2=0,2, p=0,003), среднего ДЛА (r2=0,3, p=0,008), соотношением ПЖ и ЛЖ (r2=0,5, p=0,001), амплитудой движения кольца трикуспидального клапана как маркера систолической дисфункции ПЖ (r2=0,4, p=0,001); в то же время величина VO2peak находилась в зависимости от ЛСС и среднего ДЛА (r2=0,2; p=0,04) и (r2=0,6; p=0,001), соответственно.
В группе пациентов с ИЛАГ длительность заболевания от появления симптомов до выполнения КПНТ составляла 2,6±0,4 года (6 мес.; 7 лет). За период наблюдения с 2008 по 2021гг в группе пациентов ИЛАГ (n=18) умерли 10 (62,5%) больных, с двумя пациентами контакт потерян. Основной причиной летальных исходов стало прогрессирование заболевания с развитием тяжелой правожелудочковой сердечной недостаточности. Умершие пациенты с ИЛАГ отличались большей длительностью заболевания — 9,1±1,1 vs 5,6±1,3 года (р=0,03), более высокими цифрами среднего ДЛА — 69,5±3,5 vs 55,3±2,9 мм рт.ст. (р=0,01) и более низкой диффузионной способностью легких — 43,1±5, vs 66,5±12,3% (р=0,04) по сравнению с живыми.
В группе пациентов с ХТЭЛГ длительность заболевания от появления симптомов до выполнения КПНТ составляла 5,5±0,6 года (12 мес.;10 лет). За период наблюдения с 2006 по 2022гг умерли 4 (13,3%) пациента. Периоперационные осложнения (n=2) и прогрессирование правожелудочковой сердечной недостаточности (n=2) были причинами смерти у 4 пациентов с ХТЭЛГ. В остальных случаях (n=26, 86,7%) всем пациентам успешно выполнено хирургическое лечение ХТЭЛГ (тромбэндартерэктомия и/или баллонная ангиопластика).
Пациенты с ХТЭЛГ имели лучшую выживаемость (р=0,08) по сравнению с больными ИЛАГ: на 1 год — 89 vs 83%, на 3 года — 84 vs 65%, на 5 лет — 73 vs 35%, на 7 лет — 55 vs 36%, соответственно (рисунок 1).
По данным унивариантного регрессионного анализа у пациентов с ИЛАГ выявлена взаимосвязь возраста, VO2peak, дыхательного резерва и VO2 на АП с выживаемостью (таблица 4). Однако отношение шансов (odds ratio, OR) в полученных корреляционных взаимосвязях близко к 1,0. Не выявлены достоверные корреляционные взаимосвязи между показателями ЭхоКГ, бодиплетизмографии, диффузионной способности легких и выживаемостью у пациентов с ИЛАГ, что, вероятно, связано с небольшим объемом выборки и включением пациентов с критериями исходно высокого риска по КПНТ.
Таблица 1
Клиническая характеристика пациентов
Показатель, M±m | ИЛАГ (n=18) | ХТЭЛГ (n=30) | р |
Возраст, лет | 39,3±3,1 | 52,3±2,4 | 0,002 |
Женский пол, n (%) | 18 (50) | 30 (13,3) | 0,03 |
Индекс массы тела, кг/м2 | 22,8±4,0 | 24,5±3,7 | 0,140 |
АГ, n (%) | 2 (11) | 9 (30) | 0,116 |
III ФК, n (%) | 18 (100) | 30 (100) | |
NT-proBNP (пг/мл) Me (Q25; Q75) | 1364,0 (859,8; 3017) | 1057,0 (260,8; 2719) | 0,04 |
ЭхоКГ данные | |||
Индекс объема левого предсердия, мл/м2 | 24,4±2,7 | 34±8,4 | 0,02 |
КДР ЛЖ, мм | 36,6±1,4 | 42,5±1,0 | 0,003 |
Базальный размер ПЖ, мм | 52,3±3 | 53,8±1,5 | 0,6 |
ПЖ:ЛЖ соотношение | 1,5±0,09 | 1,3±0,05 | 0,1 |
ТАPSE, мм | 14,8±1,1 | 14,7±0,6 | 0,9 |
РСДЛА, мм рт.ст. | 92,7±5,4 | 95,1±3,5 | 0,6 |
Данные катетеризации правых камер сердца | |||
Среднее ДЛА, мм рт.ст. | 62,8±2,9 | 56,3±1,4 | 0,06 |
ДЗЛА, мм рт.ст. | 9,7±1,4 | 13,5±0,7 | 0,001 |
ЛСС, ед. Вуда | 18,3±1,7 | 13,4±0,8 | 0,02 |
Давление в ПП, мм рт.ст. | 10,8±1,5 | 17,0±1,4 | 0,01 |
СИ, л/мин/м2 | 1,9±0,1 | 1,8±0,1 | 0,3 |
SpO2, % | 93,5±0,7 | 91,1±0,7 | 0,03 |
SvO2, % | 60,3±3,2 | 54,3±1,8 | 0,1 |
Примечание: данные представлены в виде средней и стандартной ошибки средней (M±m), если не указано иное. АГ — артериальная гипертензия, ДЗЛА — давление заклинивания легочной артерии, ДЛА — давление в легочной артерии, КДР — конечный диастолический размер, ЛЖ — левый желудочек, ЛСС — легочное сосудистое сопротивление, Ме — медиана, ПЖ — правый желудочек, ПЖ:ЛЖ — отношение базальных размеров ПЖо и ЛЖ в 4-камерной позиции, ПП — правое предсердие, РСДЛА — расчетное систолическое ДЛА, СИ — сердечный индекс, ФК — функциональный класс, ЭхоКГ — эхокардиографические, NT-proBNP — N-концевой промозговой натрийуретический пептид, SpO2 — насыщение крови кислородом по данным пульсоксиметрии, SvO2 — насыщение кислородом смешанной венозной крови, TAPSE — амплитуда движения латеральной части фиброзного кольца трикуспидального клапана.
Таблица 2
Показатели кардиореспираторного теста
Показатель | ИЛАГ (n=18), M±m | ХТЭЛГ (n=30), M±m | р |
VO2peak%Д (норма >85%) | 36,5±2,8 | 38,0±1,7 | 0,4 |
VO2на АП, %Д (норма >85%) | 31,6±2,4 | 33,6±2,0 | 0,4 |
VO2/W (норма 8-10 мл/мин/вт) | 6,27±0,5 | 7,2±0,4 | 0,2 |
О2пульс, %Д (норма >85%) | 51,8±13,9 | 48,4±9,4 | 0,1 |
ЧСС/VO2 (норма 4-6 уд./мл/кг) | 12,4±3,1 | 12,3±2,5 | 0,7 |
VE/VCO2 (норма <34) | 68,9±1,4 | 71,6±1,1 | 0,1 |
BR (норма 28%) | 49,5±3,7 | 43,5±2,5 | 0,1 |
VD/VTpeak, % | 23,2±0,8 | 17,9±1,2 | 0,005 |
ΔVD/VT, % | 0,8±1,7 | 5,8±1,1 | 0,03 |
SpO2peak, % | 86,6±1,1 | 90,3±0,7 | 0,008 |
ΔSpO2peak, % | 6,3±0,7 | 4,3±0,7 | 0,03 |
Примечание: VO2peak %Д — пиковое потребление кислорода, выраженное в процентах от должной, VO2 на АП, %Д — потребление кислорода на уровне анаэробного порога, выраженное в процентах от должной, VO2/W — доставка кислорода на объем выполненной работы, О2пульс — кислородный пульс, ЧСС/VO2 — прирост частоты сердечных сокращений при ФН, VE/VCO2 — вентиляторный эквивалент по СО2, BR — резерв дыхания, VD/VT — соотношение объема вентиляции мертвого пространства к дыхательному объему на пике ФН, ΔVD/VT — степень изменения значений соотношения объема вентиляции мертвого пространства к дыхательному объему между покоем и пиком ФН, SpO2peak — сатурация кислорода на пике ФН, ΔSpO2peak — степень изменения значений показателя между покоем и пиком.
Таблица 3
Взаимосвязи гемодинамических параметров с показателями кардиопульмонального нагрузочного тестирования
Показатель | ИЛАГ, n=18 | ХТЭЛГ, n=30 | |||
r | p | r | p | ||
1 | VO2peak — СИ | 0,09 | 0,72 | 0,34 | 0,03 |
2 | VO2/W — ЛСС | -0,22 | 0,37 | -0,39 | 0,04 |
3 | О2пульс — СИ | 0,53 | 0,02 | 0,42 | 0,02 |
4 | О2пульс — КДР ЛЖ | 0,5 | 0,04 | 0,52 | 0,003 |
5 | О2пульс — ЛСС | -0,44 | 0,07 | -0,52 | 0,004 |
6 | О2пульс — ПЖ:ЛЖ | -0,04 | 0,89 | -0,42 | 0,02 |
7 | VE/VCO2 — СИ | -0,53 | 0,02 | -0,43 | 0,02 |
8 | VE/VCO2 — TAPSE | -0,56 | 0,02 | 0,09 | 0,65 |
9 | VO2peak — среднее ДЛА | 0,3 | 0,23 | 0,57 | 0,001 |
10 | VD/VTpeak — SvO2 | -0,04 | 0,92 | -0,42 | 0,02 |
Примечание: ДЛА — давление в легочной артерии, ИЛАГ — идиопатическая легочная артериальная гипертензия, КДР — конечный диастолический размер, ЛЖ — левый желудочек, ЛСС — легочное сосудистое сопротивление, ПЖ — правый желудочек, СИ — сердечный индекс, ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия, ΔVO2/ΔW — потребление кислорода на объем выполненной работы, VE/VCO2 — вентиляторный эквивалент СО2, О2пульс — кислородный пульс, VD/VTpeak — соотношение объема вентиляции мертвого пространства к дыхательному объему на пике физической нагрузки, VO2peak — пиковое потребление кислорода, TAPSE — амплитуда движения латеральной части фиброзного кольца трикуспидального клапана.
Таблица 4
Результаты унивариантного регрессионного анализа в группе пациентов с ИЛАГ
β | SD | 95% ДИ | t-знач. | Wald test. | p | OR | 95% ДИ | |||
Нижняя | Верхняя | Нижняя | Верхняя | |||||||
%ДVO2peak | -0,081 | 0,036 | -0,151 | -0,011 | -2,254 | 5,081 | 0,024 | 0,923 | 0,860 | 0,990 |
BR | 0,043 | 0,022 | 0,001 | 0,086 | 1,970 | 3,882 | 0,049 | 1,044 | 1,000 | 1,089 |
%ДVO2 на АП | -0,079 | 0,041 | -0,160 | 0,001 | -1,927 | 3,715 | 0,054 | 0,924 | 0,852 | 1,001 |
Возраст | -0,081 | 0,037 | -0,153 | -0,009 | -2,208 | 4,8756 | 0,027 | 0,922 | 0,858 | 0,991 |
Примечание: ДИ — доверительный интервал, ИЛАГ — идиопатическая легочная артериальная гипертензия, BR — резерв дыхания, SD — стандартная ошибка, Wald test — статистический тест Вальда, OR — odds ratio (отношение шансов), %ДVO2peak — процент должного пикового потребления кислорода, %ДVO2 на АП — потребление кислорода на уровне анаэробного порога, выраженное в процентах от должной величины.
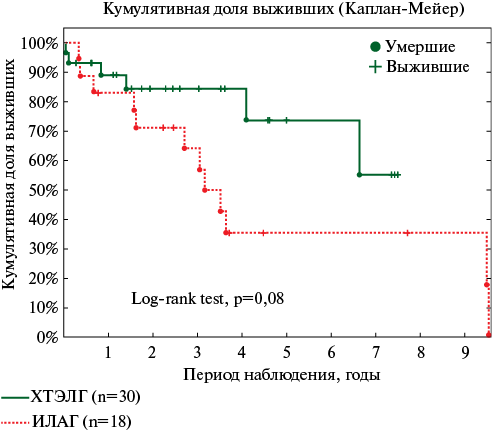
Рис. 1 Кривая Каплана-Майера кумулятивной выживаемости пациентов с ИЛАГ и ХТЭЛГ.
Примечание: ИЛАГ — идиопатическая легочная артериальная гипертензия, ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.
Обсуждение
Оценка прогноза заболевания имеет важное значение в клинической практике для выбора адекватной тактики лечения. КПНТ признан объективным методом оценки резервных возможностей сердечно-сосудистой и легочной систем, степень снижения которых определяет тяжесть и прогноз больных с ЛГ. Согласно клиническим рекомендациям, критериями неблагоприятного прогноза у больных с прекапиллярной ЛГ по результатам КПНТ являются VO2peak <11 мл/мин/кг и VE/VCO2 >44 [1][9]. По мнению большинства исследователей, VE/VCO2 — более объективный показатель неблагоприятного прогноза, т.к. его величина не зависит от мотивации пациента в отличие от VO2peak, а определяется метаболическим профилем и резервными возможностями сердечно-сосудистой и дыхательной систем. Ранее нами установлена прямая связь между показателями КПНТ и степенью тяжести ЛГ [6]. Отмечено, что VE/VCO2 увеличивается, а VO2peak, VO2 на АП, VO2/ЧСС и PETCO2peak (парциальное давление углекислого газа в конце выдоха) ΔVO2/ΔW снижаются по мере прогрессирования ЛГ. Особенностью настоящего исследования стало включение пациентов с ИЛАГ и ХТЭЛГ с вентиляторным эквивалентом по диоксиду углерода >44 в попытке выявить сходство и различие двух нозологических форм прекапиллярной ЛГ. Установлено, что в обеих группах величина VE/VCO2 была ассоциирована с такими прогностическими маркерами, как величина сердечного индекса, соотношение базальных размеров ПЖ и ЛЖ, а также амплитуда движения кольца трикуспидального клапана. Таким образом, подтверждена связь между VE/VCO2 и функциональным состоянием сердечно-сосудистой системы как у пациентов с ИЛАГ, так и ХТЭЛГ.
Сравнительный анализ результатов ЭхоКГ и КПКС у больных ИЛАГ и ХТЭЛГ показал, что пациенты с ИЛАГ имели более высокий уровень ЛСС и нумеристически более высокий уровень среднего ДЛА. В совокупности с компримированным ЛЖ это свидетельствует о большей степени поражения артериального русла МКК и, соответственно, ремоделирования правых камер сердца по сравнению с пациентами с ХТЭЛГ. У пациентов с ХТЭЛГ значения ДЗЛА и индекс объема левого предсердия были выше, что, вероятно, можно объяснить возрастными особенностями группы и наличием сопутствующей артериальной гипертензии. Более высокие значения центрального венозного давления у пациентов с ХТЭЛГ обусловлены быстрым развитием дисфункции ПЖ как на фоне формирования микроваскулопатии, так и вследствие раннего возврата отраженной волны за счет хронической обструкции проксимальных отделов ветвей ЛА [11].
Хорошо известно, что ФН вызывает активацию резервных возможностей сердечно-сосудистой и дыхательной систем, а также позволяет выявить нарушение транспорта и метаболизма кислорода [12-14]. В физиологических условиях увеличение доставки кислорода происходит за счет прироста сердечного выброса, минутной вентиляции, венозного возврата, уровня систолического АД, легочного кровотока, а также перераспределения кровотока к работающим мышцам, снижения ЛСС и уровня диастолического АД. Снижение доставки кислорода обусловлено неадекватным приростом сердечного выброса, нарушением вентиляторно-перфузионных отношений и диффузионной способности легких.
Результаты КПНТ у обследованных пациентов показали сопоставимое между группами уменьшение доставки кислорода, что характеризуется снижением VO2peak, VO2 на АП, ΔVO2/ΔW. Неадекватная доставка кислорода при возрастающей ФН со стороны сердечно-сосудистой системы характеризовалась нефизиологическим приростом сердечного выброса, а именно, низким приростом VO2/ЧСС, который является индексом ударного объема. Основными причинами неадекватного прироста сердечного выброса у больных ЛГ является уменьшение преднагрузки ЛЖ вследствие дилатации и снижения сократительной способности ПЖ и парадоксального движения межжелудочковой перегородки, что обуславливает уменьшение объема ЛЖ. Данный механизм снижения сердечного выброса в настоящем исследовании подтверждается корреляционной связью между VO2/ЧСС и конечным диастолическим размером ЛЖ. Одним из механизмов компенсации сниженной вследствие сердечной дисфункции доставки кислорода является увеличение минутной вентиляции, а маркером неэффективности минутной вентиляции служит повышение VE/VCO2. У пациентов обеих групп VE/VCO2 был значимо повышен по сравнению с должными значениями, что отражает низкую эффективность минутой вентиляции, которая обусловлена как неадекватным приростом сердечного выброса, так и ухудшением вентиляторно-перфузионных отношений и диффузии в легких у больных прекапиллярной ЛГ.
В норме оптимальная доставка кислорода в легких при ФН происходит за счет дилатации и рекрутирования функционирующих капилляров, что сопровождается снижением ЛСС и увеличением емкости микроциркуляторного русла [13]. Ремоделирование сосудов МКК, приводящее к развитию ЛГ, нарушает перфузию вентилируемых альвеол и вентиляторно-перфузионные отношения. Об этом свидетельствует увеличение вентиляции мертвого пространства. Одним из факторов повышения VE/VCO2 может служить снижение диффузионной способности легких, которое зарегистрировано у всех обследованных нами пациентов с ИЛАГ и ХТЭЛГ. Дополнительным стимулом увеличения минутной вентиляции может быть гипоксемия, которая развивается вследствие ухудшения диффузии через альвеолярно-капиллярную мембрану за счет отсутствия адекватного прироста диффузионной поверхности и повышения вязкости крови в сосудах МКК на фоне ФН [15].
В настоящем исследовании у больных ИЛАГ SpO2 на пике ФН была достоверно ниже, а степень десатурации значимо выше по сравнению с пациентами с ХТЭЛГ. Кроме того, только у пациентов с ИЛАГ было выявлено отсутствие снижения вентиляции мертвого пространства при возрастающей ФН. Подобный паттерн дыхания свидетельствует о более выраженных нарушениях вентиляторно-перфузионных отношений у больных ИЛАГ по сравнению с пациентами с ХТЭЛГ. Установлено, что соотношение VD/VT на пике ФН ассоциировано с высокими цифрами центрального венозного давления и сниженной SpO2 по данным пульсоксиметрии. С учетом более выраженной структурно-функциональной перестройки сердца и тяжести поражения артериального русла МКК у больных ИЛАГ можно предположить, что компенсаторные возможности сердца и легких уже задействованы в покое и, соответственно, ограничены в условиях ФН, определяя выраженность нарушений газообмена.
Возможно, ключевое значение, определяющее особенности декомпенсации у больных ИЛАГ и ХТЭЛГ с неблагоприятным прогнозом, имеют различия в количестве, скорости и морфологии ремоделирования ЛА. У пациентов с ИЛАГ при патоморфологических исследованиях выявляют генерализованное поражение мелких ЛА, что и обуславливает высокое ЛСС и значимое ухудшение вентиляторно-перфузионных отношений. А быстрое прогрессирование легочной васкулярной болезни у пациентов с ИЛАГ приводит к тяжелому дезадаптивному ремоделированию ПЖ. В патогенезе ХТЭЛГ первичную роль играет механическая обструкция вследствие нарушения лизиса тромботических масс в ЛА крупного и среднего калибра и в меньшей степени ремоделирование более мелких артерий, которое выражено в различной степени и развивается отсроченно [4].
Ограничения исследования. Небольшой объем выборки и включение пациентов с ИЛАГ и ХТЭЛГ с критериями исходно высокого риска по данным КПНТ не позволил оценить прогностическую ценность различных параметров КПНТ в зависимости от варианта ЛГ.
Заключение
Достоверная корреляционная взаимосвязь VE/VCO2 с гемодинамическими параметрами высокого риска, структурно-функциональными показателями ПЖ у пациентов с ИЛАГ и ХТЭЛГ подтверждает возможность использования КПНТ для определения степени тяжести и оценки прогноза различных вариантов ЛГ.
Использование КПНТ при динамическом наблюдении пациентов с ИЛАГ и ХТЭЛГ для оценки эффективности лечения и стратификации риска летальности может быть ценным неинвазивным методом, который нуждается в дальнейшем исследовании в сопоставлении с показателями КПКС и другими установленными детерминантами прогноза.
Более тяжелые нарушения газообмена в легких, регистрируемые при КПНТ у пациентов с ИЛАГ по сравнению с больными ХТЭЛГ, свидетельствуют о различиях в патогенезе двух заболеваний.
Несмотря на неблагоприятный по данным КПНТ прогноз больных ХТЭЛГ, хирургическое и эндоваскулярное лечение положительно влияло на выживаемость пациентов.
Отношения и деятельность. Исследование выполнено при поддержке гранта РНФ, соглашение № 23-15-00-318.
Список литературы
1. Humbert M, Kovacs G, Hoeper MM, Badagliacca R, et al. ESC/ERS Scientific Document Group. 2022 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. Eur Respir J. 2023;61:2200879. doi:10.1183/13993003.00879-2022.
2. Легочная гипертензия. Под редакцией С. Н. Авдеева. Москва. ГЭОТАР-Медиа. 2019. 608 с. ISBN: 9785970450000.
3. Humbert M, Guignabert C, Bonnet S, et al. Pathology and pathobiology of pulmonary hypertension: state of the art and research perspectives. Eur Respir J. 2019;53:1801887. doi:10.1183/13993003.01887-2018.
4. Simonneau G, Dorfmüller P, Guignabert C, et al. Chronic thromboembolic pulmonary hypertension: the magic of pathophysiology. Ann Cardiothorac Surg. 2022;11:106-19. doi:10.21037/acs-2021-pte-10.
5. Galiè N, Channick RN, Frantz RP, et al. Risk stratification and medical therapy of pulmonary arterial hypertension. Eur Respir J. 2019;53:1801889. doi:10.1183/13993003.01889-2018.
6. Казымлы А. В., Березина А. В., Рыжков А. В. др. Кардиопульмональное тестирование как метод оценки тяжести состояния больных с прекапиллярной легочной гипертензией. Кардиология. 2014;54(12):22-8. doi:10.18565/cardio.2014.12.22-28.
7. Симакова М. А., Злобина И. С., Березина А. В. и др. Место кардиопульмонального нагрузочного тестирования в оценке эффективности лечения пациентов с хронической тромбоэмболической легочной гипертензией. Кардиология. 2022;62:44-54. doi:10.18087/cardio.2022.4.n1611.
8. Forbes LM, Bull TM, Lahm T, et al. Exercise Testing in the Risk Assessment of Pulmonary Hypertension. Chest. 2023;164:736-46. doi:10.1016/j.chest.2023.04.013.
9. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. The Joint Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS). Eur Respir J. 2015;46:903-75. doi:10.1183/13993003.51032-2015.
10. Lang RM, Badano LP, Mor-Avi V, et al. Recommendations for Cardiac Chamber Quantification by Echocardiography in Adults: An Update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. European Heart Journal — Cardiovascular Imaging. 2015;16:233-71. doi:10.1093/ehjci/jev014.
11. Fukumitsu M, Westerhof BE, Ruigrok D, et al. Early return of reflected waves increases right ventricular wall stress in chronic thromboembolic pulmonary hypertension. Am J Physiol Heart Circ Physiol. 2020;319:H1438-50. doi:10.1152/ajpheart.00442. 2020.
12. Березина А. В., Козленок А. В. Кардиопульмональное тестирование в кардиологии. Трансляционная медицина. 2014;2:13-7. doi:10.18705/2311-4495-2014-0-2-105-116.
13. Pezzuto B, Agostoni P. The Current Role of Cardiopulmonary Exercise Test in the Diagnosis and Management of Pulmonary Hypertension. J Clin Med. 2023;12:5465. doi:10.3390/jcm12175465.
14. Кобелев Е., Берген Т. А., Таркова А. Р. и др. COVID-19 как причина хронической легочной гипертензии: патофизиологическое обоснование и возможности инструментальной диагностики. Кардиоваскулярная терапия и профилактика. 2021;20(5):2844. doi:10.15829/1728-8800-2021-2844.
15. Balady J, Arena R, Sietsema K, et al. American Heart Association Exercise, Cardiac Rehabilitation, and Prevention Committee of the Council on Clinical Cardiology. Council on Epidemiology and Prevention. Council on Peripheral Vascular Disease. Interdisciplinary Council on Quality of Care and Outcomes Research. Clinician’s Guide to cardiopulmonary exercise testing in adults: a scientific statement from the American Heart Association. Circulation. 2010;122:191-225. doi:10.1161/CIR.0b013e3181e52e69.
Об авторах
А. В. БерезинаРоссия
Аэлита Валерьевна Березина — г.н.с., руководитель НИЛ кардиопульмонального тестирования.
Санкт-Петербург
И. С. Злобина
Россия
Ирина Сергеевна Злобина — врач-кардиолог.
Санкт-Петербург
Н. С. Гончарова
Россия
Наталья Сергеевна Гончарова — к.м.н., с.н.с. НИО некоронарогенных заболеваний сердца.
Санкт-Петербург
М. А. Симакова
Россия
Мария Александровна Симакова — к.м.н., с.н.с. НИО некоронарогенных заболеваний сердца.
Санкт-Петербург
К. Б. Лапшин
Россия
Кирилл Борисович Лапшин — зав. отделением анестезиологии-реанимации с палатами реанимации и интенсивной терапии.
Санкт-Петербург
О. М. Моисеева
Россия
Ольга Михайловна Моисеева — д.м.н., профессор, г.н.с., руководитель НИО некоронарогенных заболеваний сердца.
Санкт-Петербург
Дополнительные файлы
Что известно о предмете исследования?
- Кардиопульмональное нагрузочное тестирование (КПНТ) — неинвазивный метод, позволяющий оценить функциональный статус и резервные возможности сердечно-сосудистой, дыха- тельной и мышечной систем у пациентов с легочной гипертензией (ЛГ).
Что добавляют результаты исследования?
- Благодаря прогностической способности ключевых переменных, КПНТ расширяет возможности для неинвазивной стратификации риска пациентов с различными вариантами ЛГ.
- Несмотря на неблагоприятный по данным КПНТ прогноз больных хронической тромбоэмболической ЛГ, применение хирургических и эндоваскулярных методов лечения оказывает положительное влияние на выживаемость пациентов.
Рецензия
Для цитирования:
Березина А.В., Злобина И.С., Гончарова Н.С., Симакова М.А., Лапшин К.Б., Моисеева О.М. Кардиопульмональное нагрузочное тестирование у пациентов с прекапиллярной легочной гипертензией, имеющих неблагоприятный прогноз. Кардиоваскулярная терапия и профилактика. 2024;23(9):4088. https://doi.org/10.15829/1728-8800-2024-4088. EDN: QLXMDS
For citation:
Berezina A.V., Zlobina I.S., Goncharova N.S., Simakova M.A., Lapshin K.B., Moiseeva O.M. Cardiopulmonary exercise testing in patients with precapillary pulmonary hypertension with an unfavorable prognosis. Cardiovascular Therapy and Prevention. 2024;23(9):4088. (In Russ.) https://doi.org/10.15829/1728-8800-2024-4088. EDN: QLXMDS
JATS XML

























































