Перейти к:
Новые тренды развития направления по неинвазивному исследованию микроциркуляции в коже человека. Описательный обзор
https://doi.org/10.15829/1728-8800-2025-4412
EDN: XFFGNI
Аннотация
Целью описательного обзора является анализ современного состояния и дальнейшего развития нового направления функциональной диагностики — неинвазивного исследования микроциркуляции в коже человека. В обзоре рассмотрены наиболее часто применяемые в исследовательской работе неинвазивные методы исследования микроциркуляции в коже человека. Проведена оценка диагностического потенциала различных приборов с учетом физических принципов их функционирования и особенностей ангиоархитектоники микрососудистого русла кожи. Рассмотрены основные направления совершенствования методов компьютерной видеокапилляроскопии, лазерной допплеровской флоуметрии и фотоплетизмографии, которые основаны на достижениях компьютерных технологий и микроэлектроники. Показано, что основными трендами развития направления являются миниатюризация приборов, дистанционная передача данных и применение современных методов автоматического анализа данных. Совершенно новым методом получения физиологической информации является анализ видеоплетизмограммы с помощью обычной веб-камеры. В основе метода лежит анализ изменения контрастности пикселей при видеозаписи поверхности кожи, где залегают переходные отделы капилляров, динамические изменения кровотока в которых приводят к изменению контрастности пикселей, регистрируемых стандартной веб-камерой.
Ключевые слова
Для цитирования:
Федорович А.А., Королев А.И., Ососков В.С., Саматова К.С., Драпкина О.М. Новые тренды развития направления по неинвазивному исследованию микроциркуляции в коже человека. Описательный обзор. Кардиоваскулярная терапия и профилактика. 2025;24(6):4412. https://doi.org/10.15829/1728-8800-2025-4412. EDN: XFFGNI
For citation:
Fedorovich A.A., Korolev A.I., Ososkov V.S., Samatova K.S., Drapkina O.M. New trends in non-invasive study of human skin microcirculation. A descriptive review. Cardiovascular Therapy and Prevention. 2025;24(6):4412. (In Russ.) https://doi.org/10.15829/1728-8800-2025-4412. EDN: XFFGNI
Введение
Система микроциркуляции (МЦ) представляет собой сложную сосудистую систему, которая регулирует баланс между потребностью клеток в питательных веществах и выведением продуктов тканевого обмена. Кроме того, микроциркуляторное русло (МЦР) играет важную роль в регуляции системной гемодинамики, определяя уровень артериального давления (АД) и венозный возврат крови к сердцу. В настоящее время все бóльший интерес специалистов различных областей медицины привлекает МЦР, которое первым вовлекается в различные патологические процессы и во многих случаях является основной "мишенью" для самых разных групп фармакологических препаратов.
Существует большое количество методов, которые позволяют неинвазивно или малоинвазивно исследовать состояние МЦ у человека. Для оценки уровня тканевой перфузии внутренних, глубоко расположенных органов, обычно используют радиоизотопную сцинтиграфию, однофотонную эмиссионную томографию, позитронную эмиссионную томографию. Однако оборудованием для выполнения таких исследований обладают далеко не все лечебные учреждения, поэтому более широкое распространение в научно-клинической практике получили биомикроскопия глазного дна и конъюнктивы, транскутанное определение напряжения газов, термография, полярография, веноокклюзионная плетизмография и др.
По мере технического прогресса неинвазивные методы исследования МЦ у человека постоянно совершенствуются. Благодаря бурному развитию микроэлектроники, компьютерных технологий и программного обеспечения к ним, в последние 2-3 десятилетия появился целый ряд перспективных методов исследования (компьютерная видеокапилляроскопия (ВКС), лазерная допплеровская флоуметрия (ЛДФ), лазерная спекл-визуализация, высокочастотная ультразвуковая допплерография, фотоплетизмография (ФПГ), инфракрасная спектроскопия и др.), которые позволяют неинвазивно оценивать как структурные, так и функциональные аспекты микроциркуляторного кровотока у человека.
Описательный обзор преследует две цели. Первая — акцентировать внимание исследователей на многоуровневом строении МЦР кожи, что требует применения различных инструментальных методов для оценки функционального состояния всех звеньев МЦР. Вторая цель — продемонстрировать основные тренды развития данного направления функциональной диагностики, основанные на современных достижениях компьютерных технологий, что позволяет оценивать функциональное состояние системы МЦ у человека не только в условиях специализированных лабораторий, но и открывает перспективные возможности удаленного мониторинга в режиме 24/7.
Материал и методы
Поиск публикаций, вошедших в описательный обзор, проводился на электронных ресурсах PubMed, MEDLINE, Scopus, Web of Science, e-library, cyberleninka. Период поиска был задан с 2005 по 2025гг; использовали следующие ключевые слова: микроциркуляция (microcirculation), видеокапилляроскопия (videocapillaroscopy), лазерная допплеровская флоуметрия (laser Doppler flowmetry), фотоплетизмография на пропускание (transmission photoplethysmography), портативный анализатор (portable analyzer, handheld), дистанционная передача данных (remote data transmission), автоматизированный анализ (automated analysis), нейронные сети (neural networks), искусственный интеллект (artificial intelligence), веб-камера (webcam), смартфон (smartphone).
Основной фокус в обзоре литературы сделан на портативных вариантах анализаторов с дистанционной передачей физиологических данных и автоматическом анализе получаемой информации, основанном на глубоком машинном обучении (МО) с применением элементов искусственного интеллекта (ИИ).
Результаты
Объект исследования — микрососудистое русло кожи
Доступными для неинвазивного исследования МЦ крови у человека являются глаза (бульбарная конъюнктива и глазное дно), слизистая ротовой полости и кожа. Самым удобным и доступным для исследования микроциркуляторного кровотока у человека является микрососудистое русло кожи (МЦР). Основным преимуществом кожи является то, что в ней представлены практически все механизмы регуляции микроциркуляторных процессов (местные, нейрогенные симпатические и ноцицептивные, гуморальные и др.) и отражены не только местные, но и большинство системных физиологических процессов в норме и при патологии. Еще одним неоспоримым достоинством кожи является возможность выполнения широкого спектра различных функциональных тестов [1].
Кожа является крупным (1,5-2 м²) и одним из наиболее васкуляризированных органов с суммарной площадью обменной поверхности >40 м². Как орган, кожа выполняет ряд важнейших функций — защитно-покровную, выделительную, иммунобиологическую, эндокринную, витамин-синтезирующую, терморегуляторную и другие. Одной из ведущих физиологических функций является поддержание температурного гомеостаза целостного организма, что и обуславливает особенности ее строения (рисунок 1 А) [2]. МЦР кожи состоит из двух сосудистых сплетений — глубокого (располагается на границе кожи и подкожной клетчатки) и поверхностного (в папиллярной дерме), которое формирует капиллярное русло у самой поверхности кожи. Глубокое сплетение формируется (рисунок 1 Б-2) из сосудов подлежащих межфасциальных пространств и подкожной жировой клетчатки, боковыми ветвями питает луковицы волосяных фолликулов и потовые железы, а восходящими сосудами формирует поверхностное сосудистое сплетение (рисунок 1 Б-1). Двухслойное строение МЦР увеличивает площадь теплообменной поверхности, что облегчает функционирование основных терморегуляторных механизмов путем теплопроведения, излучения, конвекции и испарения.
В настоящее время универсального метода, который позволяет одновременно оценивать структурно-функциональные параметры микроциркуляторного кровотока на уровне всех звеньев МЦР кожи, не существует, что связано со структурными особенностями строения МЦР кожи и физическими принципами современных неинвазивных методов исследования, которые основаны на принципах биофотоники. Из всего спектра современных методов исследования можно выделить три основных, которые чаще всего применяются в научно-клинической практике (рисунки 1 Г и 1 Д) — компьютерная ВКС, ЛДФ и ФПГ.
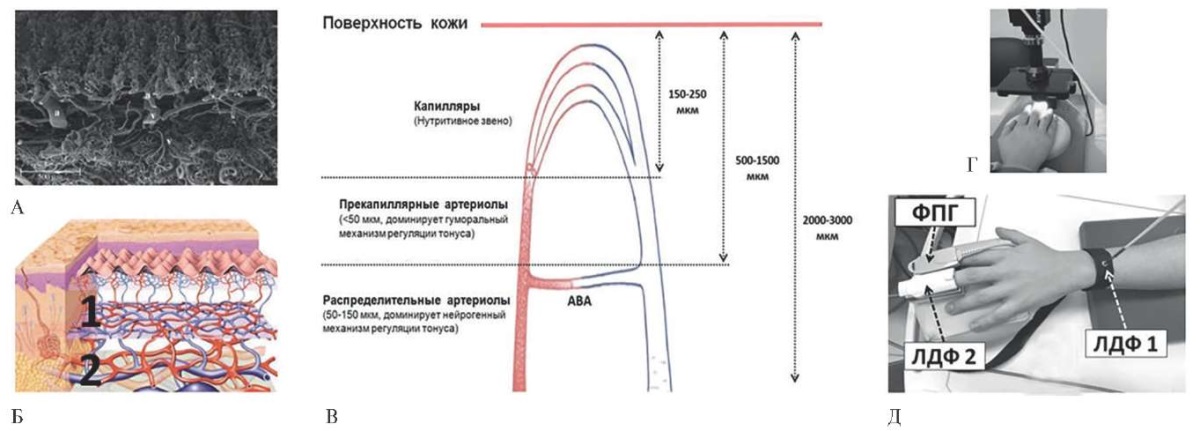
Рис. 1 Объект исследования — МЦР кожи: А — электронная микроскопия микрососудистого русла кожи [2]; Б — схема строения МЦР кожи (1 — поверхностное сосудистое сплетение; 2 — глубокое сосудистое сплетение); В — схема строения МЦР с учетом глубины залегания микрососудов относительно поверхности кожи; Г — компьютерная ВКС; Д — одномоментное исследование микрососудов поверхностного и глубокого сосудистых сплетений. ЛДФ 1 и 2 — поверхностное сосудистое сплетение. ФПГ — глубокое сосудистое сплетение (объяснение в тексте).
Примечание: ВКС — видеокапилляроскопия, ЛДФ — лазерная допплеровская флоуметрия, МЦР — микроциркуляторное русло, ФПГ — фотоплетизмография. Цветное изображение доступно в электронной версии журнала.
Компьютерная видеокапилляроскопия
Компьютерная видеокапилляроскопия — неинвазивный метод исследования структурно-функционального состояния капиллярного русла кожи, основанный на высокоскоростной видеосъёмке капилляров сосочкового слоя дермы в отраженном свете.
Особенностью МЦР кожи является то, что капилляры по отношению к поверхности кожи располагаются перпендикулярно — артериальный отдел восходит из глубины дермы, делая непосредственно у поверхности кожи изгиб (переходный отдел капилляра) с последующим переходом в глубину дермы венозным отделом капилляра (рисунок 1 В). По своей сути, капилляры кожи представляют собой противоположный сердцу "полюс" большого круга кровообращения, на уровне которых происходят основные обменные процессы между кровью и тканями [1].
Единственным участком кожи, доступным для исследования капилляров на всем их протяжении (артериальный, переходный и венозный отделы), является ногтевое ложе, где в области корня ногтя кожа истончается и вытягивается, что приводит к горизонтальному расположению капилляров относительно поверхности кожи (рисунок 1 Г). Только в этой области кожного покрова можно визуализировать капилляры на всем их протяжении, оценить их преимущественную форму, размеры, распределение, характер кровотока и ряд других параметров. Достаточно на 5 мм сместить объектив капилляроскопа от ногтевого ложа ближе к межфаланговому суставу пальца и капилляры принимают перпендикулярное к поверхности кожи положение, что позволяет визуализировать только переходные отделы обменных микрососудов.
Внедрение компьютерных технологий и высокоскоростных цифровых видеокамер существенно повысило информативность ВКС, позволяя получать такие объективные данные, как размер капилляров в различных отделах (артериальный, переходный, венозный), степень гидратации интерстициального пространства (размер перикапиллярной зоны), число капилляров на единицу площади, скорость капиллярного кровотока [3][4] Корректное измерение скорости капиллярного кровотока (СКК) является очень сложной задачей, что обусловлено несколькими факторами. Во-первых, СКК может существенно различаться в соседних капиллярах. Во-вторых, проблема корректного измерения СКК затруднена неконтролируемым смещением участка поверхности кожи при больших увеличениях и одновременным динамическим смещением потока эритроцитов в капиллярах, что приводит к появлению "оптических шумов", которые при автоматическом расчете СКК проявляется в виде высокоамплитудных выбросов [3].
Проблему измерения СКК, характерную для первых моделей компьютерных видеокапилляроскопов, смогли решить российские ученые из Санкт-Петербургского национального исследовательского университета информационных технологий, механики и оптики" (НИУ ИТМО), которые разработали компьютерную программу анализа, основанную на методе "опорного кадра" [5]. Данный алгоритм позволяет не только нивелировать проблемы высокоскоростной видеосъемки капиллярного кровотока при большом увеличении и получать корректные результаты гемодинамических параметров в самых маленьких сосудах организма, но и рассчитывать СКК одновременно в нескольких капиллярах ногтевого ложа, что раньше для исследователей было совершенно недоступно. Предложенный авторами метод компенсации смещений с помощью "опорного кадра" позволяет оценивать СКК не только в области ногтевого ложа, где капилляры располагаются параллельно поверхности кожи, но и в других участках кожного покрова, где капилляры расположены перпендикулярно относительно поверхности. Предложенный авторами подход к получению и анализу информации о гемодинамике капиллярного кровотока не только в области ногтевого ложа пальцев, но и в других участках кожного покрова, существенно расширяет возможности клинического применения метода ВКС при самом широком спектре заболеваний.
Другим трендом в развитии метода ВКС является миниатюризация приборов. Первые модели компьютерных капилляроскопов создавались путем совмещения стандартного микроскопа с цифровой видеокамерой (рисунок 2 А), что позволяет использовать их только в условиях специализированной лаборатории. Современные модели компьютеризированных капилляроскопов представляют собой очень компактные устройства (рисунки 2 Б-Д), которые можно использовать непосредственно у постели больного, а некоторые из них уже оснащены функцией дистанционной передачи зарегистрированных видеофрагментов по беспроводным (Bluetooth, Wi-Fi) каналам связи на смартфон, планшет или ноутбук.
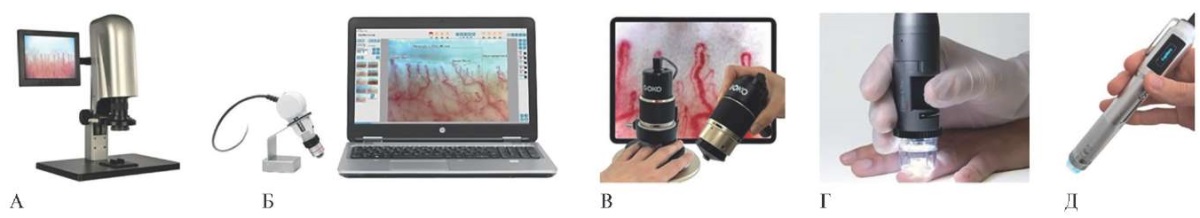
Рис. 2 Компьютерные капилляроскопы: А — стационарный вариант на базе стандартного микроскопа; Б — портативный капилляроскоп "Inspectis" (Швеция); В — портативный капилляроскоп "GOKO" (Япония); Г — портативный капилляроскоп "Dino-Lite" (Нидерланды); Д — портативный капилляроскоп "Smart G-Scope" (Южная Корея).
Внедрение в анализ видеоизображений алгоритмов компьютерного зрения и глубокого МО, основанного на сверточных нейронных сетях, позволяет не просто автоматизировать и ускорить анализ капиллярного русла кожи, но измерять совершенно новые параметры, которые раньше не поддавались количественной оценке — капиллярный гематокрит, неоднородность скорости капиллярного кровотока. Комплексная компьютерная система "CapillaryNet" может обнаруживать капилляры со скоростью 0,9 сек на кадр с точностью 93% [6].
ЛДФ
ЛДФ представляет собой оптический неинвазивный метод регистрации параметров МЦ крови, который основан на зондировании биологических тканей низкоинтенсивным когерентным лазерным излучением и анализе рассеянной от форменных элементов крови (эритроцитов) его составляющей. При лазерном зондировании кожи в диапазоне длин волн от 630 до 1064 нм, глубина проникновения излучения составляет 1-2 мм и регистрируемый доплеровский сдвиг частоты дают эритроциты, которые в различных сосудах поверхностного сплетения движутся с различными скоростями (артериолы — 700-3900 мкм/сек, капилляры — 100-900 мкм/сек, венулы — 300-1200 мкм/сек). Амплитуда отраженного сигнала формируется в результате отражения излучения от ансамбля эритроцитов, движущихся с разными скоростями и по-разному количественно распределенных в артериолах, капиллярах и венулах, поэтому в методе ЛДФ применяется алгоритм усреднения, который позволяет получить средний допплеровский сдвиг частоты по всей совокупности эритроцитов, попадающих в зондируемую область. В результате флоуметрии мы получаем данные об объемном кровотоке в 3-5 мм³ кожи, который носит колебательный характер, что обусловлено одновременным действием нескольких регуляторных механизмов [7]. При этом вклад кровотока непосредственно по капиллярам в общую спектральную мощность отраженного сигнала не превышает 20%, поэтому основную информацию при ЛДФ мы получаем от прекапиллярных (артериолы) и посткапиллярных (венулы) микрососудов, входящих в поверхностное сосудистое сплетение. Необходимо подчеркнуть, что из всех микрососудов в области зондирования только прекапиллярные артериолы содержат гладкомышечные клетки.
Фундаментальной особенностью прекапиллярных артериол является их высокая вазомоторная активность. Прекапиллярные артериолы находятся в постоянном движении, изменяя тонус и величину своего просвета, что проявляется в виде вазомоций, которые являются необходимым физиологическим механизмом, направленным на модуляцию поступающего в МЦР объема артериальной крови до оптимальных для транскапиллярного обмена значений. Применение математических аппаратов анализа колебаний микрокровотока позволяет проводить оценку функциональной активности каждого регуляторного механизма изолированно от других, для чего исходные ЛДФ-граммы подвергаются спектральному анализу с использованием Вейвлет-преобразования и, намного реже, Фурье-преобразованию. В настоящее время выделяют до 8 изолированных частотных диапазона [8], но в научной литературе чаще всего используют 5 основных — эндотелиальный, нейрогенный, миогенный, респираторно обусловленный (венулярный) и кардиальный (пульсовой).
Область исследования при ЛДФ выбирается исследователем самостоятельно в зависимости от поставленных задач. При выборе места необходимо учитывать регионарные особенности ангиоархитектоники МЦР кожи, которые могут существенно различаться. Например, наличие артериоло-венулярных анастомозов (АВА), основной функцией которых является участие в процессах терморегуляции, а величина их просвета регулируется исключительно симпатической адренергической нервной системой.
В коже предплечья АВА мало и залегают они в более глубоких слоях кожи, недоступных для лазерного зондирования. В ладонной поверхности пальцев АВА много и залегают они поверхностно. Поэтому перфузия кожи в области предплечья больше отражает нутритивный (обменный) характер микрокровотока (рисунок 1 Д — ЛДФ 1), а в подушечках пальцев (рисунок 1 Д — ЛДФ 2) терморегуляторную (шунтовую) направленность кожной перфузии. Ориентировочные параметры ЛДФ в различных областях кожного покрова приведены в методическом пособии Козлова В. И. и др. [9].
Современные модели лазерных допплеровских флоуметров основных мировых производителей (Transonic (США), MOOR (Великобритания), Perimed (Швеция), ЛАЗМА (Россия)) для доставки лазерного излучения к тканям и приема отраженного сигнала используют оптоволоконный зонд (рисунок 1 Д — ЛДФ 1, ЛДФ 2, рисунок 3 А). Недостатком применения оптоволоконной техники является высокая чувствительность зонда к любым движениям и внешним воздействиям, что вынуждает проводить исследования МЦ в специализированных лабораториях. В 2018г российским производителем лазерных анализаторов МЦ крови (НПП "ЛАЗМА", Москва, Россия) разработан и внедрен в научно-клиническую практику портативный вариант лазерного анализатора (ЛАЗМА-ПФ) без оптического волокна, который сегодня в мире аналогов не имеет. Анализатор выполнен в форм-факторе наручных часов (д×ш×в — 55×45×20 мм, масса — 40 г) и имеет встроенный термодатчик, который позволяет измерять температуру кожи в области исследования с точностью до 0,1 °С (рисунок 3 Б). Получаемая информация физиологического характера в цифровом формате передается по беспроводным каналам (Bluetooth или Wi-Fi) непосредственно на компьютер, что определяет мобильность лазерного анализатора и существенно расширяет возможности его применения. Портативность и беспроводная передача данных дают возможность одновременно использовать до 6-10 датчиков в различных участках тела во время выполнения различных функциональных тестов [10-13], в специализированном стационаре в условиях "красной зоны" во время пандемии COVID-19 (COrona VIrus Disease 2019) [14] и в настоящее время используется на борту Международной космической станции (МКС) в условиях невесомости [15].

Рис. 3 ЛДФ: А — стационарный вариант двухканального лазерного анализатора микроциркуляции крови (ЛАКК-02) с оптоволоконными зондами доставки лазерного излучения к тканям и приема отраженного сигнала; Б — портативный вариант лазерного анализатора микроциркуляции крови "ЛАЗМА-ПФ"; В — портативные варианты лазерных анализаторов микроциркуляции крови "ЛАЗМА-ПФ": 1) одноканальный "ЛАЗМА-ПФ" — ЛДФ; 2) двухканальный вариант "ЛАЗМА-ПФ" — ЛДФ + ФС.
Примечание: ЛДФ — лазерная допплеровская флоуметрия, ФС — флуоресцентная спектроскопия.
Еще более перспективным является разработанный НПП "ЛАЗМА" двухканальный вариант портативного лазерного анализатора. Первый канал представлен стандартным лазерным анализатором для оценки параметров микроциркуляторного кровотока (ЛДФ). Второй канал предназначен для флуоресцентной спектроскопии (ФС), которая позволяет оценивать соотношение коферментов никотинамид-аденин-динуклеотид восстановленный (NADH) и флавин-аденин-динуклеотид (FAD) по интенсивности возбуждаемой флуоресценции, что, в конечном итоге, позволяет оценивать непосредственно тканевой (окислительный) метаболизм. Таким образом, двухканальный вариант портативного лазерного анализатора "ЛАЗМА-ПФ" позволяет одновременно в одном объеме биоткани оценивать и параметры тканевой перфузии, и показатели кислородного обмена. Двухканальная версия "ЛАЗМА-ПФ" по длине и ширине сопоставима с одноканальным вариантом, но на 6 мм толще (д×ш×в — 55×45×26 мм) и на 10 грамм тяжелее (рисунок 3 В2). При таких массогабаритных показателях удельное давление прибора на кожу составляет 0,016 г/мм² и 0,02 г/мм² для одноканальной и двухканальной модификаций, соответственно, что не оказывает какого-либо влияния по показатели МЦ.
ФПГ
Метод ФПГ имеют очень простую конструкцию, состоящую из светового излучателя и фотоприемника. В основе ФПГ лежит регистрация пульсовой волны объема крови. Принципиально важным является геометрическое расположение оптического излучателя и фотодетектора, что позволяет записывать сигнал двумя разными способами — пропусканием и отражением. В режиме пропускания оптический излучатель (LED) и фотодетектор (PD) размещены на двух противоположных сторонах ткани (рисунок 4 А), тогда как в режиме отражения оптический излучатель и фотодетектор размещаются на одной стороне ткани (рисунок 4 Б).

Рис. 4 ФПГ: А — ФПГ в режиме пропускания; Б — ФПГ в режиме отражения; В — двухканальный фотоплетизмограф на пропускание "AngioCode-322"; Г — одноканальный вариант портативного фотоплетизмографа на пропускание "AngioCode-301" с дистанционной передачей данных.
Примечание: ФПГ — фотоплетизмография.
При использовании режима отражения, глубина проникновения света и объем зондируемой биоткани зависят от длины волны излучения и расстояния между оптическим источником и фотодетектором. В современных конструкциях ФПГ на отражение применяются источники с различными длинами волн (от 530 до 940 нм), но даже самые большие длины волн (940 нм) имеют глубину проникновения излучения не >2,5-3 мм [16], что практически сопоставимо с глубиной зондирования при ЛДФ. Единственным преимуществом конструкций ФПГ на отражение является возможность применения их практически в любых участках кожного покрова.
Совершенно другую информацию можно получить, используя ФПГ на пропускание, когда источник света и фотодетектор расположены на противоположных сторонах ткани. Такая конструкция ФПГ позволяет применять его на ограниченных участках тела (пальцы конечностей, мочка уха), но дает возможность получать информацию с более глубоких слоев кожи.
В России наибольшее распространение получил двухканальный фотоплетизмограф "Ангиоскан-01" с пальцевыми датчиками, которые работают в режиме пропускания. В настоящее время данный вариант фотоплетизмографа выпускает ООО "АльмаКод" (Москва, Россия) под новым названием — "AngioCode-322" (рисунок 4 В). Источниками излучения в данных приборах являются светодиоды с двумя длинами волн в ближней инфракрасной области спектра (680 и 870 нм), что позволяет фотонам проходить через все толщу ногтевой фаланги пальца и захватывать более крупные артериолы из глубокого сосудистого сплетения кожи и терминальные отделы магистральных сосудов мышечного типа (пальцевые), в которых доминирует нейрогенный механизм регуляции вазомоторной активности. Контурный анализ пульсовой волны при ФПГ позволяет получать большой объем информации — частоту пульса, сатурацию крови, индекс жесткости, индекс отражения, индекс аугментации, возрастной индекс, возраст сосудистой системы и множество других расчетных параметров.
Преимущество применения модификации ФПГ на пропускание продемонстрировано в исследовании Королева А. И. и др. [17]. При комплексном исследовании МЦР тремя методами (ВКС, ЛДФ, ФПГ) у мужчин трудоспособного возраста с впервые выявленной артериальной гипертензией (АГ), было показано, что на ранних стадиях развития АГ изменения на уровне капиллярного русла (ВКС) и прекапиллярных артериол (ЛДФ) отсутствуют. Основные изменения (увеличение индекса аугментации, индекса жесткости и индекса отражения) выявлены на уровне распределительных артериол (глубокое сосудистое сплетение), в которых доминирует нейрогенный механизм регуляции тонуса резистивных микрососудов, что может косвенно свидетельствовать в пользу нейрогенной теории Ланга-Мясникова в генезе АГ.
В настоящее время российские производители представили одноканальный портативный вариант прибора ФПГ на пропускание — "AngioCode-301" (рисунок 4 Г), который по своим функциональным и диагностическим характеристикам не уступает стационарному двухканальному варианту — "AngioCode-322". Разработанное мобильное приложение для Android-устройств (смартфон, планшет) и наличие bluetooth-интерфейса обеспечивают передачу данных в облачное хранилище, доступ к которому возможен как через мобильное приложение, так и через веб-интерфейс. Данная модификация прибора позволяет проводить исследования функционального состояния резистивных микрососудов в домашних условиях в режиме удаленного мониторинга.
Благодаря развитию компьютерных технологий (нейронные сети, глубокое МО, ИИ), в последние годы очень активно стало развиваться новое направление применения метода ФПГ — безманжеточное определение уровня АД. Исследования в данной области ведутся в трех основных направлениях — математическое моделирование, МО и глубокое МО с использованием нейронных сетей и ИИ.
Математическое моделирование содержит формулы, позволяющие рассчитать АД по различным переменным, извлеченным из сигнала ФПГ, среди которых основными являются время прихода импульса и время прохождения импульса, что, в свою очередь, требует дополнительно регистрировать либо электрокардиограмму, либо использовать два датчика ФПГ, расположенных в разных частях тела.
Форма волны АД и сигнала ФПГ имеют много общего. Для более детального рассмотрения этой темы исследователи приняли во внимание набор характеристик ФПГ в сочетании с моделью МО. Модель МО делает расчет на основе входных значений различных признаков необработанного ФПГ-сигнала, которые задаются исследователем. Несмотря на положительные результаты, точность модели ФПГ (МО и выбор признаков) в значительной степени зависит от алгоритмов извлечения и набора признаков. Для решения этой проблемы также была применена модель глубокого обучения, которая показала существенное улучшение результатов. Сеть глубокого МО автоматически извлекает признаки непосредственно из необработанного сигнала ФПГ, используя сверточную или рекуррентную нейронную сеть. Эти сети можно рассматривать как адаптивный фильтр, они обучаются для достижения минимально возможной ошибки. Комбинированные (гибридные) нейронные сети позволяют получать погрешность измерения АД методом ФПГ на отражение на уровне 3,97 мм рт.ст. для систолического АД, и 2,3 мм рт.ст. для диастолического [18].
Видеоплетизмография (ВПГ)
Совершенно новым трендом в развитии методов диагностики кровотока на уровне МЦР кожи является применение обычных пользовательских веб-камер. В отличие от традиционных методов ФПГ, которые требуют непосредственного контакта датчиков с кожей, в данном случае объектив веб-камеры используется в качестве фотодатчика, а само исследование проводится бесконтактно. После того как в конце 1990-х гг камеры были оцифрованы, стало возможным применять вычислительные методы для идентификации объектов на изображениях, количественной оценки мельчайших изменений в движении и обнаружения вариаций отраженного света, невидимых человеческому глазу.
Диапазон длин волн света, видимого человеком, составляет 380-740 нм. В стандартных веб-камерах используется система цветопередачи RGB (Red, Green, Blue). Это адаптивная цветовая модель получения любых оттенков видимого человеческим глазом спектра, при которой смешиваются красный (625-740 нм), зеленый (500-565 нм) и синий (380-485 нм), позволяя получать >16 млн цветов (рисунок 5 А).
Физический принцип получения физиологической информации с помощью веб-камеры основан на принципах биофотоники; в зарубежной литературе этот метод исследования относят к ФПГ, хотя более правильным следует считать термин ВПГ. В основе метода лежит анализ изменения контрастности пикселей при видеозаписи поверхности кожи. Непосредственно у поверхности кожи (на глубине ~100-150 мкм) залегают переходные отделы капилляров (рисунок 1 В). Кровоток в переходных отделах капилляров кожи при ВПГ приводит к периодическому изменению яркости (контрастности) пикселей, которые регистрируются веб-камерой в цветовом диапазоне RGB (рисунок 5 Б). Каждый отдельный кадр (25-30 кадров/сек) последовательно проходит стадию цифровой обработки и преобразовывается в один единственный отсчёт видеоплетизмографического сигнала (рисунок 5 В). По своей сути, ВПГ можно условно отнести к методу динамической ВКС, который позволяет регистрировать динамику кровотока непосредственно в переходном отделе капилляров [19-21].
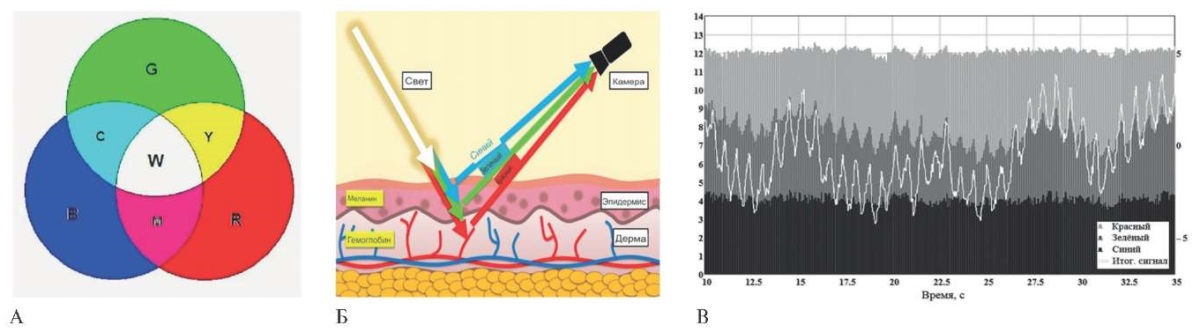
Рис. 5 ВПГ: А — адаптивная цветовая модель получения любых оттенков видимого человеческим глазом спектра; Б — регистрация веб-камерой видеосигнала в цветовом диапазоне RGB; В — цифровая обработка видеосигнала с преобразованием его в видеоплетизмограмму.
Примечание: ВПГ — видеоплетизмография, RGB — система цветопередачи в цифровых камерах. Цветное изображение доступно в электронной версии журнала.
Первые сообщения о возможности оценивать частоту сердечного ритма с помощью стандартной веб-камеры появились в конце 2000-х гг [22]. В 2012г Scully CG, et al. показали возможность извлечения из видеозаписей веб-камеры смартфона информации не только о частоте сердечных сокращений, но и частоте дыхательных движений и сатурации крови [23]. Авторы отмечают, что получаемые с помощью веб-камеры данные очень хорошо согласуются с данными общепризнанных инструментальных методов исследования этих показателей. В 2018г Yan BP, et al. привели результаты исследования частоты сердечного ритма с помощью 12-канальной электрокардиограммы и фронтальной веб-камеры смартфона с кожи лица и тыльной камерой смартфона с подушечки пальцев кисти контактным способом. Чувствительность и специфичность анализа сердечного ритма при ВПГ в коже лица составили 94,7 и 95,8%, а при пальцевой ВПГ — 94,7 и 93,0%, соответственно [24]. В дальнейшем, используя методы глубокого МО с элементами ИИ, авторы разработали алгоритм оценки и анализа сердечного ритма с помощью одной веб-камеры с расстояния в 1,5 м одновременно у 5 человек, выявляя наличие фибрилляции предсердий [25]. В январе 2021г Международное общество холтеровского мониторирования и неинвазивной электрокардиологии, Общество сердечного ритма, Европейская ассоциация сердечного ритма и Азиатско-тихоокеанское общество сердечного ритма опубликовали совместное заявление по текущему статусу технологий мобильного здравоохранения ("mHealth") в лечении аритмии. В заявлении подчеркивается, что использование любых мобильных устройств с камерами является простым и легко масштабируемым методом диагностики нарушений ритма сердца, что может изменить подход к скринингу фибрилляции предсердий [26].
Диагностические возможности ВПГ существенно шире, чем только определение параметров сердечного ритма. В 2019г коллективом ученых из Канады и Китая на 1328 нормотензивных добровольцах, с использованием метода глубокого МО с элементами ИИ, был разработан алгоритм, позволяющий прогнозировать уровень систолического АД с точностью 94,8% и диастолического АД с точностью 95,7% по 2-мин видеофрагментам кожи лица фронтальной камерой смартфона с расстояния 40-60 см. В качестве обучающей модели авторы использовали измерение АД в пальцевой артерии в режиме beat-to-beat [27]. В настоящее время авторы работают над расширением диапазона измеряемых величин АД. В другом исследовании авторского коллектива из Швейцарии приводятся результаты ВПГ контактным способом в коже пальца кисти тыльной камерой смартфона. Особенностью данной работы является то, что обучающим методом было прямое измерение АД в лучевой артерии. Обучающий массив состоял из 350 измерений с гипо-, гипер- и нормотензивным состоянием гемодинамики. Проверка разработанного алгоритма на 50 амбулаторных пациентах показала погрешность измерения для систолического АД в пределах ±8 мм рт.ст., для диастолического ±4 мм рт.ст. [28]. Сегодня исследования в данном направлении активно ведутся во многих странах мира.
Заключение
Практически все современные методы для неинвазивного исследования МЦ у человека основаны на методах биофотоники. В настоящее время универсального метода для оценки всех звеньев МЦ (капилляры, прекапиллярные артериолы, распределительные артериолы) не существует, что связано с особенностями ангиоархитектоники МЦР кожи и технических характеристик различных приборов. Каждый из методов дает информацию о функциональном состоянии какого-то определенного звена МЦР. Обменное звено и гемодинамику в капиллярах кожи можно оценить с помощью компьютерной ВКС и ВПГ. Получить информацию о микрососудах из поверхностного сосудистого сплетения (прекапиллярные артериолы) можно с помощью методов ЛДФ и ФПГ на отражение. Полноценную информацию о функциональном состоянии микрососудов глубокого сосудистого сплетения кожи можно получить методом ФПГ на пропускание.
Основным современным трендом развития неинвазивных методов исследования МЦР у человека является миниатюризация приборов и дистанционная передача физиологических данных по различным (Bluetooth или Wi-Fi) каналам связи, что существенно расширяет возможности специалистов и позволяет проводить динамический контроль функционального состояния различных звеньев МЦР кожи у человека в режиме удаленного мониторинга в формате 24/7. Еще одним современным трендом является разработка алгоритмов автоматического анализа получаемых данных с использованием методов глубокого МО и нейронных сетей. Такой подход позволяет решить сразу несколько задач — сокращение времени на анализ результатов, исключение элементов субъективизма со стороны исследователя, расширение функциональных возможностей приборов.
Весьма перспективными являются исследования по безманжеточному определению уровня АД с помощью ФПГ и ВПГ. Хотя контактные датчики ФПГ сегодня широко применяются в различных носимых устройствах (смарт-часы, фитнес-браслеты и др.), они далеко не универсальны. И если посмотреть статистику, то в 2021г мировое число пользователей смарт-часами составляло не >203 млн человек, в то время как число пользователей смартфонов приближалось к 6,4 млрд, причем в странах с более низким уровнем благосостояния неравенство было еще больше выражено. Отсюда можно сделать вывод, что развитие диагностического направления ВПГ является более предпочтительным, т.к. в конечном итоге позволит охватить большее число людей во всем мире.
Отношения и деятельность. Работа выполнена в рамках госзадания Минздрава России № 124013100904-7.
Список литературы
1. Федорович А. А. Микрососудистое русло кожи как объект исследования. Регионарное кровообращение и микроциркуляция 2017;16(4):11-26. doi:10.24884/1682-6655-2017-16-4-11-26.
2. Sangiorgi S, Manelli A, Congiu T, et al. Microvascularization of the human digit as studied by corrosion casting. J Anat. 2004; 204(2):123-31. doi:10.1111/j.1469-7580.2004.00251.x.
3. Федорович А. А. Капиллярная гемодинамика в эпонихии верхней конечности. Регионарное кровообращение и микроциркуляция. 2006;19(1):20-9. EDN: JWJRCP.
4. Гурфинкель Ю. И., Атьков О. Ю., Сасонко Р. М., Саримов Р. М. Новый подход к интегральной оценке состояния сердечно-сосудистой системы у пациентов с артериальной гипертензией. Российский кардиологический журнал. 2014;(1):101-6. doi:10.15829/1560-4071-2014-1-101-106.
5. Гуров И. П., Волков М. В., Маргарянц Н. Б., Потемкин А. В. Метод совмещения локально изменяющихся изображений в видеокапилляроскопии. Оптический журнал. 2019;86(12):35-42. doi:10.17586/1023-5086-2019-86-12-35-42.
6. Abdou MAH, Truong TT, Dykyy A, et al. CapillaryNET: An automated system to quantify skin capillary density and red blood cell velocity from handheld vital microscopy. Artif Intell Med. 2022; 127:102287. doi:10.1016/j.artmed.2022.102287.
7. Крупаткин А. И., Сидоров В. В. Функциональная диагностика состояния микроциркуляторнотканевых систем. Колебания. Информативность. Нелинейность. Руководство для врачей. Книжный дом ЛИБРОКОМ Москва. 2013. с. 496. ISBN: 978-5-397-03943-7.
8. Крупаткин А. И. Колебания кровотока — новый диагностический язык в исследовании микроциркуляции. Регионарное кровообращение и микроциркуляция. 2014;13(1):83-99. doi:10/24884/1682-6655-2014-13-1-83-99.
9. Козлов В. И., Азизов Г. А., Гурова О. А., Литвин Ф. Б. Лазерная допплеровская флоуметрия в оценке состояния и расстройств микроциркуляции. М.: Изд-во РУДН. 2012. с. 32.
10. Fedorovich AA, Loktionova YI, Zharkikh EV, et al. Body position affects capillary blood flow regulation measured with wearable blood flow sensors. Diagnostics. 2021;11:436. doi:10.3390/diagnostics11030436.
11. Фролов А. В., Локтионова Ю. И., Жарких Е. В. и др. Реакция микроциркуляции крови в коже различных участков тела при выполнении дыхательных упражнений йоги. Регионарное кровообращение и микроциркуляция. 2023;22(1):72-84. doi:10.24884/1682-6655-2023-22-1-72-84.
12. Пашкова Д. В., Попова Ю. А., Федорович А. А. Функциональное состояние микроциркуляторного русла кожи здоровых женщин в условиях "сухой" иммерсии. Авиакосмическая и экологическая медицина. 2023; 57(2):39-46. doi:10.21687/0233-528X-2023-57-2-39-46.
13. Пашкова Д. В., Попова Ю. А., Федорович А. А., Шпаков А. В. Регионарный кожный кровоток у здоровых обследуемых в условиях 21-суточной антиортостатической гипокинезии. Медицина экстремальных ситуаций. 2025;27(1):124-130. doi:10.47183/mes.2025-267.
14. Федорович А. А., Марков Д. С., Малишевский М. В. и др. Нарушения микроциркуляторного кровотока в коже предплечья в острую фазу COVID-19 по данным лазерной допплеровской флоуметрии. Регионарное кровообращение и микроциркуляция. 2022;21(3):56-63. doi:10.24884/1682-6655-2022-21-3-56-63.
15. Дунаев А. В., Локтионова Ю. И., Жарких Е. В. и др. Исследование микроциркуляции крови в условиях невесомости с помощью портативных лазерных допплеровских флоуметров. Авиакосмическая и экологическая медицина. 2024;58(1):47-54. doi:10.21687/0233-528X-2024-58-1-47-54.
16. Savo R, Pierrat R, Najar U, et al. Mean path length invariance in multiple light scattering. Science. 2017;358:765-8. doi:10.1126/science.aan4054.
17. Королев А. И., Федорович А. А., Горшков А. Ю. и др. Факторы фотоплетизмографии, ассоциированные с наличием невыявленной артериальной гипертонии у мужчин с низким и умеренным сердечно-сосудистым риском. Кардиоваскулярная терапия и профилактика. 2023;22(7):3649. doi:10.15829/1728-8800-2023-3649.
18. Panwar M, Gautam A, Biswas D, Acharyya A. PP-Net: A deep learning framework for PPG-based blood pressure and heart rate estimation. IEEE Sens J. 2020;20(17):10000-11. doi:10.1109/JSEN.2020.2990864.
19. Fedorovich AA, Drapkina OM, Pronko KN, et al. Telemonitoring of capillary blood flow in human skin: new opportunities and prospects. Clin Pract. 2018;15(2):561-7. doi:10.4172/clinical-practice.1000390.
20. Федорович А. А., Горшков А. Ю., Драпкина О. М. Современные возможности неинвазивного исследования и дистанционного мониторинга капиллярного кровотока в коже человека. Регионарное кровообращение и микроциркуляция. 2020;19(4):87-91. doi:10.24884/1682-6655-2020-19-4-87-91.
21. Федорович А. А., Драпкина О. М. Веб-капилляроскопия — новый метод неинвазивного исследования микроциркуляторного кровотока в коже человека. Профилактическая медицина. 2020;23(4):115-8. doi:10.17116/profmed202023041115.
22. Poh MZ, McDuff DJ, Picard RW. Noncontact, automated cardiac pulse measurements using video imaging and blind source separation. Opt Express. 2010;18(10):10762-74. doi:10.1364/OE.18.010762.
23. Scully CG, Lee J, Meyer J, et al. Physiological parameter monitoring from optical recordings with a mobile phone. IEEE Trans Biomed Eng. 2012;59(2):303-6. doi:10.1109/TBME.2011.2163157.
24. Yan BP, Lai WHS, Chan CKY, et al. Contactfree screening of atrial fibrillation by a smartphone using facial pulsatile photoplethysmographic signals. J Am Heart Assoc. 2020;7(8):e008585. doi:10.1161/JAHA.118.008585.
25. Yan BP, Lai WHS, Chan CKY, et al. Highthroughput, contactfree detection of atrial fibrillation from video with deep learning. JAMA Cardiol. 2020;5(1):105-7. doi:10.1001/jamacardio.2019.4004.
26. Varma N, Cygankiewicz I, Turakhia M, et al. 2021 ISHNE/HRS/EHRA/APHRS collaborative statement on mHealth in arrhythmia management: digital medical tools for heart rhythm professionals. Ann Noninvasive Electrocardiol. 2021;26(2):e12795. doi:10.1111/anec.12795.
27. Luo H, Yang D, Barszczyk A, et al. Smartphone-dases blood pressure measurement using transdermal optical imaging technology. Circ Cardiovasc Imaging. 2019;12:e008857. doi:10.1161/CIRCIMAGING.119.008857.
28. Schoettker P, Degott J, Hofmann G, et al. Blood pressure measurements with the OptiBP smartphone app validated against reference auscultatory measurements. Sci Rep. 2020;10:17827. doi:10.1038/s41598-020-74955-4.
Об авторах
А. А. ФедоровичРоссия
Андрей Александрович Федорович — к.м.н., с.н.с. лаборатории "Микроциркуляции и регионарного кровообращения", с.н.с. лаборатории "Вегетативной регуляции сердечно-сосудистой системы".
Москва
А. И. Королев
Россия
Андрей Игоревич Королев — к.м.н., руководитель лаборатории "Микроциркуляции и регионарного кровообращения".
Москва
В. С. Ососков
Россия
Виталий Сергеевич Ососков — м.н.с. лаборатории "Микроциркуляции и регионарного кровообращения".
Москва
К. С. Саматова
Россия
Камила Саматовна Саматова — аспирант.
Москва
О. М. Драпкина
Россия
Оксана Михайловна Драпкина — д.м.н., профессор, академик РАН, директор.
Москва
Дополнительные файлы
Что известно о предмете исследования?
- Микрососудистое русло кожи имеет сложно организованную, 3-звенную систему строения.
- Существует большое количество инструментальных методов для неинвазивного исследования микроциркуляции (МЦ) в коже человека.
Что добавляют результаты исследования?
- Приводится оценка диагностического потенциала трех различных исследовательских приборов с учетом физических принципов их функционирования, которые, исходя из особенностей ангиоархитектоники микрососудистого русла кожи, позволяют получать информацию физиологического характера от каждого звена микрососудистого русла кожи человека.
- Кратко описаны появившиеся за последние 5-8 лет современные портативные варианты всех трех типов приборов, что позволяет существенно расширить возможности исследователей по дистанционному мониторингу системы МЦ у человека.
- Кратко описан новый диагностический подход к исследованию МЦ в коже человека, который не требует специализированного медицинского оборудования и базируется на использовании стандартной пользовательской веб-камеры.
Рецензия
Для цитирования:
Федорович А.А., Королев А.И., Ососков В.С., Саматова К.С., Драпкина О.М. Новые тренды развития направления по неинвазивному исследованию микроциркуляции в коже человека. Описательный обзор. Кардиоваскулярная терапия и профилактика. 2025;24(6):4412. https://doi.org/10.15829/1728-8800-2025-4412. EDN: XFFGNI
For citation:
Fedorovich A.A., Korolev A.I., Ososkov V.S., Samatova K.S., Drapkina O.M. New trends in non-invasive study of human skin microcirculation. A descriptive review. Cardiovascular Therapy and Prevention. 2025;24(6):4412. (In Russ.) https://doi.org/10.15829/1728-8800-2025-4412. EDN: XFFGNI
JATS XML

























































