Перейти к:
Стратификация риска хирургических и сердечно-сосудистых осложнений в некардиальной хирургии: прогностическая значимость рекомендуемых шкал
https://doi.org/10.15829/1728-8800-2024-4016
EDN: MCKFPK
Аннотация
Цель. Оценить прогностическую значимость применяемых в настоящее время шкал и индексов для стратификации риска развития любых хирургических и сердечно-сосудистых осложнений (ССО) у пациентов, подвергающихся некардиальным хирургическим вмешательствам.
Материал и методы. Проведено одноцентровое когортное ретроспективное исследование у пациентов, которым были выполнены внесердечные оперативные вмешательства в 2018 и 2020гг. Хирургические послеоперационные осложнения (ПО) оценивали согласно классификации Clavien-Dindo. К ССО относили любые сердечно-сосудистые события — AnyCVE (Аny Cardio-Vascular Events): MACE (Major Adverse Cardiac Events); динамику ST-T на электрокардиограмме (ЭКГ); развитие острой или декомпенсацию хронической сердечной недостаточности (СН); аритмии; развитие эпизодов гипотонии или гипертонии; делирий; кровотечения; тромбоэмболические осложнения (ТЭО). Стратификация риска ПО проведена с использованием рекомендуемых прогностических шкал и индексов. Прогностическую значимость шкал и индексов определяли на основании ROC-анализа с оценкой площади под кривой (AUС).
Результаты. Стратификация риска ПО проведена у 2937 пациентов. Прогностическая ценность шкал и индексов: шкала POSSUM (Physiological and Operative Severity Score for the enUmeration of Mortality and morbidity) — AUC 0,990, 0,808, 0,825, 0,841, 0,808, 0,793, 0,701, 0,776, 0,744 в прогнозировании вероятности развития Claviеn-Dindo 5, 4 ст., СН, делирия, ТЭО, MACE, ЭКГ ST-T, аритмий, кровотечений; шкала SORT (Surgical Outcome Risk Tool) — AUC 0,973, 0,740, 0,890, 0,763, 0,721, 0,716, 0,700 в прогнозировании Claviеn-Dindo 5, 4 ст., делирия, MACE, СН, аритмии, ТЭО, соответственно; АSA (American Association of Anaesthetists) — AUC 0,648, 0,600, 0,658 в отношении СН, ЭКГ ST-T, аритмий; индекс коморбидности Charlson — AUC 0,819, 0,950, 0,789, 0,788, 0,706, 0,771, 0,898 в прогнозировании Claviеn-Dindo 4, 5 ст., MACE, CН, ЭКГ ST-T, аритмии, делирия; шкала хирургического риска, ассоциированная с риском развития кардиальных осложнений, — AUC 0,989, 0,887, 0,728 для Clavien-Dindo 3, 5 ст., MACE; индекс rRCRI (реконструированный Revised Cardiac Risk Index) — AUC 0,916 и 0,979, 0,762, 0,741, 0,737 в прогнозировании Clavien-Dindo 3, 5 ст., СН, аритмии, делирия; NSQIP MICA (National Surgical Quality Improvement Program Myocardial Infarction & Cardiac Arrest) — AUC 0,705, 0,757, 0,718 для аритмии, делирия, ТЭО; общий сердечно-сосудистый риск согласно рекомендациям ESC (European Society of Cardiology) 2022 — AUC 0,942, 0,726, 0,701, 0,748, 0,785 для Clavien-Dindo 5 ст., MACE, ЭКГ ST-T, аритмий, делирия; шкала Caprini — AUC 0,718 и VTE-Bleed (Venous ThromboEmbolism and Bleeding) — AUC 0,722 в прогнозировании ТЭО; упрощенный индекс BIMS (Вleeding Independently associated with Mortality after noncardiac Surgery) — AUC 0,729 для стратификации кровотечений. В оценке вероятности развития в целом хирургических осложнений Clavien-Dindo и AnyCVE ни одна из шкал не показала прогностической ценности >0,7.
Заключение. Для стратификации AnyCVE требуется усовершенствование имеющихся и разработка новых прогностических инструментов.
Ключевые слова
Для цитирования:
Мурашко С.С., Бернс С.А., Пасечник И.Н. Стратификация риска хирургических и сердечно-сосудистых осложнений в некардиальной хирургии: прогностическая значимость рекомендуемых шкал. Кардиоваскулярная терапия и профилактика. 2024;23(7):4016. https://doi.org/10.15829/1728-8800-2024-4016. EDN: MCKFPK
For citation:
Murashko S.S., Berns S.A., Pasechnik I.N. Risk stratification of surgical and cardiovascular complications in non-cardiac surgery: prognostic value of recommended scales. Cardiovascular Therapy and Prevention. 2024;23(7):4016. (In Russ.) https://doi.org/10.15829/1728-8800-2024-4016. EDN: MCKFPK
Введение
Хирургические вмешательства выполняются ежегодно ~5% мирового населения, 85% из них составляют некардиальные операции [1]. Сердечно-сосудистые осложнения (ССО) занимают одну из лидирующих позиций в структуре послеоперационных осложнений (ПО) и являются предметом множества исследований, посвященных стратификации риска их развития [2]. Частота развития осложнений в течение 7 дней после некардиальных операций составляет 16,8%, из них 2,8% являются летальными, по данным проспективного когортного исследования исходов после плановых оперативных вмешательств у 44814 пациентов из 27 стран мира [3]. Среди ведущих причин послеоперационных летальных исходов выделяют: крупные кровотечения (15,6%), повреждение миокарда (13%) и сепсис (4,5%) [4]. Общепринятого стандартного определения или классификации послеоперационных ССО на сегодняшний день не существует. Наиболее часто для описания конечных точек, относящихся к сердечно-сосудистым событиям при различных методах лечения, в т.ч. в некардиальной хирургии, используется термин МАСЕ (Major Adverse Cardiovascular Events). В понятие термина МАСЕ наряду с основными исходами (острый инфаркт миокарда (ИМ), ишемический инсульт, сердечно-сосудистая смерть), исследователи включают также нестабильную стенокардию, сердечную недостаточность (СН), нарушения ритма сердца и проводимости, тромбоэмболические осложнения (ТЭО) и др. [5]. Оперативные вмешательства у кардиологических пациентов, получающих длительную антитромботическую терапию, сопряжены с повышенным риском геморрагических и ТЭО. Thiele RH, et al. (2019) указывают на более широкое понимание MACE благодаря использованию сердечного тропонина (cTn) для диагностики миокардиального повреждения, мозгового натрийуретического пептида для диагностики СН, применению магнитно-резонансной томографии для выявления послеоперационных бессимптомных инсультов и рассматривают ПО как исход дисфункции органов (сердца, головного мозга, почек, органов желудочно-кишечного тракта и т.д.) вследствие ишемии, кровотечения, тромбозов [6]. В исследовании NeuroVISION (Detection and Neurological Impact of CerebroVascular Events In Noncardiac Surgery Patients: a COhort EvaluatioN Study) продемонстрировано, что применение магнитно-резонансной томографии позволило выявить бессимптомные послеоперационные инсульты у 7% прооперированных, из них у 42% пациентов в течение года отмечалось снижение когнитивных способностей, а в послеоперационном периоде был достоверно повышен риск развития послеоперационного делирия (hazard ratio, отношение рисков 2,24, 95% доверительный интервал (ДИ): 1,06-4,73, p=0,030) [7].
В поиске моделей стратификации риска ПО большое внимание уделяется созданию унифицированных прогностических шкал и индексов, удобных в использовании врачами и позволяющих наглядно информировать пациента о возможных рисках оперативного вмешательства [8]. Европейское общество кардиологов (The European Society of Cardiology — ESC) разработало и рекомендует использовать алгоритм периоперационного ведения пациентов при некардиальных хирургических вмешательствах, основанный на оценке общего сердечно-сосудистого риска (ССР), который включает риск, связанный с пациентом, и риск хирургического вмешательства [1]. Российское кардиологическое общество при некардиальных операциях также рекомендует оценивать ССР, связанный с состоянием пациента и особенностями хирургического вмешательства, и использовать унифицированные прогностические шкалы, модели и индексы [9]. Среди рекомендуемых прогностических инструментов, выделяют модели, оценивающие широкий спектр ПО — калькулятор Американского колледжа хирургов (the American College of Surgeons National Surgical Quality Improvement Program — ACS NSQIP), оценку физиологической и операционной тяжести для подсчета смертности и заболеваемости (Physiological and Operative Severity Score for the enUmeration of Mortality and morbidity — POSSUM), шкалу риска исхода в хирургии (Surgical Outcome Risk Tool — SORT). Для оценки ССО рекомендуется использование пересмотренного индекса сердечного риска (Revised Cardiac Risk Index — RCRI или rRCRI), универсальной шкалы для оценки ССР перед несердечными и сердечными операциями (the National Surgical Quality Improvement Program Myocardial Infarction & Cardiac Arrest — NSQIP MICA или Gupta MICA) [9]. Широко используемыми в клинической практике являются шкала (классификация) оценки тяжести физического состояния больного перед оперативным вмешательством Американской Ассоциации Анестезиологов (American Association of Anaesthetists — ASA), шкала (классификация) оценки хирургического риска кардиоваскулярных осложнений в зависимости от типа оперативного вмешательства, индекс RCRI, шкала индивидуальной оценки риска венозных ТЭО Caprini.
Следует отметить, что рекомендованные и используемые разнообразные прогностические инструменты демонстрируют широкую вариабельность предсказательной ценности, различия в прогнозе риска достигают до 29% несовпадений [9][10].
Цель исследования — оценить прогностическую значимость применяемых в настоящее время шкал и индексов для стратификации риска развития любых хирургических и ССО у пациентов, подвергающихся некардиальным хирургическим вмешательствам.
Материал и методы
Проведено одноцентровое когортное ретроспективное исследование по стратификации риска послеоперационных госпитальных осложнений с использованием рекомендуемых прогностических шкал и индексов у всех пациентов, которым были выполнены внесердечные оперативные вмешательства в 2018 и 2020гг. Данные о клинико-демографических характеристиках пациентов и особенностях оперативных вмешательств получены из бумажной формы стационарной истории болезни пациентов, оперированных в 2018г, и из электронной базы данных медицинской информационной системы "1С: Медицина. Больница" пациентов, оперированных в 2020г.
Критериями исключения из исследования были случаи оперативного вмешательства офтальмологического профиля в связи с узким спектром хирургического вмешательства и короткими сроками стационарного наблюдения (1-2 сут.) и эндокринологического профиля в связи с малым количеством оперативных вмешательств данного профиля.
У всех пациентов был проведен анализ частоты фактического развития любых хирургических ПО согласно классификации Claviеn-Dindo и любых сердечно-сосудистых ПО AnyCVE (Any Cardio-Vascular Events); стратификация риска ПО с использованием рекомендуемых шкал и индексов и оценка их прогностической значимости в предсказании вероятности развития любых хирургических и ССО.
Хирургические ПО, к которым относились любые негативные события, возникшие после операции на госпитальном этапе, согласно классификации Clavien-Dindo распределялись по 5 группам [11]. Осложнения 1 ст. включали любые отклонения от нормы в послеоперационном периоде, которые не требовали хирургического, эндоскопического и радиологического вмешательства. Проводилась стандартная консервативная терапия (жаропонижающие, анальгетики, диуретики, противорвотные средства, растворы электролитов, антибактериальная терапия раневой инфекции). Осложнения 2 ст. требовали расширения объема медикаментозной терапии, переливания крови и парентерального питания. Осложнениями 3а и 3b ст. считалась необходимость повторных вмешательств (оперативных, эндоскопических или радио-логических) без или с общей анестезии, соответственно. Осложнения 4 ст. подразделялись на 4a, когда имелась недостаточность функции одного органа, и 4b при полиорганной недостаточности. Осложнениям 5 ст. соответствовал летальный исход.
CCО рассматривались как любые отклонения деятельности сердечно-сосудистой системы от нормальных значений на госпитальном этапе (AnyCVE) [12] и включали: MACE — сердечно-сосудистую смерть, ИМ, острое, либо преходящее нарушение мозгового кровообращения, динамику ST-T на электрокардиограмме (ЭКГ) (расценивалось как миокардиальное повреждение в случае повышения уровня cTn и как ЭКГ-изменения ST-T в отсутствие повышения уровня cTn); СН — развитие острой или декомпенсацию хронической СН; аритмии — нарушения ритма и проводимости сердца, включая пароксизмы фибрилляции предсердий, суправентрикулярной тахикардии, частой желудочковой экстрасистолии ≥3 класса по Лауну, впервые зарегистрированные нарушения проводимости или прогрессирование ранее имеющейся степени нарушений проводимости сердца; артериальное давление (АД) — развитие эпизодов гипотонии (снижение систолического АД (САД) <90 мм рт.ст.) или гипертонии (повышение САД >160 мм рт.ст.); делирий — послеоперационный делирий, под которым понималось острое изменение психического статуса в виде дезориентации в пространстве и времени, снижение внимания, нарушение сна и бодрствования; кровотечения — кровопотеря >500 мл; ТЭО — включали тромбоз глубоких вен и/или тромбоэмболию легочной артерии.
Для стратификации общего хирургического риска ПО мы использовали шкалы POSSUM, SORT; для оценки риска развития ССО — шкалу хирургического риска, ассоциированного с риском развития кардиальных осложнений (далее — хирургическая шкала кардиального риска), индекс rRSRI, NSQIP MICA, оценку общего ССР согласно Европейским клиническим рекомендациям ESC 2022г (далее — ESC, 2022); для оценки состояния пациента использовали классификацию ASA, Индекс коморбидности Charlson; для оценки риска ТЭО и кровотечения — шкалу Caprini, классификацию инвазивных процедур/вмешательств в зависимости от величины ассоциированного с ними риска кровотечений (далее — шкала риска кровотечений), шкалу риска кровотечения у пациентов, получающих антикоагулянтную терапию по поводу риска ТЭО (Venous ThromboEmbolism and Bleeding — VTE-Bleed), индекс риска кровотечения, независимо связанного со смертью после некардиальных операций (Вleeding Independently associated with Mortality after noncardiac Surgery — BIMS).
Статистический анализ проводился с использованием программы StatTech v. 4.1.2 (разработчик — ООО "Статтех", Россия). Категориальные данные описывались с указанием абсолютных значений и процентных долей. Количественные показатели оценивались на предмет соответствия нормальному распределению с помощью критерия Шапиро-Уилка (при числе исследуемых <50) или критерия Колмогорова-Смирнова (при числе исследуемых >50). В случае отсутствия нормального распределения количественные данные описывались с помощью медианы (Me) и интерквартильного размаха (Q25-Q75). Построение прогностической модели вероятности определенного исхода выполнялось при помощи метода логистической регрессии. Мерой определенности, указывающей на ту часть дисперсии, которая может быть объяснена с помощью логистической регрессии, служил коэффициент R2 Найджелкерка. Для оценки прогностической значимости исследуемых шкал и индексов при стратификации определенного исхода, применялся метод анализа ROC-кривых. Пороговое значение (отрезная точка) (cut-off) определялась по наивысшему значению индекса Юдена. Прогностическая ценность полученной модели оценивалась с помощью определения площади под ROC-кривой (AUС). Результат AUС <0,61 свидетельствовал о плохом качестве модели, 0,61-0,70 — о среднем качестве, 0,71-0,80 отражал хорошую прогностическую ценность модели, 0,81-0,90 — очень хорошую прогностическую ценность, результат ≥0,91 оценивал модель, как обладающую отличной прогностической ценностью [13]. Различия считались статистически значимыми при p<0,05.
Результаты и обсуждение
Из 3063 стационарных историй болезни пациентов >18 лет, перенесших некардиальные вмешательства в 2018 и 2020гг, в исследование было отобрано 2937. Исключены 118 случаев оперативных вмешательств офтальмологического профиля и 5 случаев эндокринологического профиля (рисунок 1). Время наблюдения соответствовало длительности госпитализации, Me времени наблюдения составила 7 дней (Q25-Q75 — 3-11 дней).
Клинико-демографическая характеристика исследуемой когорты пациентов представлена в таблице 1. Возраст участников исследования варьировал от 18 до 98 лет, значимых различий по полу отмечено не было. Хронические неинфекционные заболевания (ХНИЗ) имели 50,6% пациентов, среди ХНИЗ преобладали хронические болезни системы кровообращения (88,7%). По данным национального обсервационного многоцентрового исследования Федерации анестезиологов и реаниматологов (Роль сопутствующих заболеваний в стратификации риска послеоперационных осложнений в абдоминальной хирургии — STOPRISK), сопутствующие заболевания имели 56,3% пациентов, причем преобладали гипертоническая болезнь (48,2%), хроническая СН (20,7%), ишемическая болезнь сердца (19,3%) [14]. Оперативные вмешательства в нашем исследовании выполнены в плановом порядке в 92,3% случаев, по области вмешательства представлены широким спектром, анестезиологическое пособие обеспечивалось с преимущественным использованием комбинированной общей анестезии — в 37,5% случаев и тотальной внутривенной анестезии — 32,8%.
Все случаи наблюдения были проанализированы на наличие послеоперационных хирургических и ССО. Частота выявленных в нашем исследовании послеоперационных осложнений соответствует мировым показателям. Любые хирургические осложнения по классификации Clavien-Dindo были зафиксированы в 54,7% случаев, из них хирургические осложнения 1 ст. — в 33,9%, 2-5 ст. — в 20,8% (рисунок 2). По литературным данным частота хирургических ПО составляет 27,7%, варьируя от 10,7 до 71,4% [15]; частота развития MACE в последние десятилетия стремительно снижается и в настоящее время составляет 0,5-1,4% [16][17]. Развитие МACE в настоящем исследовании зарегистрировано в 0,2% случаев. Мы оценили частоту развития любого ССО AnyCVE, которая составила 13,3%. В последние годы увеличивается количество исследований, указывающих на клинико-экономическую значимость стратификации риска любых ССО [12][18-22]. При структурном анализе AnyCVE выявлено, что наиболее часто регистрировались колебания САД <90 мм рт.ст. или >160 мм рт.ст. — 6,3% случаев, нарушения ритма и проводимости сердца — 2,6% случаев, кровотечения — 2,4%, ЭКГ изменения SТ-Т — 2,3%, ТЭО — 1,1%, СН — 0,7%, делирий — 0,3% (рисунок 2).
В литературе представлены данные большого количества сравнительных исследований по оценке прогностической значимости различных шкал и индексов. Анализ показывает, что они разрабатывались на неоднородных группах по демографическим и клиническим показателям, по видам хирургического вмешательства, с использованием разных предикторов, разных прогностических моделей, целью своей имели оценку различных хирургических и сердечно-сосудистых событий, в результате чего прогностическая ценность шкал и индексов имеет большой диапазон несовпадений. Так, в систематическом обзоре 11 исследований прогностической значимости шкал и индексов представлен пример оценки периоперативных кардиальных исходов у одной пациентки, равный 9,1% по шкале rRSRI, а по онлайн-калькулятору NSQIP MICA — 0,8%. В данном исследовании показано, что крупные исследования на большом количестве пациентов со стандартизированной методологией сбора данных, более длительным периодом наблюдения имеют более высокую точность прогнозирования (AUC 0,85-0,90), однако они оценивают небольшое количество исходов, чаще всего симптоматический ИМ и остановку сердца. Это же сравнительное исследование свидетельствует о значимости прогностических шкал и индексов, разработанных на меньшем количестве пациентов, с более низкой прогностической точностью (0,70-0,79), но дающих дополнительный вклад в оценку более широкого перечня переменных и сердечно-сосудистых исходов (аритмии, СН и т.д.), имеющих большое клиническое значение [23].
Анализ результатов настоящего исследования стратификации риска ПО у 2937 пациентов по 12 шкалам свидетельствует о тех же тенденциях:
1) выявлен довольно большой разброс вероятности развития тех или иных осложнений: развития заболеваний и смерти от всех причин в послеоперационном периоде (9-11,7%), развития MACE (0,5-48,9%), развития кровотечения и ТЭО (4,1-42,6%) (рисунок 3);
2) в оценке вероятности развития в целом хирургических осложнений Clavien-Dindo и AnyCVE ни одна из шкал не показала прогностической ценности >0,7;
3) предсказательная ценность шкал возрастала при использовании их в стратификации отдельных категорий осложнений согласно классификации Clavien-Dindo и AnyCVE.
Сравнительная оценка шкал и индексов в прогнозировании ПО по степеням тяжести согласно классификации Claviеn-Dindo и отдельным показателям AnyCVE по ранее описанным критериям (MACE, изменения ST-T, СН, аритмии, АД, делирий, ТЭО, кровотечения) представлена в таблице 2. В прогнозировании осложнений Claviеn-Dindo 3 ст. отличное качество продемонстрировали модели хирургической шкалы кардиального риска и rRSRI. В прогнозировании хирургических осложнений 4 и 5 ст. по Claviеn-Dindo хорошее и очень хорошее качество проявили все анализируемые шкалы, за исключением ASA, NSQIP MICA, BIMS. При прогнозировании MACE С-статистику >0,7 продемонстрировали все шкалы, за исключением ASA, rRSRI, NSQIP MICA; СН — POSSUM, SORT, Сharlson, rRSRI, VTE-bleed; делирия — все шкалы, за исключением ASA, хирургической шкалы кардиального риска; ТЭО — POSSUM, SORT, NSQIP MICA, Caprini, VTE-bleed. С удовлетворительной оценкой предсказывали изменения ЭКГ ST-T шкалы POSSUM, SORT, Сharlson, rRSRI, ESC 2022, Caprini; аритмии — все анализируемые шкалы, за исключением ASA, хирургической шкалы кардиального риска; кровотечения — POSSUM и BIMS. Шкала риска кровотечений не продемонстрировала прогностической значимости выше средней. Колебания АД не предсказывала ни одна из анализируемых шкал.
Рекомендованные шкалы и индексы были разработаны либо для стратификации только серьезных кардиальных осложнений, либо для широкого перечня заболеваний, в т.ч. включающих сердечно-сосудистые заболевания.
Шкала POSSUM была изначально разработана на основании изучения 1372 пациентов для оценки качества оказания медицинской помощи, в последующем была доработана для оценки риска осложнений (кровотечение из раны, глубокое кровотечение, инфекция, септицемия, раневая инфекция, лихорадка неясного генеза, мочевая инфекция, глубокая инфекция, расхождение раны или несостоятельность анастомоза, тромбоз глубоких вен и тромбоэмболия легочной артерии, СН, нарушение функции почек, гипотензия, "любое другое осложнение") и смерти при плановых или неотложных оперативных вмешательствах, содержит 12 параметров для оценки физиологического состояния пациента и 6 параметров для оценки тяжести операции, учитывает не только предоперационные, но и интра- и послеоперационные параметры. POSSUM во многих исследованиях показала хорошее качество, но не нашла широкого клинического применения из-за требуемого большого количества параметров для оценки. Было показано, что POSSUM является наиболее точной шкалой в предсказании осложнений в течение 30 дней после операций с высокой прогностической ценностью — AUC 0,7-0,92 [14]. В нашем исследовании шкала POSSUM продемонстрировала самую высокую прогностическую значимость, причем позволяла предсказать вероятность не только хирургических, но и большого спектра сердечно-сосудистых исходов с отличным, очень хорошим и хорошим качеством модели: Claviеn-Dindo 5 ст., 4 ст., СН, делирия, ТЭО, MACE, ЭКГ ST-T, аритмий, кровотечений с AUC, соответственно, 0,990, 0,808, 0,825, 0,841, 0,808, 0,793, 0,701, 0,776, 0,744 (таблица 2).
Конкурирующие позиции с POSSUM по литературным данным занимают шкалы SORT и ASA. Эти шкалы просты в оценке, широко используются и имеют практическую значимость. В Британском журнале анестезиологии приводятся результаты сравнительного исследования, в котором шкала SORT показала более высокие значения AUC (0,72-0,90), чем POSSUM (0,60-0,89) [24][25]. Сравнение SORT и ASA тоже продемонстрировало лучшие значения AUC для шкалы SORT 0,91 (95% ДИ: 0,88-0, 94) по сравнению с 0,87 (95% ДИ: 0,84-0,91) для ASA [26]. В настоящем исследовании стратификация риска ПО по шкале SORT незначительно уступала шкале POSSUM. Качество модели SORT в прогнозировании таких осложнений, как Claviеn-Dindo 5 ст., делирия, Claviеn-Dindo 4 ст., MACE, СН, аритмии, ТЭО соответствовало AUC — 0,973, 0,890, 0,740, 0,763, 0,721, 0,716, 0,700, соответственно. АSA имела среднюю предсказательную ценность в отношении СН, ЭКГ ST-T, аритмий (AUC — 0,648, 0,600, 0,658, соответственно), с остальными исходами не имела достоверной значимой связи. Надо отметить, что ASA создавалась не для оценки риска, а как классификатор, субъективность в ее оценке могла повлиять на предсказательную ценность ASA в настоящем исследовании.
Учитывая тот факт, что в последние десятилетия среди оперированных пациентов возрастает доля пожилых и лиц старческого возраста с полиморбидной патологией [27], для оценки риска ПО используют индекс коморбидности Charlson [28]. В настоящем исследовании индекс Charlson зарекомендовал себя как модель очень хорошего и отличного качества для прогнозирования хирургических осложнений 4 и 5 ст. по Claviеn-Dindo (AUC — 0,819 и 0,950, соответственно) и хорошего качества для предсказания MACE, CН, ЭКГ ST-T, аритмии, делирия (AUC — 0,789, 0,788, 0,706, 0,771, 0,898, соответственно), что может свидетельствовать о значительном вкладе коморбидности в риск развития ПО у пациентов, подвергающихся некардиальным оперативным вмешательствам.
Шкалы, калькуляторы, алгоритмы, созданные непосредственно для стратификации кардиального риска, не продемонстрировали высокой прогностической ценности. Хирургическая шкала кардиального риска в настоящем исследовании имела отличное, очень хорошее и хорошее качество только для стратификации хирургических осложнений 3 и 5 ст. по Clavien-Dindo и MACE (AUC — 0,989, 0,887, 0,728), что соответствует ее предназначению. Индекс rRSRI имел отличное качество в прогнозировании хирургических осложнений 3 и 5 ст. по Clavien-Dindo (AUC — 0,916 и 0,979), но для прогнозирования ССО показал лишь хорошее качество (AUC — 0,762, 0,741, 0,737 для стратификации СН, аритмии и делирия, соответственно). Калькулятор NSQIP MICA ассоциировался с хорошей предсказательной ценностью только для аритмии, делирия и ТЭО (AUC — 0,705, 0,757, 0,718). Общий ССР, согласно рекомендациям ESC 2022, продемонстрировал отличное качество в предсказании хирургических осложнений 5 ст. (AUC 0,942) и хорошую ценность при прогнозировании MACE, ЭКГ ST-T, аритмий и делирия (AUC — 0,726, 0,701, 0,748, 0,785, соответственно). Колебания АД ни одна модель не предсказывала с точностью >0,7 по С-статистике. Литературные данные свидетельствуют о довольно высокой точности прогнозирования кардиальных осложнений калькулятора NSQIP MICA (AUC — 0,83-0,90), существенно превосходящую точность rRSRI (0,70-0,79), однако калькулятор NSQIP MICA создавался для предсказания только ИМ и остановки сердца, а rRSRI призван предсказывать не только ИМ и остановку сердца, но и СН, нарушения ритма сердца, смерть от кардиальных причин [23]. Надо отметить, что валидность данных прогностических моделей существенно различается в разных исследованиях, показывая порой крайне низкие значения C-статистики для NSQIP MICA — 0,64 (95% ДИ; 0,57-0,70) и для RCRI — 0,60 (95% ДИ; 0,54-0,65) [29]. Несмотря на указание в некоторых исследованиях на неудовлетворительное качество в предсказании кардиального риска (AUC — 0,53, 95% ДИ: 0,45-0,61), rRSRI остается наиболее широко используемым инструментом для оценки периоперационного риска серь-
езных сердечных осложнений из-за простоты ее применения [30]. Ранее разработанные шкалы для стратификации кардиальных осложнений не оценивали риск развития миокардиального повреждения или динамики на ЭКГ ST-T. Среди рекомендованных шкал и индексов нет моделей, прогнозирующих значимые колебания АД в периоперационном периоде. Литературных данных по изучению прогностической ценности индекса общего ССР согласно алгоритму ESC 2022 еще не представлено. Большое внимание уделяется прогнозированию делирия, разрабатываются модели с очень хорошей прогностической ценностью (AUC — 0,84) [31].
Среди моделей, используемых для стратификации риска венозных ТЭО и кровотечений, в настоящем исследовании показали хорошее качество для ТЭО шкала Caprini и VTE-Bleed (AUC 0,718 и 0,722), для кровотечения — упрощенный индекс BIMS (AUC — 0,729), что соответствует и литературным данным. Согласно результату систематического анализа 51 исследования по изучению прогностической ценности различных шкал, включая Caprini, призванных стратифицировать риск развития венозных ТЭО у госпитализированных пациентов, были выявлены существенные различия С-статистики, преимущественно среднее и хорошее качество моделей, большой разброс чувствительности и специфичности шкал — от 7,2 до 100% [32]. Результаты проспективного исследования в 8 странах мира упрощенного индекса BIMS свидетельствуют о хорошем качестве данной модели (AUC — 0,787) [33]. Классификация инвазивных процедур/вмешательств в зависимости от величины ассоциированного с ними риска кровотечений в настоящем исследовании показала низкую прогностическую значимость (AUC — 0,616), что соответствует литературным данным (AUC — 0,71) [34].
Ограничения исследования. С ретроспективным дизайном исследования могут быть связаны возможные систематические ошибки информации архивных данных стационарных историй болезни. Исследование проведено в одном медицинском центре, что может привести к проблемам внешней обобщаемости результатов исследования. Трудности сравнения результатов исследования обусловлены ограниченным количеством сопоставимых данных в литературе.

Рис. 1 Протокол исследования.
Примечание: AUC — Area Under the ROC Curve, AnyCVE — Any CardioVascular Events, ASA — American Association of Anaesthetists, BIMS — Вleeding Independently associated with Mortality after noncardiac Surgery, NSQIP MICA — the National Surgical Quality Improvement Program Myocardial Infarction & Cardiac Arrest, POSSUM — Physiological and Operative Severity Score for the enUmeration of Mortality and morbidity, RCRI или rRCRI — Revised Cardiac Risk Index, SORT — Surgical Outcome Risk Tool, VTE-Bleed — Venous ThromboEmbolism and Bleeding.
Таблица 1
Характеристика участников исследования
Показатель | Me (Q25-Q75)/n, % |
Возраст, лет | 59 (45-68) |
Пол Ж М | 1514 (51,5) 1423 (48,5) |
ХНИЗ Болезни системы кровообращения Хронические бронхолегочные заболевания Сахарный диабет II типа Онкологические заболевания | 1486 (50,6) 1318 (88,7) 248 (16,3) 339 (22,8) 236 (15,9) |
Длительность госпитализации, дней | 7 (3-11) |
Срочность операции — планово — экстренно | 2710 (92,3) 227 (7,7) |
Область операции Абдоминальная Гинекология Урология Травматология-ортопедия Нейрохирургия Колопроктология Эндоскопия Кожа Сосуды | 374 (12,7) 500 (17,0) 535 (21,6) 495 (16,9) 429 (14,6) 69 (2,3) 294 (10,0) 39 (1,3) 102 (3,5) |
Вид анестезии ТВА Местная Регионарная КОА Сочетанная | 964 (32,8) 263 (9,0) 514 (17,5) 1102 (37,5) 94 (3,2) |
Примечание: КОА — комбинированная общая анестезия, Ме — медиана, ТВА — тотальная внутривенная анестезия, ХНИЗ — хронические неинфекционные заболевания.
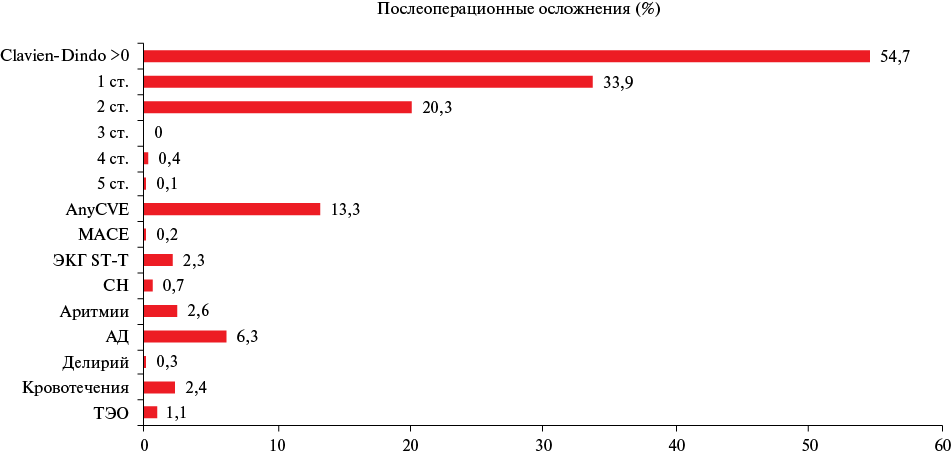
Рис. 2 Послеоперационные осложнения (%).
Примечание: АД — эпизоды гипотонии или гипертонии, СН — сердечная недостаточность, ст. — степень, ТЭО — тромбоэмболические осложнения, ЭКГ — электрокардиограмма, AnyCVE — Any CardioVascular Events, МАСЕ — Major Adverse Cardiac Events.
Таблица 2
Сравнительная характеристика прогностической ценности шкал и индексов по данным ROC-анализа и значениям AUC
Шкала/Индекс | Clavien-Dindo 3 | Clavien-Dindo 4 | Clavien-Dindo 5 | MACE | СН | ЭКГ ST-T | Аритмии | Делирий | ТЭО | Кровотечения |
POSSUM | – | 0,808 | 0,990 | 0,793 | 0,825 | 0,701 | 0,776 | 0,841 | 0,800 | 0,744 |
SORT | – | 0,740 | 0,973 | 0,763 | 0,721 | 0,675 | 0,716 | 0,890 | 0,700 | 0,622 |
ASA | – | – | – | – | 0,648 | 0,600 | 0,658 | – | – | – |
Сharlson | – | 0,819 | 0,950 | 0,798 | 0,788 | 0,706 | 0,771 | 0,898 | 0,694 | 0,598 |
Хирургическая шкала кардиального риска | 0,989 | – | 0,887 | 0,728 | – | 0,592 | 0,606 | 0,589 | 0,569 | 0,607 |
rRSRI | 0,916 | 0,762 | 0,979 | 0,652 | 0,762 | 0,636 | 0,741 | 0,737 | 0,620 | 0,555 |
NSQIP MICA | – | 0,645 | – | – | 0,680 | 0,664 | 0,705 | 0,757 | 0,718 | 0,610 |
ESC 2022 | – | 0,655 | 0,942 | 0,726 | 0,605 | 0,701 | 0,748 | 0,785 | 0,699 | 0,658 |
Caprini | – | 0,733 | – | 0,714 | 0,652 | 0,708 | 0,707 | 0,776 | 0,718 | 0,685 |
VTE-Bleed | – | 0,851 | 0,905 | 0,832 | 0,809 | 0,673 | 0,747 | 0,818 | 0,722 | 0,672 |
BIMS | – | 0,680 | – | 0,769 | – | 0,584 | 0,665 | 0,727 | 0,676 | 0,729 |
Примечание: СН — сердечная недостаточность, ТЭО — тромбоэмболические осложнения, ЭКГ — электрокардиограмма, ACS NSQIP — the American College of Surgeons National Surgical Quality Improvement Program, ASA — American Association of Anaesthetists, AUC — Area Under the ROC Curve, BIMS — Вleeding Independently associated with Mortality after noncardiac Surgery, ESC — the European Society of Cardiology, МАСЕ — major adverse cardovascular events, NSQIP MICA — the National Surgical Quality Improvement Program Myocardial Infarction & Cardiac Arrest, POSSUM — Physiological and Operative Severity Score for the enUmeration of Mortality and morbidity, RCRI или rRCRI — Revised Cardiac Risk Index, SORT — Surgical Outcome Risk Tool, VTE-Bleed — Venous ThromboEmbolism and Bleeding.

Рис. 3 Cтратификация риска послеоперационных осложнений с использованием шкал и индексов (%).
Примечание: ASA — American Association of Anaesthetists, BIMS — Вleeding Independently associated with Mortality after noncardiac Surgery, ESC — the European Society of Cardiology, NSQIP MICA — the National Surgical Quality Improvement Program Myocardial Infarction & Cardiac Arrest, POSSUM — Physiological and Operative Severity Score for the enUmeration of Mortality and morbidity, rRCRI — Revised Cardiac Risk Index, SORT — Surgical Outcome Risk Tool, VTE-Bleed — Venous ThromboEmbolism and Bleeding.
Заключение
Залогом успеха в предупреждении развития ПО является точность их прогнозирования. Результаты выполненного исследования показали, что развитие MACE в настоящее время происходит не столь часто, в то время как AnyCVE встречаются с частотой >10% и составляют до 2/3 осложнений 2-5 ст. по классификации Clavien-Dindo. Для того, чтобы своевременно предпринять профилактические мероприятия и сократить длительность пребывания пациента в стационаре, важна предоперационная стратификация не только серьезных осложнений, включающих смерть от сердечных причин, ИМ, инсульт, но и AnyCV E. Мы продемонстрировали, что модели с использованием прогностических шкал и индексов, рекомендованных для оценки риска развития ССО, преимущественно имели качество не выше хорошего в стратификации риска развития AnyCV E. Результаты настоящего исследования свидетельствуют о необходимости усовершенствования используемых в клинической практике прогностических шкал и индексов и разработки новых инструментов для своевременного прогнозирования и профилактики любых ССО AnyCV E.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Halvorsen S, Mehilli J, et al. Cassese Salvatore, et al. 2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery. Eur Heart J. 2022; 43(39):3826-924. doi:10.1093/eurheartj/ehac270.
2. Мурашко С. С., Пасечник И. Н., Бернс С. А. Сердечно-сосудистые осложнения в некардиальной хирургии: что мы о них знаем? Кремлевская медицина. Клинический вестник. 2019;4:90-7. doi:10.26269/rg71-m772.
3. Global patient outcomes after elective surgery: prospective cohort study in 27 low-, middle- and high-income countries. Br J Anaesth. 2017;119(3):553. doi:10.1093/bja/aew472.
4. Vascular Events in Noncardiac Surgery Patients Cohort Evaluation (VISION) Study Investigators, Spence J, LeManach Y, et al. Association between complications and death within 30 days after noncardiac surgery. CMAJ. 2019;191(30):E830-7. doi:10.1503/cmaj.190221.
5. Bosco E, Hsueh L, McConeghy KW, et al. Major adverse cardiovascular event definitions used in observational analysis of administrative databases: a systematic review. BMC Med Res Methodol. 2021;21(1):241. doi:10.1186/s12874-021-01440-5.
6. Thiele RH, Theodore DJ, Gan TJ. Outcome of Organ Dysfunction in the Perioperative Period. Anesth Analg. 2021;133(2):393-405. doi:10.1213/ANE.0000000000005603.
7. NeuroVISION Investigators. Perioperative covert stroke in patients undergoing non-cardiac surgery (NeuroVISION): a prospective cohort study. Lancet. 2019;394(10203):1022-9. doi:10.1016/S0140-6736(19)31795-7.
8. Harris EP, MacDonald DB, Boland L, et al. Personalized perioperative medicine: a scoping review of personalized assessment and communication of risk before surgery. Can J Anaesth. 2019;66(9):1026-37. doi:10.1007/s12630-019-01432-6.
9. Сумин А. Н., Дупляков Д. В., Белялов Ф. И. и др. Рекомендации по оценке и коррекции сердечно-сосудистых рисков при несердечных операциях. Российский кардиологический журнал. 2023;28(8):5555. doi:10.15829/1560-4071-2023-5555. EDN MQQWMW
10. Glance LG, Faden E, Dutton RP, et al. Impact of the Choice of Risk Model for Identifying Low-risk Patients Using the 2014 American College of Cardiology/American Heart Association Perioperative Guidelines. Anesthesiology. 2018;129(5):889-900. doi:10.1097/ALN.0000000000002341.
11. Manekk RS, Gharde P, Gattani R, Lamture Y. Surgical Complications and Its Grading: A Literature Review. Cureus. 2022; 14(5):e24963. doi:10.7759/cureus.24963.
12. Мурашко С. С., Бернс С. А., Пасечник И. Н. Сердечно-сосудистые осложнения в некардиальной хирургии: что остается вне поля зрения? Кардиоваскулярная терапия и профилактика. 2024;23(1):3748. doi:10.15829/1728-8800-2024-3748.
13. Белялов Ф. И. Прогнозирование заболеваний с помощью шкал. Комплексные проблемы сердечно-сосудистых заболеваний. 2018;7(1):84-93. doi:10.17802/2306-1278-2018-7-1-84-93.
14. Заболотских И. Б., Трембач Н. В., Магомедов М. А. и др. Структура и частота сопутствующих заболеваний и связанных с ними послеоперационных осложнений: национальное наблюдательное многоцентровое исследование STOPRISK. Вестник интенсивной терапии имени А. И. Салтанова. 2023;(3):43-57. doi:10.21320/1818-474X-2023-3-43-57.
15. De la Plaza Llamas R, Ramia JM. Cost of postoperative complications: How to avoid calculation errors. World J Gastroenterol. 2020;26(21):2682-90. doi:10.3748/wjg.v26.i21.2682.
16. Smilowitz NR, Berger JS. Perioperative Cardiovascular Risk Assessment and Management for Noncardiac Surgery: A Review. JAMA. 2020;324(3):279-90. doi:10.1001/jama.2020.7840.
17. Peterson BR, Cotton A, Foy AJ. Reevaluating the Cardiac Risk of Noncardiac Surgery Using the National Surgical Quality Improvement Program. Am J Med. 2021;134(12):1499-105. doi:10.1016/j.amjmed.2021.07.016.
18. Соколова М. М., Киров М. Ю., Шелыгин К. В. Послеоперационный делирий: современные аспекты диагностики, профилактики и терапии. Кубанский научный медицинский вестник. 2018;25(6):184-91. doi:10.25207/1608-6228-2018-25-6-184-191.
19. Aldecoa C, Bettelli G, Bilotta F, et al. European Society of Anaesthesiology evidence-based and consensus-based guideline on postoperative delirium [published correction appears in Eur J Anaesthesiol. 2018;35(9):718-719]. Eur J Anaesthesiol. 2017;34(4):192-214. doi:10.1097/EJA.0000000000000594.
20. Smilowitz NR, Gupta N, Guo Y, et al. Trends in Perioperative Venous Thromboembolism Associated with Major Noncardiac Surgery. TH Open. 2017;1(2):e82-e91. doi:10.1055/s-0037-1605360.
21. Dobrev D, Aguilar M, Heijman J, et al. Postoperative atrial fibrillation: mechanisms, manifestations and management. Nat Rev Cardiol. 2019;16(7):417-36. doi:10.1038/s41569-019-0166-5.
22. Sessler DI, Khanna AK. Perioperative myocardial injury and the contribution of hypotension. Intensive Care Med. 2018;44(6):811-22. doi:10.1007/s00134-018-5224-7.
23. Wright DE, Knuesel SJ, Nagarur A, et al. Examining Risk: A Systematic Review of Perioperative Cardiac Risk Prediction Indices. Mayo Clin Proc. 2019;94(11):2277-90. doi:10.1016/j.mayocp.2019.03.008.
24. Wong DJN, Oliver CM, Moonesinghe SR. Predicting postoperative morbidity in adult elective surgical patients using the Surgical Outcome Risk Tool (SORT). Br J Anaesth. 2017;119(1):95-105. doi:10.1093/bja/aex117.
25. Wong DJN, Harris S, Sahni A, et al. Developing and validating subjective and objective risk-assessment measures for predicting mortality after major surgery: An international prospective cohort study. PLoS Med. 2020;17(10):e1003253. doi:10.1371/journal.pmed.1003253.
26. Protopapa KL, Simpson JC, Smith NCE, et al. Development and validation of the Surgical Outcome Risk Tool (SORT), Br J Surg. 2014;101(13):1774-83. doi:10.1002/bjs.9638.
27. Kim TI, Brahmandam A, Skrip L, et al. Surgery for the Very Old: Are Nonagenarians Different? Am Surg. 2020;86(1):56-64. doi:10.1177/000313482008600129.
28. Kim S, Park J, Kwon JH, et al. The Charlson Comorbidity Index is associated with risk of 30-day mortality in patients with myocardial injury after non-cardiac surgery. Sci Rep. 2021;11(1): 18933. doi:10.1038/s41598-021-98026-4.
29. Moraes CMT, Corrêa LM, Procópio RJ, et al. Tools and scores for general and cardiovascular perioperative risk assessment: a narrative review. Rev Col Bras Cir. 2022;49:e20223124. doi:10.1590/0100-6991e-20223124.
30. Che L, Xu L, Huang Y, Yu C. Clinical utility of the revised cardiac risk index in older Chinese patients with known coronary artery disease. Clin Interv Aging. 2017;13:35-41. doi:10.2147/CIA.S144832.
31. Chaiwat O, Chanidnuan M, Pancharoen W, et al. Postoperative delirium in critically ill surgical patients: incidence, risk factors, and predictive scores [published correction appears in BMC Anesthesiol. 2019;19(1):58]. BMC Anesthesiol. 2019;19(1):39. doi:10.1186/s12871-019-0694-x.
32. Pandor A, Tonkins M, Goodacre S, et al. Risk assessment models for venous thromboembolism in hospitalised adult patients: a systematic review. BMJ Open. 2021;11(7):e045672. doi:10.1136/bmjopen-2020-045672.
33. Roshanov PS, Eikelboom JW, Sessler DI, et al. Bleeding Independently associated with Mortality after noncardiac Surgery (BIMS): an international prospective cohort study establishing diagnostic criteria and prognostic importance. Br J Anaesth. 2021;126(1):163-71. doi:10.1016/j.bja.2020.06.051.
34. Tafur AJ, Clark NP, Spyropoulos AC, et al. Predictors of Bleeding in the Perioperative Anticoagulant Use for Surgery Evaluation Study. J Am Heart Assoc. 2020;9(19):e017316. doi:10.1161/JAHA.120.017316.
Об авторах
С. С. МурашкоРоссия
Мурашко Светлана Степановна — к.м.н., зам. главного врача, доцент кафедры анестезиологии и реаниматологии.
Москва
С. А. Бернс
Россия
Бернс Светлана Александровна — д.м.н., профессор, зав. кафедрой терапии и общей врачебной практики.
Москва
И. Н. Пасечник
Россия
Пасечник Игорь Николаевич — д.м.н., профессор, зав. кафедрой анестезиологии и реаниматологии.
Москва
Дополнительные файлы
Что известно о предмете исследования?
- В настоящее время нет прогностических инструментов для оценки риска развития любых сердечно-сосудистых осложнений (ССО) после некардиальных операций.
Что добавляют результаты исследования?
- Проведена стратификация риска широкого спектра послеоперационных хирургических и любых ССО (AnyCVE — Any Cardio-Vascular Events) с использованием рекомендованных в настоящее время шкал и индексов.
- Впервые проведена оценка прогностической значимости наиболее широко используемых шкал и индексов в предсказании вероятности развития любых ССО (AnyCVE).
- Прогностическая ценность рекомендованных шкал и индексов в оценке риска любых ССО (AnyCVE), не только MACE (Major Adverse Cardiac Events), преимущественно не выше хорошего качества, что свидетельствует о необходимости усовершенствования имеющихся и разработки новых прогностических инструментов.
Рецензия
Для цитирования:
Мурашко С.С., Бернс С.А., Пасечник И.Н. Стратификация риска хирургических и сердечно-сосудистых осложнений в некардиальной хирургии: прогностическая значимость рекомендуемых шкал. Кардиоваскулярная терапия и профилактика. 2024;23(7):4016. https://doi.org/10.15829/1728-8800-2024-4016. EDN: MCKFPK
For citation:
Murashko S.S., Berns S.A., Pasechnik I.N. Risk stratification of surgical and cardiovascular complications in non-cardiac surgery: prognostic value of recommended scales. Cardiovascular Therapy and Prevention. 2024;23(7):4016. (In Russ.) https://doi.org/10.15829/1728-8800-2024-4016. EDN: MCKFPK
JATS XML

























































